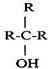Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Ориентация при электрофильном замещении в бензольном ядре
Однозамещённый бензол изомеров не имеет. При вступлении в молекулу второго заместителя могут образоваться три изомера (о-, м-, п-). Место вступления нового заместителя определяется природой уже имеющегося в ароматическом ядре заместителя. Их можно разделить на две группы. Заместители I рода - алкильные радикалы, группы ОН, NН2, галогены - доноры электронов, они активизируют ядро, облегчают введение нового заместителя, реакции электрофильного замещения протекают легче, чем в бензоле. Заместители I рода направляют преимущественно в орто- и пара- положения. Заместители II рода - направляют преимущественно в мета- положение - это мета -ориентанты - NО2, SОзН, СООН, СN и другие. Заместители II рода акцепторы электронов, оттягивают электронную плотность из ядра, уменьшая его активность в реакциях электрофильного замещения. Например:
Пример. Получить м-метилбензолсульфокислоту из бензола. Формула а) SОзН - заместитель II рода, м-ориентант б) СНз - заместитель I рода, направляет вторую частицу в орто- или пара- положения. Для того, чтобы получить мета- замещённый бензол, необходимо вначале ввести сульфогруппу, а затем метильную группу.
Если необходимо получить соединение, имеющее в м-положении два заместителя I рода, в первую очередь вводится заместитель, который является ориентантом нужного вам положения. В этом случае сначала обязательно вводится заместитель II рода, из которого в дальнейшем можно получить требуемый заместитель I рода. Пример. Из бензола получить м-хлоранилин.
Вопросы для самоконтроля знаний по разделу «Углеводороды»
1 Какие из приведенных соединений являются гомологами метана: С2Н2, СзН6, С4Н10, С7Н16,С6Н6, С5Н12? 2 Какие атомы углерода называют первичными, вторичными, третичными, четвертичными? Приведите формулы соединений, содержащих эти атомы. 3 Назовите по систематической номенклатуре следующие углеводороды:
4 Напишите структурные формулы следующих углеводородов: а) 3,3 – диметилпентан; 6)3,5- диметил-4-этилгексен-2; в) 3 - метилпентин-1. 5 Напишите структурные формулы изомерных углеводородов следующих алканов, алкенов, ароматических углеводородов состава: С6Н14, С5Н10, С8Н10. Назовите.
6. Осуществите схемы превращений: а) Метан → ацетилен → бензол → нитробензол. б) Этилен → этилхлорид → бутан -→ бутен – 1. в) Ацетилен → этилен → бутан → бутадиен 1.3. 7 Какой ароматический углеводород получится при каталитической дегидроциклизации гептана? 8 В каких условиях осуществляются следующие превращения: а) Толуол б) Бутен в) Бутен - 1 9 С помощью каких реакций можно различить: а) стирол и этилбензол; б) бензол и толуол; в) этилен и ацетилен? 10 Выведите молекулярную формулу углеводорода, содержащего: ω (С) = 85,7% и ω (Н) = 14,3%. Плотность паров по водороду равна 21. Галогенопроизводные
Производные углеводородов (алканов, алкенов, циклоалканов, ароматических углеводородов), в молекулах которых один или несколько атомов водорода замещены галогеном, называются галогенпроизводными.
В ненасыщенных галогенпроизводных начало нумерации определяет двойная связь - она старшая.
При изучении способов получения галогенпроизводных можно использовать материал прошлых тем: галогенирование алканов, алкенов, алкинов, алкадиенов, циклоалканов, ароматических углеводородов, и их получение. При изучении химических свойств могут быть также использованы методические рекомендации для изучения этих же тем. Следует обратить внимание на различные реакции галогенпроизводных с водными растворами щелочей (реакция замещения с образованием спиртов) и с их спиртовыми растворами (реакция дегидрогалогенирования с образованием непредельных углеводородов). Спирты (Алкоголи). Фенолы
Соединения, в которых группа (ОН) непосредственно связана: а) с углеводородным радикалом, называются спиртами R – ОН; б) с ароматическим радикалом, называются фенолами АrОН.. По количеству гидроксильных групп (ОН) эти соединения делятся на: одноатомные - одна гидроксигруппа; двухатомные - две гидроксигруппы; трёхатомные — три; многоатомные - гидроксигрупп более трёх. В зависимости от того, при каком атоме углерода находится гидроксил, спирты делятся на:
а) первичные R-СН2ОН
Названия спиртов производят от названия алканов с добавлением суффикса – ол. Главную цепь нумеруют с того конца, к которому ближе расположена гидроксильная группа. СНзОН – метанол
СН3СН2ОН – этанол
СНзСН2СН2ОН – пропанол - 1 (первичный спирт)
СНз-СН-СНз- пропанол - 2 или изопропиловый спирт (вторичный спирт)
Методы получения спиртов
1 Присоединение воды к алкенам (гидратация)
2 Гидролиз галогенопроизводных (с водой или водным раствором щелочей)
СН3СН2Вr + НОН → СН3СН2ОН + НВr
Если в молекуле имеются 2 атома галогенов, расположенные у разных атомов углерода, то в результате реакции образуются двухатомные спирты.
3 Восстановление альдегидов и кетонов
Химические свойства спиртов
1 Взаимодействие со щелочными металлами (спирты проявляют кислотные свойства)
2СН3-СН2ОН + 2Nа → 2СН3СН2ОNа + Н2 этилат (алкоголят) натрия
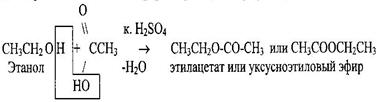
2 Образование простых эфиров СН3СН2ONа + С2Н5Сl → СН3-СН2-О-СН2-СН3+NаСl диэтиловый эфир 3 Образование сложных эфиров - реакция этерификации
4 Замена гидроксила на галоген
СНзОН + НВr → СН3Вr + Н2О 5 Отщепление воды а) внутримолекулярная дегидратация (по правилу Зайцева)
б) межмолекулярная дегидратация
6 Окисление спиртов а) окисление первичных спиртов: в мягких условиях приводит: к образованию альдегидов, в жёстких условиях - к образованию кислот.
При окислении б) при окислении вторичных спиртов образуются кетоны
1 Гидролиз галогенопроизводных
2 Кумольный метод (на Омском заводе СК)
Более новый способ - циклогекановый:
Химические свойства фенола
Как у спиртов, так и у фенолов имеется гидроксильная группа, которая также проявляет кислотные свойства. Группа ОН - ориентант I рода повышает электронную плотность в ароматическом ядре, ароматическое ядро увеличивает подвижность атома водорода в гидроксигруппе. Реакции с участием гидроксигруппы: 1 Взаимодействие с раствором щёлочи
С6Н5ОН + NaOH → С6Н5ОNа +Н2О фенолят натрия
2 Образование простых эфиров
Реакции с участием ароматического ядра: 1 Галогенирование Фенолы галогенируются легче, чем бензол и его гомологи. В результате получаются орто- и пара- изомеры.
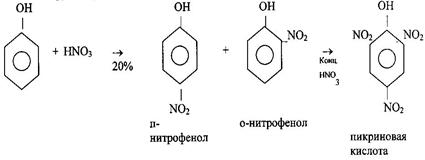
2 Нитрование Фенол нитруется разбавленной азотной кислотой
3 сульфирование
Альдегиды и кетоны
Для альдегидов и кетонов характерно наличие в молекуле карбонильной группы С=О. В альдегидах данная группа связана с радикалом и водородом – R-СНО, в кетонах с двумя радикалами – R-СО-R. Название альдегидов составляют из названий соответствующих алканов с добавлением суффикса «аль», у кетонов «он» с указанием положения карбонильной группы в углеродной цепи.
|
||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-19; просмотров: 601; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.193.129 (0.025 с.) |







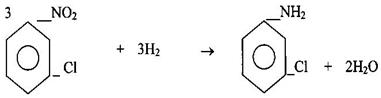



 метилциклогексан;
метилциклогексан; бутадиен 1.3;
бутадиен 1.3; бутин – 2.
бутин – 2.