
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Спектроскопические опыты и введения понятия квантового числаСодержание книги
Поиск на нашем сайте
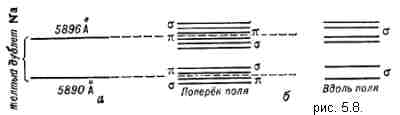
Согласно классической электродинамике, электрон должен непрерывно излучая терять энергию и очень скоро упасть на ядро. Однако атомы стабильны и излучают спектральные линии только строго определенной частоты. Бор предположил, что в стационарных состояниях атом не излучает, а излучение возникает только когда электрон переходит с одного энергетического уровня на другой. Это позволило Бору объяснить распределение частот излучения атома водорода, но он не мог ничего сказать об интенсивности и поляризации излучения. Чтобы восполнить этот пробел Бор сформулировал принцип соответствия: результаты квантовой теории должны асимптотически стремиться к классическим в области больших квантовых чисел. Бор предложил рассматривать фиктивный классический атом в котором электрон непрерывно испускает весь набор частот. Реальный атом в стационарном состоянии не излучает. Оказывается, что каждой частоте фиктивного атома соответствует определенный переход электрона с одного энергетического уровня на другой в квантовом атоме, приводящий к испусканию излучения той же частоты. То есть, в области больших значений квантовых чисел имеется хорошее соответствие между частотами излучения, испускаемого по классическим законам и частотам, которые может излучать в процессе квантового перехода электрон. Если классический фиктивный атом испускает все частоты непрерывно и одновременно, реальный атом может испускать при каждом отдельном акте излучения лишь одну из них. Подтвердив одинаковость предсказаний классической и квантовой теорий в отношении частот, Бор допустил, что предсказания классической теории в отношении интенсивности и поляризации излучения фиктивных атомов будут справедливы и для реальных атомов (принцип соответствия). Таким образом, принцип соответствия позволил приближенно вычислять интенсивность линий атомных спектров. Но, несмотря на успехи квантовой механики, она не могла в то время объяснить все факты спектроскопии. В частности в спектрах атомов существовали «лишние» линии, происхождение которых не могли объяснить. Например, в 1896 г. Петер Зееман открыл, что основные спектральные линии расщеплялись в магнитном поле на несколько компонент, то есть имели «тонкую структуру» (эффект Зеемана, см. рис. 5.8. расщепление спектральных линий атома натрия в магнитном поле). Чтобы дать объяснение спектроскопическим явлениям ввели понятие квантовых чисел.
Квантовые числа – энергетические параметры, определяющие состояние электрона и тип атомной орбитали, на которой он находится. Для характеристики состояния электрона в атоме используют четыре квантовых числа. 1. Главное квaнтовое число n определяет общую энергию электрона и степень его удаления от ядра (номер энергетического уровня); оно принимает положительные целочисленные значения, начиная с 1 (n = 1, 2, 3,...) Если использовать для описания квантовых чисел понятия механики, то орбитальное или главное квантовое число является орбитальным моментом количества движения 2. Орбитальное (побочное или азимутальное) квантовое число l определяет форму атомной орбитали. Оно может принимать целочисленные значения от 0 до n -1. 3. Магнитное квантовое число m определяет направление орбитали в пространстве. Его значения изменяются от + l до - l. Например, при l = 1 число m принимает 3 значения: +1, 0, -1, поэтому существуют 3 типа р-орбиталей перпендикулярно ориентированных в пространстве: px, py, pz. 4. Спиновое квантовое число s может принимать лишь два возможных значения +1/2 и –1/2. Его открыли Гаудсмит и Уленбек, которые при анализе атомных спектров пришли к выводу, что помимо орбитального момента количества движения электрон в атоме обладает еще и собственным моментом Набор четырех значений квантовых чисел полностью характеризует состояние электрона в атоме. Согласно принципу запрета Паули для каждого набора квантовых чисел в атоме в фиксированный Момент времени существует не более одного электрона с соответствующим набором. Квантовая теория поля Квантовая механика позволяла описать многие атомные явления при помощи дискретного набора значений энергии, момента, но электромагнитное поле по-прежнему описывалось классическими уравнениями Максвелла, т.е. рассматривалось как непрерывное поле. В квантовой теории поля, в отличие от классической электродинамики, поле рассматривается, как состоящее из виртуальных частиц – квантов. Эта особенность обуславливает второе отличие полей от частиц: поле может порождаться и поглощаться, в то время как идея возникновения и уничтожения частиц чужда квантовой механике. В квантовой теории поля испускание и поглощение электромагнитных волн описывается как рождение и уничтожение фотона. Рождаться и исчезать могут не только фотоны, взаимопревращаемость частиц является универсальным свойством микромира. В результате столкновений при высоких энергиях одни частицы превращаются в другие. Квантовая механика является низкоэнергетическим приближением квантовой теории поля, когда энергии недостаточно для взаимопревращений частиц. Чтобы определить количество энергии, достаточной для превращения частиц, нужно воспользоваться отношением между массой и энергией, установленным в специальной теории относительности:
Энергия, необходимая для образования новой частицы не может быть меньше
|
||||
|
Последнее изменение этой страницы: 2017-02-10; просмотров: 396; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.116.24.111 (0.009 с.) |

 , где р – импульс, а r – расстояние до ядра.
, где р – импульс, а r – расстояние до ядра.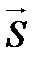 =±½. Это число соответствует двум возможным ориентациям магнитного момента электрона.
=±½. Это число соответствует двум возможным ориентациям магнитного момента электрона.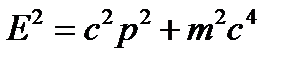 .
.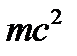 . Если система состоит из медленно движущихся частиц, то их энергия недостаточна для образования новых частиц. Сказанное относится к массивным частицам, но у фотона масса покоя равна нулю и для его образования не требуется больших релятивистских энергий. В квантовой теории поля фотон играет особую роль – он является частицей-переносчиком взаимодействия.
. Если система состоит из медленно движущихся частиц, то их энергия недостаточна для образования новых частиц. Сказанное относится к массивным частицам, но у фотона масса покоя равна нулю и для его образования не требуется больших релятивистских энергий. В квантовой теории поля фотон играет особую роль – он является частицей-переносчиком взаимодействия.


