
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Часть II. Молекулярная физика и термодинамика
Тема 1. Уравнение состояния идеального газа. Состояние системы задается термодинамическими параметрами – совокупностью физических величин, характеризующих свойства термодинамической системы, например, давлением р, объемом V и температурой Т. Между этими параметрами существует определенная связь, называемая уравнением состояния. Для идеального газа уравнением состояния является уравнение Клапейрона – Менделеева:
где m – масса газа,
R – универсальная газовая постоянная, (Идеальным называется такой газ, в котором считается, что собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда, в котором он находится, силы взаимодействия между молекулами газа отсутствуют, а столкновения между молекулами газа абсолютно упругие.) Исходя из уравнения Клапейрона – Менделеева и понятия концентрации n (n – число молекул в единице объема:
где
Тема 2. Термодинамические процессы. Изопроцессы. Любое изменение в системе, связанное с изменением ее термодинамических параметров, называется термодинамическим процессом. Из уравнения Клапейрона – Менделеева следует, что Если в термодинамическом процессе один из параметров газа ( Процесс, протекающий при постоянном давлении, называется изобарным. Из объединенного газового закона для изобарного процесса следует:
Процесс, протекающий при постоянном объеме, называется изохорным. Из объединенного газового закона для изохорного процесса следует:
Процесс, протекающий при постоянной температуре, называется изотермическим. Для изотермического процесса:
Тема 3. Основное уравнение молекулярно-кинетической теории Идеального газа.
Основное уравнение молекулярно-кинетической теории идеального газа связывает термодинамические параметры газа с параметрами, характеризующими движение его молекул. Так, давление газа, как следствие соударений молекул газа со стенками сосуда, определяется, согласно основному уравнению молекулярно-кинетической теории идеального газа, кинетической энергией поступательного движения молекул газа.
Выделив на стенке сосуда элементарную площадку D S (рис. 1), определяют давление газа p на эту площадку. Построив цилиндр с основанием D S и высотой 1/6 части всех N молекул, содержащихся в объеме выделенного цилиндра ( При столкновении с площадкой D S эти молекулы передадут ей импульс D P:
что соответствует, согласно второму закону Ньютона, действию силы F:
Тогда давление газа, оказываемое им на стенки сосуда:
Однако, молекулы газа движутся с различными скоростями
Так как
где Е – суммарная кинетическая энергия всех молекул газа, Таким образом, получены два эквивалентных уравнения:
связывающие кинематические параметры движения отдельных молекул газа с термодинамическими параметрами газа в целом, каждое из которых называют основным уравнением молекулярно-кинетической теории идеального газа.
Из сравнения между собой уравнений
то есть еще одно уравнение, связывающее термодинамический параметр газа (Т) со средней кинетической энергией молекулы одноатомного газа С другой стороны, величина средней кинетической энергии молекул газа
|
||||||
|
Последнее изменение этой страницы: 2017-02-07; просмотров: 134; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.16.212.99 (0.007 с.) |
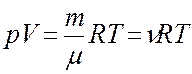 ,
,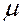 – молярная масса (масса одного моля вещества),
– молярная масса (масса одного моля вещества),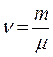 – количество вещества,
– количество вещества,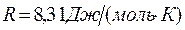 .
.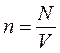 , где N – число всех молекул газа), можно получить уравнение состояния идеального газа в ином виде:
, где N – число всех молекул газа), можно получить уравнение состояния идеального газа в ином виде: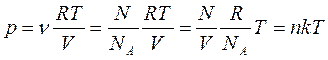 , то есть
, то есть 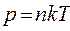 ,
,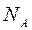 – постоянная Авогадро – число молекул в одном моле вещества,
– постоянная Авогадро – число молекул в одном моле вещества,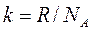 ,
, 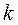 – постоянная Больцмана.
– постоянная Больцмана.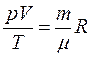 , то есть для данной массы газа
, то есть для данной массы газа 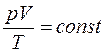 в любом термодинамическом процессе, что является объединенным газовым законом.
в любом термодинамическом процессе, что является объединенным газовым законом.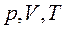 ) не изменяется, то такой процесс называется изопроцессом.
) не изменяется, то такой процесс называется изопроцессом.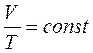 (уравнение изобарного процесса).
(уравнение изобарного процесса).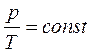 (уравнение изохорного процесса).
(уравнение изохорного процесса).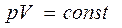 (уравнение изотермического процесса).
(уравнение изотермического процесса).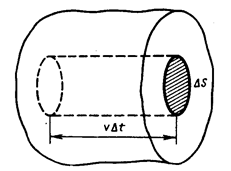 При выводе основного уравнения молекулярно-кинетической теории идеального газа полагают, что соударения молекул газа со стенками сосуда являются абсолютно упругими. Тогда, при соударении одна молекула газа массой m 0, движущаяся перпендикулярно стенке сосуда со скоростью
При выводе основного уравнения молекулярно-кинетической теории идеального газа полагают, что соударения молекул газа со стенками сосуда являются абсолютно упругими. Тогда, при соударении одна молекула газа массой m 0, движущаяся перпендикулярно стенке сосуда со скоростью 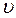 , передает ей импульс
, передает ей импульс 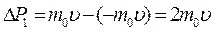 .
.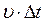 (рис. 1), учитывают, что число молекул, способных за время D t достигнуть площадки D S соответствует Рис. 1
(рис. 1), учитывают, что число молекул, способных за время D t достигнуть площадки D S соответствует Рис. 1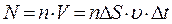 , где n – концентрация молекул). Коэффициент 1/6 учитывает, что из всех N молекул, движущихся хаотично вдоль трех (x, y, z) взаимно перпендикулярных направлений, только их 1/6 часть движется по направлению к площадке D S. Тогда число ударов молекул, движущихся в данном направлении, о площадку D S за время D t будет равно:
, где n – концентрация молекул). Коэффициент 1/6 учитывает, что из всех N молекул, движущихся хаотично вдоль трех (x, y, z) взаимно перпендикулярных направлений, только их 1/6 часть движется по направлению к площадке D S. Тогда число ударов молекул, движущихся в данном направлении, о площадку D S за время D t будет равно: 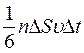 .
.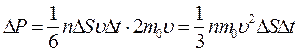 ,
,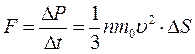 .
.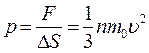 .
.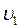 ,
, 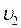 ,….
,…. 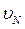 , что можно учесть в полученной формуле, введя понятие средней квадратичной скорости движения молекул
, что можно учесть в полученной формуле, введя понятие средней квадратичной скорости движения молекул 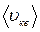 :
: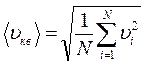 , тогда
, тогда 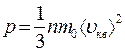 .
.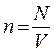 , а
, а 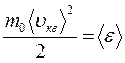 – средняя кинетическая энергия движения одноатомной молекулы, то получим:
– средняя кинетическая энергия движения одноатомной молекулы, то получим: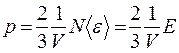 ,
,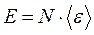 .
.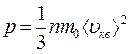 и
и 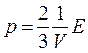 ,
,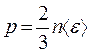 и
и 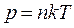 следует, что
следует, что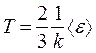 ,
,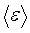 .
.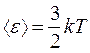 .
.


