
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Вопрос. Второе начало термодинамики.
Первое начало термодинамики, выражая закон сохранения и превращение энергии. Не позволяет при этом установить направление протекания термодинамических процессах. Второе начало термодинамики дает ответ на вопрос какие процессы возможны в природе а какие нет. Используя понятия энтропии и неравенство Клаузиуса
Вопрос. Цикл Карно. Основываясь на второе начало термодинамики Карно вывел следующие теорему из все периодических действующих тепловых машин имеющих одинаковую температуры нагревателей Т1 и холодильников Т2 наибольшим КПД обладают обратимые машины при этом КПД машин работающих при одинаковых температурах Т1 и Т2 равны друг другу и не зависят от природы рабочего тела а определяются только температурами. Карно проанализировал цикл состоящий из двух изотерм и двух адиабат.
Изотермическое расширение и сжатие 1-2, 3-4. А адиабатное расширение 2-3, 4-1. При изотермическом расширении U=const и количество теплоты получаемым газом Q1= работе расширения.
|
|||||
|
Последнее изменение этой страницы: 2017-02-05; просмотров: 260; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.88.249 (0.004 с.) |
 второе начало термодинамики можно сформулировать как закон возрастания энтропии: любой необратимый процесс в замкнутой системе происходит так что энтропия при этом возрастает или другими словами в процессах проходящих в замкнутых системах энтропия не убывает. Формула Больцмана позволяет объяснит второе начало термодинамики возрастание энтропии означает переход системы из менее вероятных в более вероятные.
второе начало термодинамики можно сформулировать как закон возрастания энтропии: любой необратимый процесс в замкнутой системе происходит так что энтропия при этом возрастает или другими словами в процессах проходящих в замкнутых системах энтропия не убывает. Формула Больцмана позволяет объяснит второе начало термодинамики возрастание энтропии означает переход системы из менее вероятных в более вероятные.  Термодинамическая вероятность состояния системы это число способов которые могут быть реализовано данное состояние
Термодинамическая вероятность состояния системы это число способов которые могут быть реализовано данное состояние  . Реальные процессы необратимы поэтому можно утверждать что все процессы замкнутой системы ведут к увеличению энтропии. Существуют еще 2 формулировки второго начало термодинамики. Формулировка по Кельвину невозможен круговой процесс, единственным результатом которого является превращение теплоты полученный от нагревателя в эквивалентную ей работу. По Клаузиуса невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому. Первые два начала дают недостаточно сведений о поведении термодинамических систем при абсолютном 0 поэтому они дополняются третьим началом термодинамики или теоремой Нернста Планка энтропия всех тел в состоянии равновесия стремится к 0 по мере приближения температуры к нулю Кельвина
. Реальные процессы необратимы поэтому можно утверждать что все процессы замкнутой системы ведут к увеличению энтропии. Существуют еще 2 формулировки второго начало термодинамики. Формулировка по Кельвину невозможен круговой процесс, единственным результатом которого является превращение теплоты полученный от нагревателя в эквивалентную ей работу. По Клаузиуса невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому. Первые два начала дают недостаточно сведений о поведении термодинамических систем при абсолютном 0 поэтому они дополняются третьим началом термодинамики или теоремой Нернста Планка энтропия всех тел в состоянии равновесия стремится к 0 по мере приближения температуры к нулю Кельвина  .
.
 . При адиабатном расширении отсутствует тепло обмен а работа расширения совершается за счет изменения внутренней энергии
. При адиабатном расширении отсутствует тепло обмен а работа расширения совершается за счет изменения внутренней энергии  . Количество теплоты отданная газом при изотермическом сжатии равно работе сжатия
. Количество теплоты отданная газом при изотермическом сжатии равно работе сжатия  . Работа адиабатного сжатия
. Работа адиабатного сжатия  . Работа совершаемая в результате кругового процесса
. Работа совершаемая в результате кругового процесса  . КПД цикла
. КПД цикла 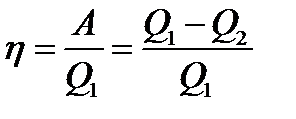 . Применив уравнение Пуассона КПД цикла Карно
. Применив уравнение Пуассона КПД цикла Карно  . То есть определяется температурами нагревателя и холодильника.
. То есть определяется температурами нагревателя и холодильника.


