
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Вопрос 31. Фазовые переходы 1 и 2 рода. ⇐ ПредыдущаяСтр 8 из 8
Фазой называется термодинамически-равновесное состояние в-ва, отличающееся по физич. св-вам от других возможных равновесных состояний. В пределах 1-го агрегатного состояния в-во может находится в нескольких фазах, отличающихся по св-ву. составу и строению. Фазовый переход, т.е. переход в-ва из одной фазы в другую всегда связан с качественными изменениями св-в в-ва. Различают фазовые переходы 1 и 2 рода: Фазовый переход первого рода (например: плавление, кристаллизация) всегда сопровождаются поглощением или выделением теплоты называемой теплотой фазового перехода. Фазовые переходы первого рода характеризуются постоянством температуры, а также изменением энтропии и объема кристаллической решетки, которая идет не на нагрев, а на разрыв межатомных связей. Фазовые переходы не связываемые с выделением или поглощением теплоты называются фазовыми переходами второго рода. Эти переходы характеризуются постоянством объема и энтропии, но скачко- образным изменением теплоемкости. Переходами второго рода являются: переход ферро магнитных веществ (например: железа, никеля) при определенном давлении и температуре в парамагнитное состояние. Переход металлов при низких температурах в сверхпроводящие состояние которое характеризуется скачко-образным уменьшением до нуля сопротивления.
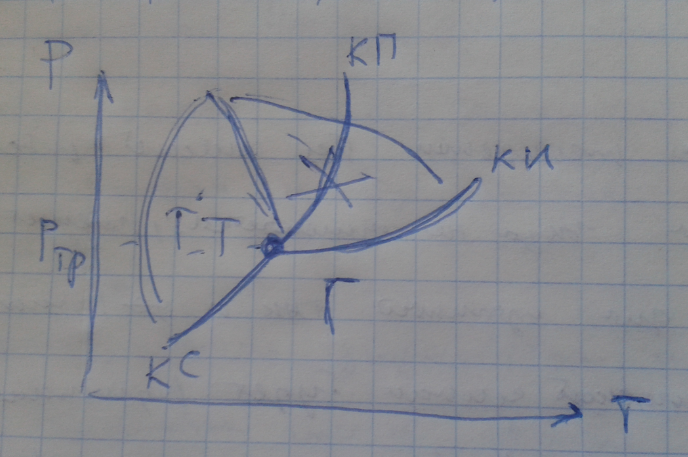
Вопрос 32. Диаграмма состояния. Тройная точка. Если система является однокомпонентной то есть состоящая из химически однородного вещества то понятие фазы совпадает с агрегатным состоянием. Соотношение между твердым жидким и газообразным состоянием определяется внешними условиями температурой и давлением. Для наглядности изображения фазовых превращений используется диаграмма состояния.
Точка в которой пересекается все три кривые то есть точка в которой одновременно существуют три фазы называется тройной точкой. Ки испарение Кп плавление Кс сублимация разделяющая поля на три области твердое тело жидкость газ. каждое вещество имеет одно тройную точку так например тройная точка воды 273,016 К ил 0,01С0 термодинамика дает метод расчета кривой равновесия двух фаз одного и то гоже вещества. Согласно уравнению Клаперона –Клаузиуса- Приводит к увеличению температуры и на оборот. При плавлении большинства веществ объем как правило возрастает что приводит к повышению температуры. Для некоторых веществ например вода чугун германий объем жидкой фазы меньше объема твердой фазы. Следовательно увеличение давления сопровождается понижением температуры плавления. (верхний пунктир)
|
||||
|
Последнее изменение этой страницы: 2017-02-05; просмотров: 2341; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.243.184 (0.003 с.) |
 . где L теплота фазового перехода. Данное уравнение позволяет определить наклоны кривых так как L и Т положительные то наклон задается знаком V2 –V1 при испарении жидкостей и сублимации твердых тел объем всегда возрастает следовательно повышение температуры
. где L теплота фазового перехода. Данное уравнение позволяет определить наклоны кривых так как L и Т положительные то наклон задается знаком V2 –V1 при испарении жидкостей и сублимации твердых тел объем всегда возрастает следовательно повышение температуры


