Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Глицин, его строение и роль в обмене веществ. Основные пути метаболизма глицина. Глицин как важнейший донор углеродных фрагментов для биосинтезов.Содержание книги
Поиск на нашем сайте
Основные пути метаболизма глицина. Глицин как важнейший донор углеродных фрагментов для биосинтезов. Глицин является единственной из всех входящих в состав белков аминок-т, в молекуле которой нет ассиметричного атома углерода. Г.незаменим в синтезе в боразовании белков,париновых нуклеотидов, гемма гемоглобина, парных желчных кислот, креатина, глутатиона.
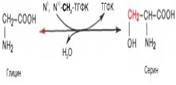
Серин легко превращается в пируват под действием сериндегидратазы. В связи с этим в тканях имеются условия для превращения глицина (через серин) в пируват. Этим путем осуществляется участие глицина в обмене углеводов. Глицин, его строение и роль в обмене веществ. При распаде глицина обр-ся СО2, NH3, метилентетрагидрофолиевая к-та.. катализ. глицинсинтазным комплексом. Биологическая роль: протеиногенная АК, исп. для синтеза пуринов, поставляя атомы углерода в положении 4, 5 и 7 пуринового остова; при коньюгации с холевой к-той обр-ся гликохолевая к-та; синтез гема (порфириновое кольцо) синтез липидов, синтез НАД. ФАД, синтез креатина (косп. N-метилглицин) синтез желчных кислот, уч. в глюконеогенезе. Уч. в синтезе глутатиона, в обезвреживании бензойной к-ты. Глицин - заменимая АК, основным источником к-й служит серии. Р-цию синтеза глицина из серина катализирует серин-оксиметилтрансфераза, коферментом является Н4-фолат. При образовании ПВК из глицина, глицин сначала превращ. в серин. а затем в ПВК.
Аспарагиновая и глутаминовая кислоты, строение, роль в метаболизме основные пути метаболизма, биологическое значение глутатиона. Глутамат и аспартат. Аспарагиновая к-та участвует в р-циях трансаминирования, в синтезе мочевины явл. донором NH2, в синтезе пуриновых и пиримидиновых оснований. синтезе аспарагина.
Глутаминовая к-та подверг прямому окислит. зезаминированию с образованием а-кетоглутората. Вступают в р-ции трансаминирования. Явл. субстратом для синтеза глютамина.к-й явл. транспортной формой аммиака, уч. в синтезе мочевины в печени, пуриновых оснований нуклеотидов, АК, аминосахаров, участвует в синтезе трипептида глутатиона, явл. субстратом для синтеза ГАМК.
Обе АК участ. в формир. третич. и четвертич. струк. белков, т.к. являются полярными заряженными АК, и в обр-ии гидратной об-ки белков, формировании актив. центров ферментов.
Глутатион - трипептид, состоящий из глутаминовой к-ты, цистеина, глицина. Связывает токсины с желчью, участвует в тканевых дыхательных процессах. Уч. в образовании "правильных" дисульфидных связей в белках и гормонах. Функционирут в кач-ве кофермента в различ. окислит-восст. р-циях.
Строение аргинина и гистидина. Их роль в обмене веществ. Аргинин и гистидин. Аргинин - образуется в ходе синтеза мочевины из карбомоилфосфата при уч. аспарагиновой к-ты и орнитина. Аргинин участвует в синтезе креатина. Участвует в образовании ионных связей и формир. гидратной оболочки ядра, явл-сь полярной положит заряженной. Из гистидина обр. а-кетоглуторат. Из гистидина путем декарбоксилирования. синтезируется гистамин. явл. медиатором воспаления и аллерг. р-ций. Имидазольная группа гистидина участ. в связ метллов в акт. центре многих ферментов.Гистидин способен превращ. вглутаминовую к-ту под дейст. гистидинаммиаклиазы и урокиназы.
S-аденозилметионин, его химическое строение и роль в метаболизме клетки. Липотропные факторы. S-денозилметионин. Его хим. строение и роль в метаболизме клетки. Активный метионин; донор метильных групп при трансметилировании. Аденозилметионин участвует в синтезе фосфатидилхолина, холина, адреналина, витамина В12. Обезвреживание биогенных аминов с участием О-метилтрансфераз, синтез адреналина из норадреналина, Обр-ся в рез-те АТФ-зависимой р-ции, катализ. метионинаденозилтрансферазой. после отщепления метильной группы обр. Sаденозилгомоцистеин.
|
|||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 529; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.22.242.110 (0.005 с.) |