
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Препарата лактатдегидрогеназы по Корнбергу
Реактивы. Фосфатный буфер, 0,1 М с рН 7,4*; пируват натрия, раствор 2∙10-2 М на 0,1 М фосфатном буфере с рН 7,4; НАД∙Н динатриевая соль, свежеприготовленный 6∙10-3 М раствор в дистиллированной воде. Оборудование. Пипетки вместимостью 0,1; 1 и 5 мл; стеклянная палочка; секундомер; СФ или ФЭК типа КФК-2. Материал. Разведенный продажный препарат фермента 0,2 мкг/мл. Кристаллический препарат в виде суспензии в 2,2 М растворе сульфата аммония, имеющий активность около 200 ФЕ/мг белка, разводят в 1000 раз 0,1 М фосфатным буфером с рН 7,4 перед опытом (1 ФЕ соответствует 1 мкмоль превращенного субстрата за 1 мин)[2].
Метод основан на непрерывном измерении скорости окисления НАД∙Н2, используемого на восстановление пирувата в реакции, катализируемой ЛДГ. По уменьшению экстинкции НАД∙Н2 при 340 нм рассчитывают количество превращенного субстрата за единицу времени. Лактатдегидрогеназа (ЛДГ) катализирует обратимое превращение пирувата в лактат:
Н
║ │ О ОН пируват лактат
Равновесие реакции сдвинуто вправо, поэтому при изучении ЛДГ удобнее использовать в качестве субстрата пируват и НАД∙Н2 и по скорости окисления последнего рассчитать активность этого фермента. Ход определения. В кювету спектрофотометра последовательно вносят 2,4 мл фосфатного буфера, 0,2 мл раствора НАД∙Н2 и 0,1 мл образца фермента. Перемешивают стеклянной палочкой и ставят в кюветодержатель. Устанавливают шкалу отсчета экстинкции на 0,400 и ручкой «щель» выводят стрелку гальванометра (при открытой шторке) на нуль. В течение 1 мин проверяют отсутствие неферментативного окисления НАД∙Н2 (в этом случае экстинкция не падает). Добавляет в кювету 0,3 мл раствора пирувата натрия (запускают реакцию), быстро перемешивают, ручкой «щель» при открытой шторке возвращают стрелку гальванометра к нулевой отметке и включают секундомер. Снимают показания экстинкции (падение ее, начиная от отметки 0,400) через каждые 30 с в течение 2-3 мин. Если условия реакции подобраны верно, то за каждые 30 с наблюдается примерно одинаковое уменьшение экстинкции. Расчет. Удельную активность ЛДГ х (мкмоль∙мин-1∙мг-1) рассчитывают по формуле ∆Емин3,0∙1000
х = ———————, 6,22∙0,02
где ∆Емин – изменение экстинкции в ходе реакции за 1 мин; 6,22 – коэффициент экстинкции 1 мкмоль НАД∙Н2 в 1 мл среды; 3,0 – объем инкубационной смеси, мл; 0,02 – количество белка в кювете, мкг; 1000 – коэффициент пересчета количества белка в миллиграммы. Оформление работы. Рассчитать удельную активность ферментного препарата, молекулярную активность ЛДГ (учитывая, что ее молекулярная масса 135000). Сделать вывод о качестве исследуемого препарата (сохранность исходной активности, %). Практическое значение работы. Принципы измерения активности лактатдегидрогеназы спектрофотометрическим методом непрерывного наблюдения используются при исследовании других ферментных препаратов, очищенных ферментов и в клинико-биохимических лабораториях при количественном определении активности ферментов в биологических жидкостях и биоптатах в норме и при патологии.
Работа 31. Фотоколориметрический метод исследования активности лактатдегидрогеназы в сыворотке крови по Севелу и Товареку
Реактивы. Лактат натрия, 0,45 М раствор или нейтрализованная гидроксидом натрия молочная кислота той же концентрации; пирофосфат натрия, 0,03 М раствор (Na4P2O7∙10H2O растворить в 50 мл воды, довести рН до 8,8 с помощью 1 М соляной кислоты и долить водой до 500 мл); НАД, свежеприготовленный раствор 3мг/мл; 2,4-динитрофенилгидразин, 0,2%-ный раствор в 1 М растворе соляной кислоты; гидроксид натрия, 0,4 М раствор; пируват натрия, раствор для построения калибровочного графика (содержит 11 мкг пирувата натрия или 8,8 мкг пировиноградной кислоты в 1 мл). Оборудование. Штатив с пробирками; пипетки вместимостью 0,1; 1 и 5 мл; ФЭК; водяная баня с лабораторным термометром. Материал. Сыворотка крови.
Метод основан на определении скорости образования пирувата в ходе окисления лактата с участием лактатдегидрогеназы сыворотки крови:
│ ║ ОН О лактат пируват
Пируват с 2,4-динитрофенилгидразином образует соответствующий гидразон, имеющий красно-бурое окрашивание в щелочной среде, интенсивность которого прямо пропорциональна содержанию кетокислоты:
Ход определения. Сыворотку крови разводят в 3 раза дистиллированной водой. Вносят в пробирку 0,1 мл разведенной сыворотки, 0,3 мл раствора НАД+ и ставят на 5 мин в водяную баню при 37˚С (для прогревания смеси). Во вторую пробирку добавляют 0,8 мл раствора пирофосфата натрия и 0,2 мл раствора лактата натрия и нагревают на водяной бане при 37˚С. Выливают содержимое второй пробирки в первую, быстро перемешивают стеклянной палочкой, не вынимая пробирки из бани, и отмечают время начала инкубации. Через 25 мин реакцию останавливают, прибавляя 0,5 мл раствора 2,4-ДНФГ, и оставляют пробирку на 20 мин при комнатной температуре (для образования гидразона). К смеси приливают 5 мл раствора гидроксида натрия, содержимое перемешивают стеклянной палочкой и через 10 мин (после развития окраски) измеряют экстинкцию опытной пробы против контрольной на ФЭКе при длине волны 520-560 нм (светофильтр зеленый) в кювете с толщиной слоя 1 см. Контрольную пробу готовят как опытную, но разведенную сыворотку добавляют после инкубации. Расчет. Активность фермента рассчитывают по калибровочному графику, условия построения которого приведены в таблице.
По оси ординат откладывают значения экстинкции, а по оси абсцисс – соответствующие им единицы активности ЛДГ, выраженные в ммоль/(ч∙л). Оформление работы. Рассчитать активность фермента в исследуемой сыворотке крови, сделать вывод о возможном изменении активности и его причинах. Практическое значение работы. Определение активности лактатдегидрогеназы используется в клинико-биохимических лабораториях для диагностики и установления прогноза заболевания. В норме активность фермента составляет 0,8-4,0 ммоль/(ч∙л) и возрастает, как правило, у больных с повреждением миокарда, скелетных мышц, почек, а также при анемиях, опухолевых поражениях, остром гепатите и т.д.
Работа 32. Определение активности щелочной фосфатазы в сыворотке крови по Боданскому
Фосфатазы – ферменты, отщепляющие фосфат от различных субстратов. Среди них имеются энзимы с неодинаковой специфичностью по отношению к субстратам. Щелочная фосфатаза действует в щелочной среде (чем отличается от фосфатаз, осуществляющих катализ в нейтральной или кислой средах) и является малоспецифичной. Реактивы. β-Глицерофосфат, щелочной раствор на мединаловом буфере с рН 8,6*; трихлоруксусная кислота, 10%-ный раствор; реактив молибдата аммония*; аскорбиновая кислота, 1%-ный раствор на 0,1 М растворе соляной кислоты; дигидрофосфат калия (навеску 0,4394 г KH2PO4, предварительно высушенного в эксикаторе над серной кислотой, взвешивают на аналитических весах и растворяют в колбе вместимостью 100 мл; затем этот раствор разводят в 100 раз и используют для построения калибровочной кривой). Оборудование. Штатив с пробирками; центрифуга лабораторная с центрифужными весами; пипетки вместимостью 0,2; 1 и 5 мл; водяная баня с лабораторным термометром; ФЭК.
Материал. Сыворотка крови.
Метод основан на фотоколориметрическом определении неорганического фосфора, отщепляемого от β-глицерофосфата под действием фосфатазы сыворотки крови в щелочной среде:
СН2ОН СН2ОН │ Фосфатаза │
│ рН 8,6 │ СН2ОН СН2ОН β-глицерофосфат глицерин
Неорганический фосфат определяют по образованию фосфомолибдата аммония с последующим восстановлением его в молибденовую синь аскорбиновой кислотой (см. работу 11). Ход определения. В две пробирки вносят по 1 мл раствора β-глицерофосфата и помещают на 5 мин в водяную баню при 37˚С. Затем в опытную пробирку добавляют 0,2 мл сыворотки крови, перемешивают и отмечают время начала инкубации в водяной бане. Через 1 час приливают в обе пробирки по 1,8 мл раствора трихлоруксусной кислоты, а в контрольную – еще 0,2 мл сыворотки крови. Перемешивают пробы, оставляют стоять 5 мин для осаждения белка. Центрифугируют содержимое обеих проб в течение 5 мин при 3000 об/мин. Отбирают в чистые пробирки по 1,5 мл надосадочной жидкости (для определения в ней неорганического фосфата Фн) и приливают по 1 мл реактива молибдата аммония и по 1 мл раствора аскорбиновой кислоты. Через 10 мин измеряют экстинкцию опытной и контрольной проб на ФЭКе, при длине волны 630-690 нм (красный светофильтр) в кювете с толщиной слоя 0,5 см против раствора реактивов (1,5 мл раствора трихлоруксусной кислоты и 1,5 мл дистиллированной воды). Расчет. Активность фермента рассчитывают по калибровочному графику, условия построения которого приведены в таблице.
По оси ординат откладывают значения экстинкции, а по оси абсцисс – соответствующие единицы щелочной фосфатазы, выраженные в ммоль/(ч∙л). Оформление работы. По полученным значениям экстинкции найти активность фермента. На основании этого сделать вывод о возможности изменения активности в исследуемой сыворотке и указать на предполагаемые причины. Практическое значение работы. В клинике используется определение активности щелочной фосфатазы в сыворотке крови в основном у больных с поражениями костной ткани и печени, особенно с явлениями задержки оттока желчи. В норме активность фермента составляет 0,5-1,3 ммоль/(ч∙л). Повышение активности в сыворотке крови наблюдается при рахите (гиповитаминозе D), опухолях костной ткани, гиперпаратиреозе, механической желтухе, вирусном гепатите и т.д., а снижение – при гипотиреозе, гиповитаминозе С и др.
Исследование изоферментов
Изоферменты отличаются друг от друга несколькими физико-химическими признаками и, в частности, зарядом молекул, поэтому электрофорез издавна используется для их разделения. Изоферменты лактатдегидрогеназы были открыты одними из первых. Различают пять типов изоферментов ЛДГ, которые в порядке подвижности к аноду обозначаются: ЛДГ1, ЛДГ2, ЛДГ3, ЛДГ4 и ЛДГ5. Каждый из них представляет собой тетрамер, отличающийся составом субъединиц (см. учебник, с.226, 438).
Работа 33. Разделение изоферментов лактатдегидрогеназы сыворотки крови методом электрофореза в полиакриламидном геле по Дитцу и Лубрано
Использование в качестве среды геля полиакриламида позволяет добиться высокого разрешения при электрофорезе белков и ферментов, поскольку этот гель играет роль молекулярного сита, что обеспечивает дополнительное разделение частиц по молекулярной массе.
Реактивы. Раствор № 1 для полимеризации геля с рН 8,9 (1,0 М соляная кислота – 48 мл, трис-основание – 36,6 г, N,N,N,N-тетраметилэтилендиамин, или ТЕМЕД – 0,23 мл и дистиллированная вода до 100 мл); раствор № 2 (акриламид – 30,0 г, N,N-метиленбисакриламид – 0,8 г и дистиллированная вода до 100 мл); персульфат аммония, 0,14%-ный свежеприготовленный раствор; сахароза, 40%-ный раствор; электродный буфер с рН 8,9 (трис-основание – 6,0 г, глицин – 28,8 г, дистиллированная вода до 1 л; перед употреблением разводят в 10 раз); уксусная кислота, 7%-ный раствор; фосфатный буфер, 0,5 М с рН 7,4; лактат натрия, 1 М раствор; НАД, 10 г/л раствор; нитротетразолиевый синий (НС), 1 г/л раствор; феназинметасульфат (ФМС), 1 г/л раствор; хлорид магния, 0,005 М раствор; хлорид натрия, 0,1 М раствор. Оборудование. Колба коническая вместимостью 25 мл; пипетки с оттянутым тонким концом; фильтровальная бумага; стеклянные палочки; штатив с пробирками; пипетки вместимостью 0,1; 1,5 и 10 мл; резиновые колпачки; аппарат для электрофореза со стеклянными трубочками; источник постоянного напряжения; микроденситометр; спектрофотометр или ФЭК. Материал. Сыворотка крови.
Метод основан на разной электрофоретической подвижности изоферментов ЛДГ, положение которых на столбиках полиакриламидного геля выявляется с помощью веществ, переносящих водород от лактата через феназинметасульфат на нитротетразолиевый синий. В результате в месте нахождения фракции ЛДГ выпадает фиолетово-синий осадок диформазана. Ход определения. Для полимеризации геля берут сухие чистые стеклянные трубочки, закрывают их с одного конца резиновыми колпачками, устанавливают в штативе строго перпендикулярно и вносят в них каплю раствора сахарозы. Затем готовят полимеризующую смесь, состоящую из растворов № 1, № 2, персульфата аммония и дистиллированной воды в соотношении 1:2:4:1. Смеси готовят из расчета 2 мл на одну трубочку.
Приготовленную полимеризующую смесь разливают в стеклянные трубочки, используя по 2 мл на каждую. Затем на поверхность этого раствора осторожно наслаивают 0,2-0,3 мл дистиллированной воды пипеткой с тонким оттянутым концом (это улучшает полимеризацию геля в трубочках, которая протекает без доступа кислорода воздуха, и формирует гладкую поверхность геля). Через 30 мин обычно полимеризация завершается, о чем свидетельствует ясно различимая граница между полиакриламидным гелем и водой. После этого переворачивают трубочки и осторожно стряхивают с геля наслоенную воду, а остатки воды удаляют из трубочки с помощью фильтровальной бумаги. Стеклянные трубочки с заполимеризованным гелем закрепляют в гнездах верхней камеры для электрофореза. На поверхность геля в трубочке наносят сначала 0.1 мл сыворотки крови, затем такой же объем раствора сахарозы и перемешивают нанесенные жидкости стеклянной палочкой. Осторожно наслаивают на эту жидкость разведенный в 10 раз электродный буфер, заполняя им пространство до верхнего края трубочки. Нижнюю камеру аппарата заливают тем же электродным буфером, устанавливают верхнюю камеру над нижней так, чтобы нижние концы трубочек были погружены в электродный буфер. Затем верхнюю камеру тоже заполняют электродным буфером. Аппарат для электрофореза ставят в холодильник. Электроды подключают к источнику постоянного напряжения: нижний электрод к аноду, верхний к катоду (см. рис. 3). В течение первых 10 мин электрофорез проводят при силе тока 2 мА на каждую трубочку. Затем силу тока увеличивают до 4 мА. Длительность электрофореза около 90 мин. Пока идет электрофорез, для выявления изоферментов ЛДГ готовят в колбе инкубационную смесь следующего состава: растворы лактата натрия, хлорида магния, НАД – по 1 мл, фосфатного буфера и НС – по 2,5 мл и ФМС– 0,25 мл. Перемешивают содержимое колбочки. По окончании электрофореза гели извлекают из трубочек. Для этого используют шприц на 10-20 мл с тонкой длинной иглой. Вводят иглу между стенкой трубочки и гелем. Круговыми движениями отслаивают гель, постоянно выдавливая воду из шприца и продвигая иглу к противоположному концу трубки. При этом столбик геля легко выскакивает из трубки. Столбик геля помещают в пробирки диаметром 7-8 мм и наливают в них инкубационную смесь так, чтобы весь столбик геля был погружен в проявляющую жидкость. Пробирки ставят в термостат при 37˚С на 40-60 мин. Изоферменты ЛДГ выявляются в виде сине-фиолетовых колец на столбике геля. По истечении инкубации столбики геля промывают водой, переносят в пробирки, содержащие раствор уксусной кислоты, и хранят в темноте. Количественную обработку гелевых изоэнзимограмм проводят спектрофотометрическим методом или посредством денситометрии. В первом случае лезвием вырезают окрашенные участки геля, помещают их в пробирки и заливают 1 мл подогретого до +80-85˚С раствора диметилформамида. Затем окрашенную жидкость сливают в микрокюветы и измеряют экстинкцию на спектрофотометре или ФЭКе при 540 нм против раствора диметилформамида. Второй способ обработки заключается в сканировании гелей на микроденситометре. Денситограммы подвергаются количественной обработке. Расчет. Относительную активность каждого изофермента х (%) выражают в процентах от суммы экстинкций всех изоферментов ЛДГ:
ЕА100% Е100 х = ——————, или, упрощенно, х = ———, ∑Е ∑Е
где Е – экстинкция элюата изофермента из зоны геля, относящаяся к данному изоферменту; ∑Е – сумма экстинкций всех изоферментов; А – активность ЛДГ сыворотки крови, ммоль/(ч·л). Оформление работы. Зарисовать полученную изоэнзимограмму и рассчитать относительную активность изоферментов ЛДГ (в %). Сделать вывод о сдвигах спектра изоферментов ЛДГ в исследуемой сыворотке и указать на вероятные причины этого явления. Практическое значение работы. Состав изоферментов ЛДГ имеет внутриклеточную, тканевую и видовую специфичность. Тканевые различия изоферментного спектра ЛДГ явились предпосылкой для использования его в диагностике и прогнозе ряда заболеваний, сопровождающихся некрозом органов и тканей. Известно, что в сердечной мышце, нервной ткани, почках высокая активность ЛДГ1 и ЛДГ2 (изоферменты Н-типа), в поджелудочной железе и легочной ткани преобладает ЛДГ3, а в скелетной мышце и печени – ЛДГ4 и ЛДГ5 (изоферменты М-типа). При некрозе этих тканей находящиеся в них изоферменты поступают в кровь и изменяют ее нормальный спектр. В норме сыворотка крови имеет примерно следующие соотношения изоферментов (в % от общей активности): ЛДГ1 – 32, ЛДГ2 – 47, ЛДГ3 – 12, ЛДГ4 – 5, ЛДГ5 – 4. При инфаркте миокарда в сыворотке крови увеличивается доля ЛДГ1 и ЛДГ2 (спектр смещается в сторону изоферментов Н-типа), причем этот сдвиг определяется размерами очага некроза в сердце. Заживление сопровождается нормализацией состава изоферментов в сыворотке крови. При инфекционном гепатите повышена относительная активность ЛДГ4 и ЛДГ5. Если она сохраняется при клиническом выздоровлении, то это свидетельствует о незавершенности восстановительных процессов в печени. При поражении поджелудочной железы (панкреатит), легочной ткани увеличивается относительная активность ЛДГ3 в сыворотке крови.
Работа 34. Определение активности γ-глутамилтрансферазы В сыворотке крови
Реактивы. L-γ-глутамил-п-нитроанилид; натрия хлорид; глицил-глицин*; субстратно-буферный раствор*; уксусная кислота ледяная, раствор 100 г/л; основной калибровочный раствор п-нитроанилида*. Оборудование. Пипетки на 0,1; 1,0 и 5,0 мл; термостатирующая водяная баня; спектрофотометр или фотоэлектроколориметр. Материал. Сыворотка крови.
Метод основан на определении п-нитроанилида, образующегося из L-γ-глутамил-п-нитроанилида при ферментативном переносе L-γ-глутамилового остатка на глицил-глицин. ГТФ
γ-глутамил-глицилглицид + п-нитроанилин
Ход определения. В опытную пробирку вносят 0,5 мл раствора субстрата и помещают в водяную баню при температуре 37°С. Через 5 минут приливают 0,05 мл сыворотки крови, содержимое перемешивают и инкубируют точно 15 минут при температуре 37°С. Затем прибавляют 3 мл раствора уксусной кислоты и перемешивают. Контрольную пробу ставят также как опытную, но сыворотку добавляют после инкубации. Измеряют на спектрофотометре при длине волны 410 нм или на ФЭКе при длине волны 400-500 нм (фиолетовый или синий светофильтр) в кювете с толщиной слоя 10 мм против контрольной пробы. Окраска стабильна в течение нескольких часов. Расчет. Активность фермента рассчитывают по калибровочному графику. Оформление работы. По полученным значениям экстинкции найти активность фермента. На основании этого сделать вывод о возможности изменения активности в исследуемой сыворотке и указать на предполагаемые причины. Практическое значение работы. В клинике используется определение активности γ-глутамилтрансферазы в сыворотке крови в основном при заболеваниях печени и желчных путей. В норме активность составляет для мужчин 250-1767 нмоль/с·л (15-106 МЕ), для женщин – 167-1100 нмоль/с·л или 10-66 МЕ. Повышение активности фермента наблюдается при заболеваниях желчных путей с явлениями обтурации, при гепатитах, опухолях и метастазах в печень. Следует отметить, что увеличение γ-глутамилтрансферазы, как правило, увеличивается параллельно активности щелочной фосфатазы, но активность γ-глутамилтрансферазы возрастает раньше, остается повышенной более длительное время и относительное увеличение активности фермента в несколько раз выше, чем щелочной фосфатазы. Следует отметить, что наркотики, седативные средства, этанол, стимулируют активность фермента, что используется для диагностики алкогольно-токсических заболеваний печени. БИОХИМИЯ ПИЩЕВАРЕНИЯ
Пищеварение – это ферментативный гидролиз компонентов пищи. Для оценки его используются методы исследования активности ферментов и других компонентов пищеварительных соков, играющих вспомогательную роль в переваривании питательных веществ, например, соляная кислота, желчные кислоты, ионы кальция и т.д. Отклонения в составе пищеварительных соков или появление в них компонентов, не содержащихся в физиологических условиях, дают важную информацию о патологии пищеварения.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 193; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.224.149.242 (0.085 с.) |
 СН3―С―СООН + НАД·Н2 НАД+ + СН3―С―СООН
СН3―С―СООН + НАД·Н2 НАД+ + СН3―С―СООН СН3―СН―СООН + НАД+ СН3―С―СООН + НАД·Н2
СН3―СН―СООН + НАД+ СН3―С―СООН + НАД·Н2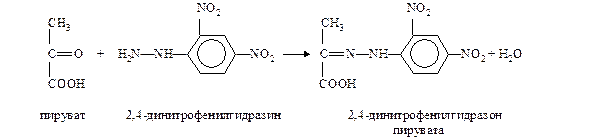
 НС―О―РО3Н2 + Н2О НС―ОН + Н3РО4
НС―О―РО3Н2 + Н2О НС―ОН + Н3РО4 γ-глутамил-п-нитроанилид + глицил-глицин
γ-глутамил-п-нитроанилид + глицил-глицин


