Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Структура и функция G-белка при передаче сигналаСодержание книги
Поиск на нашем сайте
G-белки (англ. G proteins) — это семейство белков, относящихся к ГТФазам и функционирующих в качестве вторичных посредников во внутриклеточных сигнальных каскадах. G-белки названы так, поскольку в своём сигнальном механизме они используют замену ГДФ на ГТФ как молекулярный функциональный «выключатель» для регулировки клеточных процессов. G-белки принадлежат к большой группе ферментов ГТФаз.
G-белки были обнаружены и исследованы Альфредом Гилманом (University of Texas Southwestern Medical Center at Dallas
ГТФ-азный цикла G‑ белков
В покое на постсинаптической мембране находится комплекс рецептор‑G-белок c ГДФ (рис. 809251335, 809251304).
Использованные в рис. 809251335 обозначения фаз ГТФ-азного цикла G‑белков не являются обязательными. В литературе выделяют 5, 6 и более фаз. На рис. 809251304 использовано иное обозначения. Однако принципиальной разницы в представленных схемах нет. Рисунок 809251304 Вам при желании легче будет воспроизвести.
Рис. 809251304. ГТФ-азный цикла G‑белков. 1- фаза покоя; 2 - оединяется медиатора (лиганда) к рецептору; 3 - диссоциация G‑белка; 4 - активация эффектора; 5 - дефосфорилирование ГТФ. Красное окрашивание рецептора на рисунке символизирует активацию; R – рецептор; Е - эффектор; L – медиатор (лиганд, агонист).
Связывание медиатора (агониста) с рецептором приводит к белок-белковому взаимодействию между рецептором и G-белком и ускоряет диссоциацию ГДФ. В результате образуется короткоживущий комплекс агонист - рецептор - G-белок, не связанный ни с каким нуклеотидом. Связывание с этим комплексом молекулы ГТФ снижает сродство рецептора к G‑белку, что приводит к диссоциации комплекса и высвобождению рецептора. Потенциально рецептор может активировать большое количество молекул G-белка, обеспечивая, таким образом, высокий коэффициент усиления внеклеточного сигнала на данном этапе. Активированная альфа-субъединица G‑белка[A42] диссоциирует от бета-гамма-субъединиц и вступает во взаимодействие с соответствующим эффектором, оказывая на него активирующее или ингибирующее воздействие. Альфа-субъдиница с присоединенным с ней ГТФ способна взаимодействовать с эффектором в мембране - ферментами, такими, как аденилатциклаза, или, возможно, ионными каналами. Фермент может активироваться или ингибироваться, а ионный канал - открываться или закрываться. Конкретные примеры будут рассмотрены ниже и в последующих лекциях. Взаимодействие с эффектором, однако, длится до тех пор, пока альфа-субъединица, являющаяся ГТФ-азой, удерживает ГТФ. Вскоре присоединенный ГТФ гидролизуется до ГДФ. Когда это происходит, альфа‑субъединица снова меняет свою конформацию и теряет способность активировать эффектор. После этого альфа-ГДФ взаимодействует с бета-гамма-комплексом и снова образует тримерный комплекс, завершая, таким образом, цикл.
Предполагают, что комплекс из бета-гамма-субъединиц тоже может (прямо или опосредованно) влиять на эффекторные ферменты и ионные каналы (рис. 809251405).
Пример прямой активация калиевого канала субъединицами G-белка показан на рис. 809251442.
Пример прямого ингибирования Са2+-канала субъединицами G-белка показан на рис. 809251458.
Активация пресинаптических адренорецепторов (ауторецепторов) приводит к диссоциации G-белка и последующему ингибированию (закрытию) кальциевых каналов, т.е. снижению уровня освобождение медиатора (норадреналина)
Пример метаботропной модуляции ионных каналов показан на рис. 709200023.
Рис. 709200023. Модуляция потенциал-зависимых кальциевых каналов норадреналином.
|
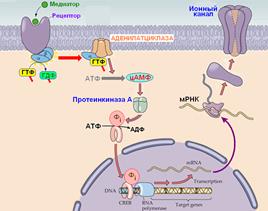
[Мф45] Пример регуляции экспрессии белков путем активации метаботропных рецепторов показан на рис. 809251517.
Рис. 809251517. Регуляция экспрессии белков путем активации метаботропных рецепторов.
|
|
| Поделиться: |





 Рис. 809251152[A41]. Структура G-белка. Альфа-субъединица изображена с полостью, символизирующей сайт связывания ГДФ или ГТФ
Рис. 809251152[A41]. Структура G-белка. Альфа-субъединица изображена с полостью, символизирующей сайт связывания ГДФ или ГТФ
 Рис. 809251335. Цикл активации G-белка под действием G-белок-связанного рецептора. 1 - фаза покоя; 2 - лиганд присоединяется и активирует рецептор; G-белок сталкивается с активированным рецептором, диссоциирует, альфа-субъединица теряет ГДФ; 3 - альфа-субъединица активируется, присоединяя ГТФ; альфа-субъедница присоединяется к эффектору и активирует его. Эффектор, в свою очередь, катализирует синтез вторичного мессенджера; 4 - дефосфорилирование ГТФ деактивирует альфа‑субъединицу, которая отсоединяется от эффектора, готовая начать весь цикл сначала. L – медиатор (лиганд, агонист).
Рис. 809251335. Цикл активации G-белка под действием G-белок-связанного рецептора. 1 - фаза покоя; 2 - лиганд присоединяется и активирует рецептор; G-белок сталкивается с активированным рецептором, диссоциирует, альфа-субъединица теряет ГДФ; 3 - альфа-субъединица активируется, присоединяя ГТФ; альфа-субъедница присоединяется к эффектору и активирует его. Эффектор, в свою очередь, катализирует синтез вторичного мессенджера; 4 - дефосфорилирование ГТФ деактивирует альфа‑субъединицу, которая отсоединяется от эффектора, готовая начать весь цикл сначала. L – медиатор (лиганд, агонист).

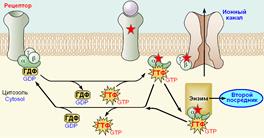 Рис. 809251405. Влияние бета-гамма-субъединиц G‑белка[A43] на ионные каналы.
Рис. 809251405. Влияние бета-гамма-субъединиц G‑белка[A43] на ионные каналы.
 Рис. 809251405. Влияние бета-гамма-субъединиц G‑белка[A44] на ионные каналы (вариант для воспроизведения).
Рис. 809251405. Влияние бета-гамма-субъединиц G‑белка[A44] на ионные каналы (вариант для воспроизведения).

 Рис. 809251442. Прямая активация калиевого канала субъединицами G-белка.
Рис. 809251442. Прямая активация калиевого канала субъединицами G-белка.
 Рис. 809251442. Прямая активация калиевого канала субъединицами G-белка (вариант для воспроизведения).
Рис. 809251442. Прямая активация калиевого канала субъединицами G-белка (вариант для воспроизведения).
 Рис. 809251458. Прямое ингибирование Са2+‑канала субъединицами G-белка.
Рис. 809251458. Прямое ингибирование Са2+‑канала субъединицами G-белка.
 Рис. 809251512. Прямое ингибирование Са2+‑канала субъединицами G-белка (вариант для воспроизведения).
Рис. 809251512. Прямое ингибирование Са2+‑канала субъединицами G-белка (вариант для воспроизведения).