
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Теория гетерогенного горения углеродаСодержание книги Поиск на нашем сайте
В чистом виде гетерогенные реакции проявляются в крайне ограниченных областях температур, когда скорости этих реакций малы. Искажение закона реагирования вызывается появлением диффузионного торможения: диффузией кислорода и продуктов горения в объеме, окружающем горящую частицу и диффузией внутри массы кокса. Физическая картина заключается в следующем: кислород подводится к внешней поверхности куска, на участках этой поверхности, где нет трещин, часть кислорода вступает в соединение с углеродом и выделяется определенное количество оксида и диоксида углерода. При горении углеродной частицы можно выделить два основных процесса, определяющих скорость выгорания: диффузию кислорода к поверхности углеродной частицы и собственно скорость химического реагирования кислорода с углеродом [18]. Рассмотрим общую теорию гетерогенного горения на примере горения одиночной углеродной сферической частицы, принимая следующие условия (рис. 4.1): 1. Концентрация кислорода по всей поверхности одинакова. 2. Реакция протекает на поверхности с образованием конечных продуктов, вторичное реагирование на поверхности и в газовом объеме отсутствует, т. е. идет только реакция (р1). 3. Имеет место реакция первого порядка по кислороду.
Поток кислорода, поглощаемый за счет химического реагирования, может быть рассчитан по формуле, кг/(м2×с),
где k – константа скорости химического реагирования, м/с; с п – концентрация кислорода на поверхности частицы кокса, кг/м3. С другой стороны, поток кислорода, доставляемый за счет диффузии к реагирующей поверхности, кг/(м2·с),
где aD – коэффициент диффузионного массообмена, м/с; с 0 – концентрация кислорода в объеме газа, кг/м3. Приравнивая потоки и исключая неизвестное значение концентрации углерода на поверхности с п, получим выражение для константы обобщающей скорости взаимодействия кислорода с горящей углеродной частицей, включающей как диффузионное сопротивление, так и сопротивление химической реакции, кг/(м2·с),
где αэф – коэффициент реакционного газообмена, м/с. В области низких температур скорость химических реакций мала (рис. 4.2) и во много раз меньше k << aD (
При высоких температурах скорость реакции, определяемая законом Аррениуса k = k 0·exp[- E / (RT)], настолько возрастает, что процесс горения начинает лимитироваться скоростью доставки кислорода к частице k >> aD (1/k << 1/άD). Скорость реакции настолько велика, что доставляемый диффузией кислород мгновенно вступает в химическую реакцию с п→0. Скорость горения в этом случае определяется скоростью диффузии кислорода к поверхности частицы (j = άDc0), режим горения называется диффузионным. При сжигании твердого топлива в плотном либо псевдоожиженном слое, горение крупных частиц идет обычно в диффузионной области. При пылевидном сжигании относительная скорость между газом и топливной частицей невелика, при этом число Шервуда стремится к двум:
В данной области поток почти пропорционален температуре
|
||||||
|
Последнее изменение этой страницы: 2016-12-30; просмотров: 345; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.009 с.) |


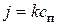 , (4.7)
, (4.7) , (4.8)
, (4.8) , (4.9)
, (4.9)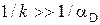 ) скорости, с которой кислород может быть доставлен диффузией к поверхности. Процесс ограничивается скоростью самого химического реагирования (j = kc 0). Поэтому эта область протекания реакции получила название кинетической. Концентрация кислорода на поверхности частицы равна концентрации кислорода в объеме газа с п = с 0. При высоких температурах горение в кинетической области может наступить при больших скоростях потока и малых размерах частиц топлива.
) скорости, с которой кислород может быть доставлен диффузией к поверхности. Процесс ограничивается скоростью самого химического реагирования (j = kc 0). Поэтому эта область протекания реакции получила название кинетической. Концентрация кислорода на поверхности частицы равна концентрации кислорода в объеме газа с п = с 0. При высоких температурах горение в кинетической области может наступить при больших скоростях потока и малых размерах частиц топлива.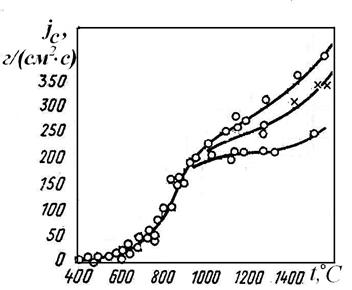
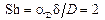 . В данном выражении коэффициент молекулярной диффузии рассчитываю как коэффициент взаимодиффузии кислорода в азоте
. В данном выражении коэффициент молекулярной диффузии рассчитываю как коэффициент взаимодиффузии кислорода в азоте . (4.10)
. (4.10)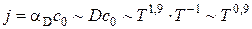 . С уменьшением диаметра частицы, падает диффузионное сопротивление
. С уменьшением диаметра частицы, падает диффузионное сопротивление 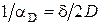 , т. е. уменьшение диаметра пылевых частиц, позволяет повысить скорость их горения.
, т. е. уменьшение диаметра пылевых частиц, позволяет повысить скорость их горения.


