
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Химическая кинетика. Химическое равновесие.Содержание книги
Поиск на нашем сайте
Правило Ле Шателье-Брауна
Характер смещения под влиянием внешних воздействий можно прогнозировать, применяя принцип Ле Шателье: если на систему, находящуюся в равновесии оказывается воздействие извне, то равновесие в системе смещается так, чтобы ослабить внешнее воздействие.
1. Влияние концентраций. Повышение концентрации одного из реагирующих веществ смещает равновесие в сторону расходования вещества. Понижение концентрации – в сторону образования вещества. 2. Влияние температуры. Повышение температуры смещает равновесие в сторону реакции, идущей с поглощением теплоты (эндотермической), а понижение температуры смещает равновесие в сторону реакции, идущей с выделением теплоты (экзотермической). 3. Влияние давления. Повышение давления смещает равновесие в сторону реакции, идущей с уменьшением объема и, наоборот, понижение давления – в сторону реакции, идущей с увеличением объема. Пример 1. Как сместится химическое равновесие при синтезе аммиака в экзотермической реакции?
Решение. При повышении температуры в экзотермической реакции 3H2(г) + N2(г) = 2NH3(г); ΔH0 = -92,4 кДж реакция протекает с выделением теплоты, равновесие должно сдвигаться влево (в сторону исходных веществ).
Скорость реакции:
При увеличении давления в три раза концентрация веществ увеличивается также в три раза:
Такое изменение концентрации увеличивает скорость прямой реакции в 81 раз, а обратное в 9 раз, т.е. при увеличении давления в три раза состояние равновесия достигается быстрее в 81: 9 = 9 раз. В левой части уравнения участвуют в реакции 3 + 1 = 4 моль веществ, а в правой части уравнения получается 2 моль, поэтому увеличение давления приводит к повышению выхода целевого продукта, что подтверждает принцип Ле Шателье. Пример 2. При синтезе аммиака N2(г) + 3H2(г)
Решение. Константа равновесия реакции
Начальная концентрация вещества складывается из равновесной концентрации этого вещества и количества вещества, израсходованного на образование равновесной концентрации продукта реакции. На основе уравнения реакции определяем количество израсходованного N2:
на образование 2 моль NH3 расходуется 1 моль N2; на образование 6 моль NH3 расходуется x моль N2. Отсюда
Начальная концентрация азота
Аналогично составим пропорцию:
на образование 2 моль NH3 расходуется 3 моль H2; на образование 6 моль NH3 расходуется y моль H2. Отсюда
Начальная концентрация водорода
Ответ: начальные концентрации Задания
81-84. В гомогенной газовой системе установилось равновесие. Напишите выражение для константы равновесия. Дайте обоснованные ответы на вопросы: а) как и во сколько раз изменится скорость прямой реакции при увеличении давления в системе в два раза; б) как увеличение давления отразится на состоянии равновесия; в) в каком направлении сместится равновесие при увеличении температуры?
85-88. В гетерогенной системе установилось равновесие. Напишите выражение для константы равновесия. Дайте обоснованные ответы на вопросы: а) как уменьшение давления отразится на состоянии равновесия; б) в каком направлении сместится равновесие при уменьшении температуры; в) как и во сколько раз изменится скорость прямой реакции при уменьшении давления в системе в два раза?
89. Напишите выражения для скоростей прямой и обратной реакций и для константы равновесия:
2CO(г) + O2(г)
Как следует изменить в реакционном сосуде: а) температуру; б) давление, чтобы сместить равновесие в прямом направлении?
90. Напишите выражения для скоростей прямой и обратной реакций и константы равновесия:
MgCO3(к)
В каком направлении сместится равновесие: а) по мере накопления в реакторе MgO; б) при увеличении в реакторе давления; в) при увеличении температуры?
91. Напишите выражения для скоростей прямой и обратной реакций:
2NO2(г)
Как изменятся эти скорости: а) при увеличении концентрации NO в три раза; б) при увеличении давления в реакционном сосуде в два раза? Как эти воздействия повлияют на состояние равновесия и величину константы равновесия? Напишите выражение для константы равновесия.
92. Константа равновесия гомогенной системы
N2 + 3H2 = 2NH3
при температуре 400°С равна 0,1. Равновесные концентрации водорода и аммиака соответственно равны 0,2
93. При некоторой температуре равновесие гомогенной системы
2NO + O2 = 2NO2
установилось при следующих концентрациях реагирующих веществ: [NO] = 0,2
|
||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-15; просмотров: 426; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.166.34 (0.006 с.) |

 ;
; .
.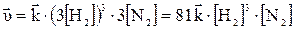 ;
; .
. 2NH3(г) равновесие установилось при следующих концентрациях реагирующих веществ,
2NH3(г) равновесие установилось при следующих концентрациях реагирующих веществ,  : [N2] = 4; [H2] = 2; [NH3] = 6. Рассчитайте константу равновесия этой реакции и исходные концентрации азота и водорода.
: [N2] = 4; [H2] = 2; [NH3] = 6. Рассчитайте константу равновесия этой реакции и исходные концентрации азота и водорода.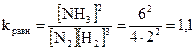 .
. .
. = [N2] + x = 4 + 3 = 7
= [N2] + x = 4 + 3 = 7 
 = [H2] + y = 2 + 9 = 11
= [H2] + y = 2 + 9 = 11  ;
; 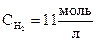
 2HI
2HI
 и 0,08
и 0,08 


