
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Общая характеристика классов веществСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
В соответствии со сводной таблицей классов веществ (табл.) ниже приводятся определения классов неорганических веществ, их важнейшие химические свойства и способы получения. Неорганические вещества – соединения, образуемые всеми химическими элементами (кроме большинства органических соединений углерода). Делятся по химическому составу:
Простые вещества Сложные вещества
1.1. Простые вещества образованы атомами одного элемента. Делятся по химическим свойствам:
Металлы Амфигены Аэрогены Неметаллы Металлы – простые вещества элементов с металлическими свойствами (низкая электроотрицательность). Типичные металлы: IA-группа Li, Na, K, Rb, Cs IIA-группа Mg, Ca, Sr, Ba Металлы обладают высокой восстановительной способностью по сравнению с типичными неметаллами. В электрохимическом ряду напряжений они стоят значительно левее водорода, вытесняют водород из воды (магний – при кипячении): 2М + 2Н2О = 2МОН + Н2↑ (M= Li, Na, K, Rb, Cs) М + 2Н2О = М(ОН)2 + Н2↑ (M= Mg, Ca, Sr, Ba) Простые вещества элементов Cu, Ag и Ni также относят к металлам, так как у их оксидов CuO, Ag2O, NiO и гидроксидов Cu(OH)2, Ni(OH)2 преобладают основные свойства.
Неметаллы – простые вещества элементов с неметаллическими свойствами (высокая электроотрицательность). Типичные неметаллы:
VIA-группа O2, S, Se VA-группа N2, P, As IVA-группа C, Si Неметаллы обладают высокой окислительной способностью по сравнению с типичными металлами.
Амфигены – амфотерные простые вещества, образованные элементами с амфотерными (двойственными) свойствами (электроотрицательность промежуточная между металлами и неметаллами). Типичные амфигены:
VIБ-группа Cr IIБ-группа Zn IIIA-группа Al, Ga IVA-группа Ge, Sn, Pb Амфигены обладают более низкой восстановительной способностью по сравнению с типичными металлами. В электрохимическом ряду напряжений они примыкают слева к водороду или стоят за ним справа. Аэрогены – благородные газы, одноатомные простые вещества элементов VIIIA-группы: He, Ne, Ar, Kr, Xe, Rn. Из них He, Ne и Ar химически пассивны (соединения с другими элементами не получены), а Kr, Xe и Rn проявляют некоторые свойства неметаллов с высокой электроотрицательностью.
1.2. Сложные вещества образованы атомами разных элементов. Делятся по составу и химическим свойствам:
Оксиды Гидроксиды Соли Бинарные соединения
1.2.1. Оксиды – соединения элементов с кислородом, степень окисления кислорода в оксидах всегда равна (–II). Делятся по составу и химическим свойствам:
Основные Кислотные Амфотерные Двойные Несолеобразующие
Элементы He, Ne и Ar соединений с кислородом не образуют. Соединения элементов с кислородом в других степенях окисления – это не оксиды, а бинарные соединения, например O+IIF2–I и H2+IO2–I. Не относятся к оксидам и смешанные бинарные соединения S+IVCl2–IO–II. Причины разделения оксидов на основные, кислотные и амфотерные легче вскрываются в результате рассмотрения характера диссоциации их гидратов. Электролитическая диссоциация гидратов (гидроокисей), имеющих общую формулу ЭОН, может происходить по основному (I) и кислотному (II) направлениям:
 
I II Преобладание того или иного направления зависит от относительной полярности связей Э−О и О−Н (а она зависит от разности электроотрицательностей (Δχ) компонентов, а также от размеров и эффективного заряда атомов). Так, для NaOH разность электроотрицательностей элементов в связи Na−O (3,5-0,9) больше, чем в связи O−H (3,0-2,1). Связь Na−O, следовательно, более полярна, чем связь O−H, и диссоциация происходит при разрыве связи Na−O, т.е. по основному типу (I). В случае H−O−Cl, степень полярности связи H−O > O−Cl, т.к. Δχ H−O (3,5-2,1) > Δχ O−Cl (3,5-3,0); следовательно, диссоциация будет происходить по месту связи H−O, т.е. диссоциация в этом случае будет происходить по кислотному типу (II). В случае, если полярности обеих связей будут близки друг к другу, приходится считаться с возможностью диссоциации по обоим направлениям. Подобные соединения, способные при одних и тех же условиях отщеплять и ионы водорода и ионы гидроксильной группы, называются амфотерными. Характер диссоциации (кислотный или основной) можно объяснить также, исходя из понятия плотности заряда иона. Плотность заряда иона – отношение заряда иона к его радиусу r. Связь условного иона O2– с H+ значительна, потому что плотность заряда иона водорода большая. При небольшой плотности заряда у ионов металлов, т.к. радиусы их велики, связь их с О2– ионами менее прочна, чем связь О−Н, поэтому происходит диссоциация по основному типу – на ионы металлов и ОН- - ионы. Но чем большую плотность заряда имеет положительно заряженный ион элемента, тем в большей степени он будет притягивать О2– – ионы и отталкивать Н+ - ионы, что приведет к диссоциации кислотного характера – на Н+-ионы и анионы.
Это объяснение находит полное подтверждение, если рассмотреть его в связи с положением элементов в периодической системе. Так, у элементов начала каждого периода, т.е. у металлов I и II групп, диссоциация гидроксидов протекает по основному типу потому, что плотность заряда ионов этих металлов незначительна. При переходе в периоде слева направо заряд ионов элементов растет, а радиус уменьшается, потому что при этом же числе квантовых слоев атомы сжимаются вследствие увеличения заряда ядра. Плотность заряда возрастает и гидроксиды типичных металлов, расположенных в начале периода, обладают резко выраженными основными свойствами, а гидроксиды неметаллов – элементов, расположенных в конце каждого периода, диссоциируют по кислотному типу. Ниже приведено изменение ионных радиусов элементов III периода в высшей степени окисления:
У гидроксидов элементов, находящихся в периодах между типичными металлами и активными неметаллами, постепенно уменьшается основной характер и возрастает кислотный характер диссоциации. Гидроксиды, образованные этими элементами, проявляют амфотерный характер, т.е. могут диссоциировать и как основания, и как кислоты. Например, Al(OH)3 является амфолитом с преобладанием основного свойства, гидроксид Si(OH)4 - амфолит с резко преобладающими кислотными свойствами, он образует в растворе кислородосодержащие анионы. Также закономерно изменяется характер диссоциации гидроокисей в зависимости от положения элементов в каждой главной подгруппе периодической системы: кислотный характер диссоциации гидроокисей возрастает, если перемещаться по подгруппе снизу вверх, т.к. при одном и том же заряде ионов элементов одной группы радиус их снизу вверх убывает (потому что уменьшается число квантовых слоев), а плотность заряда элемента возрастает.
Оснóвные оксиды – продукты полной дегидратации (реальной или условной) оснóвных гидроксидов, сохраняют химические свойства последних. Из типичных металлов только Li, Mg, Ca и Sr образуют оксиды Li2O, MgO, CaO и SrO при сжигании на воздухе; оксиды Na2O, K2O, Rb2O, Cs2O и BaO получают другими способами. Оксиды CuO, Ag2O и NiO также относят к оснóвным.
Химические свойства оснóвных оксидов Оснóвные оксиды: а) взаимодействуют с водой с образованием оснований K2O+H2O=2KOH б) взаимодействуют с кислотными оксидами и кислотами с образованием солей BaO+N2O5=Ba(NO3)2 Fe2O3+3H2SO4=Fe2(SO4)3+3H2O. в) взаимодействуют с амфотерными оксидами и гидроксидами, образуя соли сплавление BeO+ZnO=BeZnO2+H2O BeO+Zn(OH)2=H2O+BeZnO2
Кислотные оксиды – продукты полной дегидратации (реальной или условной) кислотных гидроксидов, сохраняют химические свойства последних. Из типичных неметаллов только S, Se, P, As, C и Si образуют оксиды SO2, SeO2, P2O5, As2O3, CO2 и SiO при сжигании на воздухе; оксиды Cl2O, Cl2O7, I2O5, SO3, SeO3, N2O3, N2O5 и As2O5 получают другими способами.
И с к л ю ч е н и е: у оксидов NO2 и ClO2 нет соответствующих кислотных гидроксидов, но их считают кислотными, так как NO2 и ClO2 реагируют со щелочами, образуя соли двух кислот, а ClO2 с водой, образуя две кислоты: а) 2NO2+2NaOH=NaNO2+NaNO3+H2O б) 2ClO2+H2O(хол.)=HClO2+HClO3 2СlO2+2NaOH(хол.)=NaClO2+NaClO3+H2O Оксиды CrO3 и Mn2O7 (Хром и марганец в высшей степени окисления) также являются кислотными.
|
|||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-26; просмотров: 592; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.19.77.231 (0.015 с.) |




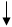
 VIIA-группа F2, Cl2, Br2, I2
VIIA-группа F2, Cl2, Br2, I2 IIA-группа Be
IIA-группа Be



 Оксиды
Оксиды


