
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Признаки протекании реакции ионного обменаСодержание книги
Поиск на нашем сайте
Билет Чистые вещества и смеси. Способы разделения смесей. В природе вещества встречаются преимущественно в виде смесей. Однородным называют такие смеси, в которых даже с помощью микроскопа нельзя обнаружить частицы веществ, входящих в смесь. Например, растворы сахара или поваренной соли в воде. Неоднородным называют такие смеси, в которых невооруженным глазом или при помощи микроскопа можно заметить частицы веществ, составляющих смесь. Для химических лабораторий и промышленности часто требуются чистые вещества. Чистыми называют вещества, которые обладают постоянными физическими свойствами, например, дистиллированная вода. (Практически абсолютно чистые воды не получены.) Существует различные способы разделения смесей. Отстаивание Выделение веществ из неоднородной смеси, образованной нерастворимым в воде веществами с различной плотностью. Например, железные опилки от древесных можно отделить, взбалтывая эту смесь с водой, а затем отстаивая. Железные опилки опускается на дно сосуда, а древесные всплывают, и их вместе с водой можно слить. Фильтрование Выделение веществ из неоднородной смеси, образованной растворимыми и нерастворимыми в воде веществами. Для выделения поваренной соли смесь ее с песком взбалтывают в воде. Поваренная соль растворяется, а песок оседает.Чтобы ускорить отделение нерастворимых частиц из раствора, смесь фильтруют. Песок остается на фильтровальной бумаге, а прозрачный раствор поваренной соли проходит через фильтр. Выпаривание. Кристаллизация Чтобы растворное вещество, например поваренную соль, выделить из раствора, последний выпаривают. Вода испаряется, а фарфоровой чашке остается поваренная соль. Иногда применяют упаривание, т. е. частичное испарение воды. В результате образуется более концентрированный раствор, при охлаждении которого растворенное вещество выделяется в виде кристаллов. Этот способ очистки веществ называется кристаллизацией. Дис тилляция Этот способ разделения смесей основан на различии в температурах кипения растворимых друг в друге компонентов.Дистилляция (перегонка) прием разделения однородных смесей путем испарения летучих жидкостей с последующей конденсацией их паров. Например, получение дистиллированной воды. Для этого воду с растворенными в ней веществами кипятят в одном сосуде. Образующиеся водяные пары конденсируются в другом сосуде в виде дистиллированной воды. Соли их состав и свойства. Соли – это сложные вещества, образованные атомами металлов и кислотными остатками. С точки зрения теории электролитической диссоциации соли - это электролиты, диссоциирующие в водных растворах на катионы металлов и анионы кислотных остатков. Соли бывают средние (нормальные), кислые и основные. Средние соли – это продукты полного замещения водорода в кислоте на атомы металла или гидроксогруппы ОН- в основании на кислотный остаток. Кислые соли можно рассматривать как продукты неполного замещения атомов водорода кислоты на атомы металлов. Основные соли можно рассматривать как продукты неполного замещения ионов ОН- основания на ионы кислотных остатков. Получение 1. Взаимодействие металла с неметаллом: Fe + S
2. Взаимодействие металлов, расположенных в ряду напряжений левее водорода, с растворами кислот: Zn + H2SO4
3. Взаимодействие металлов с растворами солей:
Fe + CuSO4
4. Взаимодействие кислот с основаниями (реакция нейтрализации): HCI + NaOH
5. Взаимодействие кислот с основными оксидами:
H2SO4 + CaO Билет Молекулы и атомы. Относительная атомная масса Атомы — это маленькие частицы, из которых состоит вещество. Невозможно даже представить себе, насколько они малы. Если сложить в цепочку сто миллионов атомов, у нас получится ниточка длиной всего лишь в 1 см. В тонком листе бумаги, наверное, не меньше миллиона слоев атомов. Науке известно более ста видов атомов; соединяясь друг с другом, они образуют все окружающие нас вещества. Молекула — это мельчайшая частица вещества, которая может существовать самостоятельно. Она состоит из атомов, удерживающихся вместе при помощи связей. Например, у молекулы воды два атома водорода связанны с атомом кислорода. Атомы удерживаются вместе благодаря электрическим зарядам частиц, из которых они состоят. Описывая строение молекул, ученые прибегают к помощи моделей. Как правило, они пользуются структурными и пространственными моделями. Структурные модели представляют связи, удерживающие атомы вместе, в виде палочек. Таким образом, за единицу атомной массы принималась 1/16 часть атома кислорода, получившая название кислородной единицы. В дальнейшем было установлено, что природный кислород представляет собой смесь изотопов, так что кислородная единица массы характеризует среднее значение массы атомов природных изотопов кислорода. Для атомной физики такая единица оказалась неприемлемой, и в этой отрасли науки заединицу атомной массы была принята 1/16 часть массы атома кислорода 16О. В результате оформились две школы атомных масс — химическая и физическая. Наличие двух шкал атомных масс создавало большие неудобства. В 1961 году принята единая шкала относительных атомных масс, в основу которой положена 1/12 часть массы атома изотопа углерода 12С, названная атомной единицей массы (а.е.м.). Оксиды. Способы получения основных оксидов. Оксидами называются сложные вещества, состоящие из двух химических элементов, один из которых кислород. По химическим свойствам оксиды делятся на две группы: 1) безразличные – не образуют солей, например: NO, CO, H2O; 2) солеобразующие, – кислотные – – амфотерные оксиды Основными называются оксиды, которые образуют соли при взаимодействии с кислотами или кислотными оксидами. Основным оксидам соответствуют основания. Например, оксиду кальция CaOотвечает гидроксид кальция Ca(OH)2, оксиду кадмия CdO – гидроксид кадмия Cd(OH)2. Получение 1. Непосредственное взаимодействие металла с кислородом:2Mg + O2 2. Горение сложных веществ:2FeS + 3O2 3. Разложение солей кислородсодержащих кислот:CaCO3 4. Разложение оснований:Ca(OH)2
Билет
|
||||
|
Последнее изменение этой страницы: 2016-08-25; просмотров: 1046; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.72.24 (0.006 с.) |


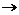 FeS.
FeS.
 2MgO.
2MgO.


