
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Оперативный контроль точностиСодержание книги
Поиск на нашем сайте
В качестве характеристики случайной составляющей погрешност и результата анализа принимают наибольшее возможное значение среднего квадратического отклонения случайной составляющей погрешности (показатель) — σ (∆). В качестве характеристики систематической составляющей принимают границы интервала (∆сн, ∆св, Р), в которых неисключенная систематическая составляющая погрешности находится с принятой вероятностью Р. Контроль сходимости результатов параллельных определений при анализе одной пробы следует проводить по двум параллельным результатам анализа Х1 и Х2, полученным в одинаковых условиях. Считается, что методика находится в контрольном состоянии, если расхождение между параллельными определениями не превышает допускаемого, то есть выполняется условие: │ X1 – X2 │≤ d,
где d — норматив контроля сходимости — значение допускаемого расхождения между параллельными определениями, приведенное в методике КХА. При выполнении данного условия среднее арифметическое значение (Х = (Х1 + Х2)/ 2 ) принимается за результат анализа. В противном случае анализ следует повторить, используя резервную пробу. Контроль сходимости следует проводить при каждом анализе. Контроль воспроизводимости. Образцами для контроля являются реальные пробы анализируемых объектов. Контроль воспроизводимости следует проводить по двум результатам анализа одной и той же пробы, полученным в разных условиях (Х1 и Х2), допускаемых методикой, например, в разные дни, разными руками, на разных приборах данного типа, с использованием разной посуды и реактивов и т.д. Методика находится в контрольном состоянии, если выполняется условие: │ X1 – X2 │≤ D, где D — норматив контроля воспроизводимости допускаемого расхождения в результате анализа пробы в различных условиях, который также должен приводится в методике КХА. В противном случае один результат или оба неверны, анализ необходимо повторить. Контроль воспроизводимости обязательно следует проводить при смене партии реактивов, посуды, после ремонта прибора и т.д. Контроль точности результатов анализа можно проводить по вариантам: 1. В первом варианте образцами для контроля точности являются пробы стандартных образцов (ГСО), по составу адекватные пробам анализируемых объектов. Если предварительно установлено, что в анализируемой пробе отсутствует определяемый компонент, то образцами для контроля точности может служить реальная проба с добавками ГСО определяемого компонента в диапазоне определяемых концентраций. Добавка делается на самой ранней стадии (до пробоподготовки). Тогда контроль точности результатов анализа можно проводить путем сравнения результатов анализа стандартного образца (образца для контроля) и аттестованным значением концентрации элемента в стандартном образце (образце для контроля). В этом случае расхождения результатов анализа (Х) стандартного образца и его аттестованного значения (Сат) не должны превышать значений К, приведенных в прописи методики анализа: │ X – Сат │≤ К где К — норматив оперативного контроля точности — значение допускаемого расхождения между результатом анализа стандартного (контрольного) образца и аттестованного значения содержания компонента в нем.
ГЛАВА 4. ФОТОКОЛОРИМЕТРИЯ
Общие положения
Фотоколориметрический анализ (молекулярная абсорбционная спектроскопия) относится к оптическим методам анализа. Метод основан на способности вещества поглощать электромагнитное излучение оптического диапазона, который включает ультрафиолетовую, видимую и ИК-области. Наибольшее распространение получили фотометрические методы анализа, основанные на поглощении окрашенными соединениями в видимой области спектра, т.е. в интервале длин волн 400 — 780 нм. Фотометрический метод анализа широко применяется в практике аналитического контроля. Метод имеет низкий предел обнаружения (10-5 — 10-6 М), относительная ошибка большинства определений 1 — 2 %. Поглощение квантов hn электромагнитного излучения оптического диапазона молекулой или ионом обусловлено переходом электронов на орбитали с более высокой энергией. Каждая молекула обладает определенным набором возбужденных квантовых состояний, отличающихся значением энергии, поэтому интенсивно поглощаются те кванты света, энергия которых равна энергии возбуждения молекулы. Характер поглощения зависит от природы вещества, на этом основан качественный анализ. За формирование аналитического сигнала ответственными являются в основном d ® d*- и p ® p*- переходы. d ® d*- переходы характерны для аква-ионов и некоторых комплексных соединений d-элементов с неполностью заполненными d-орбиталями. p ® p*- переходы свойственны молекулам органических соединений и обеспечивают их окраску. Для количественного анализа используют зависимость светопоглощения от концентрации определяемого вещества.
Поглощение света подчиняется закону Ламберта – Бугера – Бера А = elc где А — оптическая плотность, I 0 и I — интенсивности падающего и прошедшего через образец света, T — пропускание, e — молярный коэффициент поглощения (экстинкиции), l — длина оптического пути (толщина поглощающего слоя) в см, c — молярная концентрация.
Закон этот строго справедлив только для разбавленных растворо в и в определенных условиях: · постоянство состава и неизменность поглощающих частиц в растворе; · монохроматичность и параллельность проходящего через раствор потока небольшой интенсивности; · постоянство температуры
Молярный коэффициент светопоглощения характеризует чувствительность реакции и является постоянной величиной для данного окрашенного соединения. Для повышения чувствительности определения выбирают реакцию с максимальным значением e (см. справочник по аналитической химии). Молярный коэффициент поглощения раствора можно рассчитать, если приготовить серию растворов с известными концентрациями веществ и измерить оптическую плотность раствора. Коэффициент линейной регрессии зависимости А = f(С) представляет собой молярный коэффициент поглощения. Спектры поглощения одного и того же вещества в координатах А - l имеют одинаковый вид независимо от толщины слоя раствора или концентрации вещества в растворе и характеризуются максимумом при одной и той же длине волны, при которой и проводят все определения. Селективно подбирая длину волны, отвечающую максимуму поглощения вещества, можно исключить влияние матрицы (растворителя). Если исследуется смесь нескольких поглощающих веществ, то концентрацию каждого из них определяют, проводя измерения при длинах волн, отвечающих максимумам поглощения этих веществ Возможности современных измерительных приборов таковы, что позволяют измерять величину А от 0,02 до 3,0. Однако для получения удовлетворительных по точности результатов значения измеряемой оптической плотности должны находиться в пределах 0,2 < А < 0,8. Для проведения фотометрических исследований необходимо соблюдать ряд условий: · цветная реакция должна проходить быстро, избирательно, полностью и воспроизводимо, а окраска образующейся аналитической формы должна быть устойчивой во времени и к действию света; · аналитический реагент вводят в количестве, достаточном для перевода всего определяемого вещества в аналитическую форму; · при проведении реакции выбирают такую область рН, в которой небольшие изменения рН не влияют на светопоглощение, а оно при этом максимально; · фотометрические измерения проводят в определенном интервале длин волн, при этом ориентируются на большее различие в поглощении аналитической формы и исходных реагентов. Чем больше контрастность, тем удобнее реакция для фотометрирования; · поглощение всегда измеряют относительно раствора сравнения, поглощение которого принимается за оптический ноль; Все фотометрические определения проводят по единой схеме: · переведение пробы анализируемого вещества в раствор; · получение окрашенной аналитической формы в результате проведения цветной реакции; · измерение светопоглощения раствора аналитической формы; · обработка полученных данных. Измерение поглощения проводят с помощью фотоэлектроколориметров. Фотоэлектроколориметрия — анализ на основе измерения поглощения нестрого монохроматичного излучения. Цвет раствора всегда является дополнительным к цвету поглощенного излучения (табл. 1). Цвет светофильтра является дополнительным к цвету раствора и соответствует участку спектра, который этим светофильтром пропускается. Таблица 1 Наблюдаемые цвета и соответствующие им поглощенные участки спектра
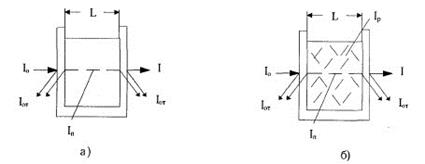
Прохождение потока электромагнитной энергии через какую-либо жидкую среду сопровождается такими явлениями, как поглощение (уменьшение энергии потока), рассеяние и некоторые другие. Поток световой энергии, переносимый через единицу площади, называют интенсивностью потока световой энергии. На рис. показано изменение интенсивности потока световой энергии при прохождении света через раствор (а) и дисперсную среду (б) с толщиной поглощающего слоя L.
10 — интенсивность падающего потока световой энергии; 1от — интенсивность потока световой энергии, отраженной от стенки кюветы; 1п— интенсивность потока световой энергии, поглощенной окрашенным раствором; 1р — интенсивность потока световой энергии, рассеянного дисперсной средой; I — интенсивность потока световой энергии, прошедшего через слой исследуемого вещества. Если не учитывать поглощение потока световой энергии стенками кюветы, то интенсивность падающего светового потока 10 при прохождении кюветы с раствором и дисперсной средой разлагается на составляющие следующим образом: I 0 = Iот + Iп + I — для раствора, I0 = Iот + Iп + Iр + I — для дисперсной среды. В фотометрии 1 от, как правило, компенсируется или учитывается.
|
||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-15; просмотров: 236; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.171.72 (0.011 с.) |

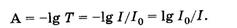
 где:
где:


