
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Смещение химического равновесия. Принцип Ле ШательеСодержание книги
Поиск на нашем сайте
Как уже отмечалось ранее, химическое равновесие всегда отвечает определенным условиям. При изменении внешних параметров (температуры, концентрации, в некоторых случаях – давления) равновесие может нарушиться. Это объясняется тем, что изменение условий неодинаково влияет на скорости прямой и обратной реакций. Через некоторое время эти скорости вновь сравниваются (за счет изменения равновесных концентраций) и наступает состояние равновесия, отвечающее новым условиям. Изменение равновесных концентраций реагирующих веществ, вызванное изменением какого-либо параметра системы, называется смещением, или сдвигом, химического равновесия. В 1884 г. Ле Шателье сформулировал принцип, который помогает качественно предсказать смещение химического равновесия при изменении одного из параметров: Если на систему, находящуюся в состоянии химического равновесия, оказано внешнее воздействие, то равновесие сместится в направлении той реакции, которая ослабляет это воздействие. Влияние изменения концентрации. Введение в равновесную систему дополнительных количеств любого из реагирующих веществ ускоряет ту реакцию, в которой оно расходуется. Например, в реакции: 2NO + O2 ⇄ 2NO2 повышение концентраций NO или O2 смещает равновесие вправо, повышение концентрации NO2 – влево. Равновесие смещается вправо также при уменьшении концентрации NO2, а при уменьшении концентрации NO или O2 – влево. Влияние температуры. Повышение температуры смещает равновесие в сторону эндотермической реакции. Таким образом, для того, чтобы судить о влиянии температуры на химическое равновесие, необходимо знать тепловой эффект (изменение энтальпии) реакции. Например, реакция: CO(газ) + H2O(пар) ⇄ CO2(газ) + H2(газ); характеризуется отрицательным значением стандартной энтальпии, следовательно, прямая реакция является экзотермической, обратная – эндотермической. Таким образом, при увеличении температуры равновесие сместится в сторону эндотермической, т.е., обратной реакции, а уменьшение температуры сместит равновесие в сторону экзотермической (прямой) реакции. Влияние давления. Изменение давления оказывает существенное влияние только на реакции, протекающие в газовой фазе.
При увеличении давления равновесие смещается в сторону образования меньшего числа моль (молекул) газа. Действительно, уменьшение общего числа молекул в газовой смеси влечет за собой уменьшение давления в системе, что в свою очередь, ослабляет внешнее воздействие. Так, уравнение обратимого процесса: N2 + 3H2 ⇄ 2NH3, показывает, что из четырех молекул в левой части (одной молекулы азота и трех молекул водорода) образуются две молекулы аммиака. Таким образом, повышение давления смещает равновесие вправо, а понижение давления – влево. В тех случаях, когда в результате реакции число молекул остается постоянным, равновесие при изменении давления не смещается. К таким реакциям относятся, например: CO + H2O ⇄ CO2 + H2; N2 + O2 ⇄ 2NO.
Эталоны решения задач 1. Рассчитать константу химического равновесия Kc для реакции: NO2(газ) + SO2(газ) ⇄ NO(газ) + SO3(жидк.) по известным данным:
Оценить возможность самопроизвольного протекания реакции в прямом направлении и значение константы равновесия. Решение. Рассчитаем стандартную энергию Гиббса реакции по первому следствию из закона Гесса:
Величину Kc найдем из уравнения изотермы Вант-Гоффа:
Kc >> 1, т. е. при данной температуре равновесие данной реакции сильно смещено в сторону образования продуктов реакции. 2. Для равновесной реакции: N2 + 3H2 ⇄ 2NH3 имеются следующие данные:
1) Рассчитать: а) температуру, при которой система находится в равновесии (Kc = 1); б) значение константы равновесия при 298 К. 2) Указать направление смещения равновесия при повышении (понижении) температуры. Решение. При Кс = 1 стандартная энергия Гиббса равна нулю. Тогда из соотношения:
получим:
Для данной реакции зависимость энергии Гиббса от температуры выглядит следующим образом:
При стандартной температуре (298 К):
Значение Кс при данной температуре найдем из соотношения:
Проведенный расчет показывает, что:
Это означает, что при понижении температуры равновесие смещается в прямом направлении. Аналогичный вывод можно сделать и исходя из принципа Ле Шателье. Действительно реакция образования аммиака – экзотермическая (
3. Для реакции CO2(газ) + H2(газ) ⇄ CO(газ) + H2O(пар) константа равновесия равна 1. Исходные концентрации веществ составили: С0(СO2) = 0,2 моль/л; С0(H2) = 0,8 моль/л. Рассчитать, при каких концентрациях всех четырех веществ установилось равновесие. Решение. Обозначим концентрации С(СО2) и С(Н2), вступивших в реакцию, через «х», т. е. С(СO2)прореаг. = С(H2)прореаг. = х моль/л. Тогда: С(СO2)равн. = С0(CO2) - С(СO2)прореаг. = 0,2 - х; С(H2)равн. = С0(H2) - С(H2)прореаг. = 0,8 - х. Из уравнения реакции видно, что: [СO2] = [H2O] = x. Выражение для константы равновесия имеет вид:
x2 = 0,16 - 0,2x - 0,8x + x2 x = 0,16. Равновесные концентрации всех веществ равны: [СO2] = 0,2 - 0,16 = 0,04 моль/л; [H2] = 0,8 - 0,16 = 0,64 моль/л; [СO] = [H2O] = 0,16 моль/л. 4. Реакция образования йодистого водорода протекает по уравнению: H2(газ) + I2(газ) ⇄ 2HI(газ). Исходные концентрации веществ составили: С0(H2) = 0,02 моль/л; С0(I2) = 0,04 моль/л. Известно, что в реакцию вступило 50% Н2. 1) Вычислить константу химического равновесия. 2) В каком направлении сместится равновесие, если: а) увеличить концентрацию I2? б) уменьшить концентрацию HI? в) увеличить давление?
Решение. Исходя из уравнения реакции, определяем концентрации веществ, прореагировавших между собой: С(H2)прореаг. = 0,5·0,02 = 0,01 моль/л; С(I2)прореаг. = С(H2)прореаг. = 0,01 моль/л. Находим равновесные концентрации: [HI] = 2×c(H2)прореаг. = 0,02 моль/л (по уравнению реакции); [H2] = c0(H2) - с(H2)прореаг. = 0,02 - 0,01 = 0,01 моль/л; [I2] = c0(I2) - с(I2)прореаг. = 0,04 - 0,01 = 0,03 моль/л. Подставляем равновесные концентрации в выражение константы равновесия:
Увеличение концентрации I2 и уменьшение концентрации HI приведет к сдвигу равновесия в сторону прямой реакции. Увеличение давления не вызовет сдвига равновесия. 5. При определенных условиях в системе установилось равновесие: 2NO + O2 ⇄ 2NO2. Равновесные концентрации веществ составили: [NO] = 4 моль/л; [O2] = 6 моль/л; [NO2] = 10 моль/л. Найти исходные концентрации NО и О2. Решение. Исходные концентрации равны сумме равновесных концентраций и концентраций вступивших в реакции веществ. Последние можно определить из стехиометрических соотношений: С(NO)прореаг. = [NO2] = 10 моль/л; С(O2)прореаг. = Отсюда: С0(NO) = [NO] + С(NO)прореаг. = 4 + 10 = 14 моль/л; С0(O2) = [O2] + С(O2)прореаг. = 6 + 5 = 11 моль/л. Вопросы для самоконтроля 1. Какие реакции называют обратимыми? Какие необратимыми? Приведите примеры. 2. Что называется химическим равновесием? Сформулируйте термодинамическое и кинетическое определение состояния химического равновесия. 3. Прекращаются ли реакции после наступления равновесия? 4. Как формулируется закон действующих масс для обратимой реакции? 5. Концентрации каких фаз входят в выражение закона действующих масс для обратимой реакции? 6. Что такое константа равновесия? 7. От каких факторов зависит и от каких не зависит константа равновесия? 8. Может ли К быть равной нулю? 9. Какова взаимосвязь между Kc и Kp? 10. Сформулируйте принцип Ле Шателье. Какие факторы влияют на химическое равновесие? 11. Сформулируйте частные принципы смещения равновесия при изменении температуры, концентрации, давления. 12. Смещает ли равновесие в системе введение в нее катализатора?
Варианты задачи для самостоятельного решения Вариант №1 1. Реакция взаимодействия азота с водородом обратима: N2 + 3H2 ⇄ 2NH3. В состоянии равновесия концентрации участвующих в реакции веществ составляют: С(N2) = 0,8 моль/л; С(H2) = 4,8 моль/л; С(NH3) = 0,6 моль/л. Вычислить исходные концентрации азота и водорода. 2. Константа равновесия для реакции: CH4 + Cl2 ⇄ CH3Cl + HCl при 800С равна 1. Исходные концентрации взятых веществ составляли: С(CH4) = 2 моль/л; С(Cl2) = 6 моль/л. Рассчитать, при каких концентрациях всех четырех веществ установилось равновесие. Вариант №2 1. Реакция протекает по уравнению: H2 + Cl2 ⇄ 2HCl. Рассчитать константу химического равновесия, если в реакцию вступило 30% С12. Начальные концентрации веществ равны: С(H2) = 3 моль/л; С(Cl2) = 6 моль/л. 2. При состоянии химического равновесия в системе: 2CO + O2 ⇄ 2CO2 концентрации веществ равны: С(CO) = 5 моль/л; С(O2) = 3 моль/л; С(CO2) = 8 моль/л. Найти исходные концентрации СО и О2. Вариант №3 1. Равновесие реакции: C2H2 + 2H2 ⇄ C2H6 установилось при следующих концентрациях газов: С(C2H2) = 2 моль/л; С(H2) = 1 моль/л; С(C2H6) = 3 моль/л. Рассчитать константу равновесия этой системы и исходные концентрации ацетилена и водорода. 2. Реакция описывается уравнением: A + B ⇄ C + D. Начальные концентрации веществ равны: С(A) = 0,4 моль/л; С(B) = 0,6 моль/л. Константа химического равновесия равна 1. Рассчитать равновесные концентрации всех четырех веществ.
Вариант №4 1. При состоянии химического равновесия в системе: N2 + 3H2 ⇄ 2NH3 концентрации веществ составляют: С(N2) = 2 моль/л; С(H2) = 4 моль/л; С(NH3) = 9 моль/л. Найти исходные концентрации азота и водорода. 2. Константа химического равновесия для реакции: СO2 + H2 ⇄ CO + H2O(пар) при определенной температуре равна 1. Исходные концентрации составляли: С(СO2) = 4 моль/л; С(H2) = 9 моль/л. Рассчитать, при каких концентрациях всех четырех веществ установилось равновесие. Вариант №5 1. При состоянии химического равновесия в системе: Cl2 + 2NO ⇄ 2NOCl концентрации участвующих в реакции веществ составляют: С(Cl2) = 2 моль/л; С(NO) = 6 моль/л; С(NOCl) = 9 моль/л. Рассчитать исходные концентрации веществ С12 и NO. 2. При взаимодействии азота и водорода установилось равновесие: N2 + 3H2 ⇄ 2NH3. Исходные концентрации азота и водорода равны: С(N2) = 2 моль/л; С(H2) = 1 моль/л. Равновесная концентрация азота С(N2) = 1,8 моль/л. Найти равновесные концентрации водорода и аммиака. Вариант №6 1. Реакция протекает по уравнению: H2 + I2 ⇄ 2HI. В равновесной смеси при температуре 4000С: С(H2) = 0,5 моль/л; С(I2) = 0,2 моль/л; С(HI) = 0,4 моль/л. Вычислить константу равновесия реакции при указанной температуре и исходные концентрации Н2 и I2.
2. Константа равновесия реакции: CH3COOH + C2H5OH ⇄ CH3COOC2H5 + H2O при температуре 120С равна 1. Определить равновесные концентрации всех четырех веществ, если исходные концентрации веществ равны: С(CH3COOH) = 1 моль/л; С(C2H5OH) = 0,2 моль/л. Вариант №7 1. Равновесие реакции: 2Cl2 + O2 ⇄ 2Cl2O установилось при следующих концентрациях газов: С(Cl2) = 5 моль/л; С(O2) = 7 моль/л; С(Cl2O) = 3 моль/л. Рассчитать константу равновесия системы и исходные концентрации С12 и О2. 2. Реакция выражается уравнением: A + B ⇄ C + D. Начальные концентрации веществ: С(A) = 1 моль/л; С(B) = 3 моль/л. Константа химического равновесия равна 1. Рассчитать, сколько моль С и D образовалось. Вариант №8 1. В системе C2H6 + H2 ⇄ 2CH4 химическое равновесие установилось к моменту, когда 20% Н2 вступило в реакцию. Рассчитать константу химического равновесия, зная, что исходные концентрации были равны: С(H2) = 8 моль/л; С(C2H6) = 3 моль/л. 2. При определенных условиях в системе: 2SO2 + O2 ⇄ 2SO3 установилось химическое равновесие. При этом концентрации всех веществ были следующими: С(SO2) = 5 моль/л; С(O2) = 6 моль/л; С(SO3) = 10 моль/л. Вычислить исходные концентрации SO2 и О2. Вариант №9 1. При состоянии химического равновесия в системе: N2 + 3H2 ⇄ 2NH3 концентрации участвующих в реакции веществ составили: С(N2) = 3 моль/л; С(H2) = 6 моль/л; С(NH3) = 9 моль/л. Вычислить исходные концентрации Н2 и N2. В каком направлении сместится равновесие, если в системе: а) увеличить давление; б) уменьшить концентрацию водорода. 2. Вычислить константу химического равновесия для реакции: H2 + Cl2 ⇄ 2HCl, если известно, что равновесие наступит тогда, когда прореагирует 50% Н2. Исходные концентрации: С(H2) = 6 моль/л; С(Cl2) = 8 моль/л.
Вариант №10 1. В системе установилось равновесие: H2 + Cl2 ⇄ 2HCl. Исходные концентрации С(H2) = 2 моль/л; С(Cl2) = 3 моль/л. Константа равновесия равна 4. Рассчитать равновесные концентрации всех веществ в системе. 2. При нагревании диоксида азота в закрытом сосуде до некоторой температуры равновесие реакции: 2NO2 ⇄ 2NO + O2 установилось при следующих концентрациях: С(NO2) = 0,5 моль/л; С(NO) = 1,2 моль/л; С(O2) = 0,6 моль/л. Вычислить константу равновесия реакции для этой температуры и найти исходную концентрацию NO2. Вариант №11 1. При взаимодействии азота и водорода установилось равновесие: N2 + 3H2 ⇄ 2NH3. Исходные концентрации азота и водорода составляли: С(N2) = 2 моль/л; С(H2) = 6 моль/л. Равновесная концентрация азота равна: С(N2) = 1,5 моль/л. Рассчитать равновесные концентрации водорода и аммиака. 2. Равновесие реакции: C2H4 + H2 ⇄ C2H6 установилось при следующих концентрациях газов: С(C2H4) = 0,6 моль/л; С(H2) = 0,4 моль/л; С(C2H6) = 1,2 моль/л. Рассчитать константу равновесия этой системы, а также исходные концентрации С2Н4 и Н2. Вариант №12 1. Вычислить константу химического равновесия для реакции: N2 + 3H2 ⇄ 2NH3, если известно, что равновесие наступит тогда, когда прореагирует 50% Н2. Исходные концентрации: С(N2) = 0,8 моль/л; С(H2) = 2,4 моль/л. 2. При нагревании оксида серы (VI) в закрытом сосуде до некоторой температуры равновесие реакции: 2SO3 ⇄ 2SO2 + O2 установилось при следующих концентрациях: С(SO3) = 0,8 моль/л; С(SO2) = 3,2 моль/л; С(O2) = 1,6 моль/л. Вычислить исходную концентрацию SO3.
Вариант №13 1. Реакция взаимодействия азота и водорода обратима: N2 + 3H2 ⇄ 2NH3. В состоянии равновесия концентрации участвующих в реакции веществ равны: С(N2) = 0,3 моль/л; С(H2) = 0,2 моль/л; С(NH3) = 0,2 моль/л. Вычислить исходные концентрации азота и водорода. 2. Константа химического равновесия для реакции: CH4 + Cl2 ⇄ CH3Cl + HCl при 300К равна 1. Исходные концентрации взятых веществ: С(CH4) = 5 моль/л; С(Cl2) = 4 моль/л. Рассчитать, при каких концентрациях всех четырех веществ установилось равновесие. Вариант №14 1. При нагревании СОС12 в закрытом сосуде до некоторой температуры равновесие реакции: COCl2 ⇄ CO + Cl2 установилось при следующих концентрациях: С(COCl2) = 3 моль/л; С(CO) = 6 моль/л. Вычислить константу химического равновесия для данной реакции и исходную концентрацию СОСl2. 2. В системе H2 (газ) + I2 (газ) ⇄ 2HI (газ) установилось равновесие. Исходные концентрации веществ равны: С(H2) = 0,2 моль/л; С(I2) = 0,4 моль/л. Константа равновесия равна 4. Рассчитать равновесные концентрации всех веществ в системе. Вариант №15 1. При определенных условиях в системе установилось равновесие: Cl2 + 2O2 ⇄ 2ClO2. При этом равновесные концентрации веществ равны: С(Cl2) = 4 моль/л; С(O2) = 8 моль/л; С(ClO2) = 10 моль/л. Вычислить исходные концентрации хлора и кислорода. 2. Реакция протекает по уравнению: 2CO + O2 ⇄ 2CO2. Рассчитать константу химического равновесия, если в реакцию вступило 50% О2. Начальные концентрации веществ равны: С(CO) = 5 моль/л; С(O2) = 2 моль/л.
Вариант №16 1. При взаимодействии хлора и оксида азота (II) установилось равновесие: 2NO + Cl2 ⇄ 2NOCl. Исходные концентрации хлора и оксида азота (II) равны: С(NO) = 6 моль/л; С(Cl2) = 3 моль/л. Равновесная концентрация хлора: С(Cl2) = 1,5 моль/л. Найти равновесные концентрации NO и NOC1. 2. Равновесие реакции С2H2 + 2H2 ⇄ C2H6 установилось при следующих концентрациях газов: С(С2H2) = 2 моль/л; С(H2) = 4 моль/л; С(С2H6) = 3 моль/л. Рассчитать константу химического равновесия этой системы и исходные концентрации С2Н2 и Н2. Вариант №17 1. Реакция протекает по уравнению: H2 + Br2 ⇄ 2HBr. Равновесная смесь при температуре 2000С содержит С(H2) = 4 моль/л; С(Br2) = 0,2 моль/л; С(HBr) = 0,8 моль/л. Вычислить константу химического равновесия реакции при указанной температуре и исходные концентрации Н2 и Вr2. 2. Константа равновесия реакции: CO2 + H2 ⇄ CO + H2O (пар) при некоторой температуре равна 1. Определить равновесные концентрации всех четырех веществ, если исходные концентрации веществ равны: С(CO2) = 2 моль/л; С(H2) = 3 моль/л. Вариант №18 1. В системе 2SO2 + O2 ⇄ 2SO3 установилось химическое равновесие к моменту, когда прореагировало 60% О2. Рассчитать константу химического равновесия, зная, что исходные концентрации составляли: С(SO2) = 6 моль/л; С(O2) = 4 моль/л. 2. При определенных условиях в системе CO2 + H2 ⇄ CH3OH установилось химическое равновесие. При этом концентрации всех веществ составили: С(CO) = 0,8 моль/л; С(H2) = 1 моль/л; С(CH3OH) = 6 моль/л. Вычислить исходные концентрации СО и Н2. БЛОК ИНФОРМАЦИИ
РАСТВОРЫ Общие сведения Растворы - это гомогенные системы переменного состава, состоящие из двух и более веществ, называемых компонентами. По агрегатному состоянию растворы могут быть газообразными (воздух), жидкими (кровь, лимфа) и твердыми (сплавы). В медицине наибольшее значение имеют жидкие растворы, которые играют исключительную роль в жизнедеятельности живых организмов. С образованием растворов связаны процессы усвоения пищи и выведения из организма продуктов жизнедеятельности. В форме растворов вводится большое количество лекарственных препаратов. Для качественного и количественного описания жидких растворов используются термины «растворитель» и «растворенное вещество», хотя в некоторых случаях такое разделение является достаточно условным. Так, медицинский спирт (96% раствор этанола в воде) скорее следует рассматривать как раствор воды в спирте. Все растворители делятся на неорганические и органические. Важнейшим неорганическим растворителем (а в случае биологических систем – единственным) является вода. Это обусловлено такими свойствами воды, как полярность, низкая вязкость, склонность молекул к ассоциации, относительно высокие температуры кипения и плавления. Растворители органической природы разделяют на полярные (спирты, альдегиды, кетоны, кислоты) и неполярные (гексан, бензол, четыреххлористый углерод). Процесс растворения в равной степени зависит как от природы растворителя, так и от свойств растворенного вещества. Очевидно, что способность образовывать растворы выражена у разных веществ по-разному. Одни вещества могут смешиваться друг с другом в любых количествах (вода и этанол), другие – в ограниченных (вода и фенол). Однако, следует помнить: абсолютно нерастворимых веществ не существует! Склонность вещества растворяться в том или ином растворителе можно определить, используя простое эмпирическое правило: подобное растворяется в подобном. Действительно, вещества с ионным (соли, щелочи) или полярным (спирты, альдегиды) типом связи хорошо растворимы в полярных растворителях, например, в воде. И наоборот, растворимость кислорода в бензоле на порядок выше чем в воде, так как молекулы O2 и C6H6 неполярны. Степень сродства соединения к определенному типу растворителя можно оценить, анализируя природу и количественное соотношение входящих в его состав функциональных групп, среди которых выделяют гидрофильные (притягивающие воду) и гидрофобные (отталкивающие воду). К гидрофильным относят полярные группы, такие как гидроксильная (-OH), карбоксильная (-COOH), тиольная (-SH), амино (-NH2). Гидрофобными считают неполярные группы: углеводородные радикалы алифатического (-CH3, -C2H5) и ароматического (-C6H5) рядов. Соединения, имеющие в своем составе как гидрофильные, так и гидрофобные группы, называют дифильными. К таким соединениям относят аминокислоты, белки, нуклеиновые кислоты. Теории растворов В настоящее время известны две основные теории растворов: физическая и химическая.
|
|||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-15; просмотров: 2921; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.92.96 (0.013 с.) |

 = -43,0 кДж
= -43,0 кДж , кДж/моль
, кДж/моль
 =
= 

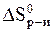 = -0,1978 кДж/К.
= -0,1978 кДж/К.


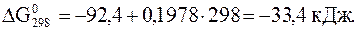





 = 5 моль/л.
= 5 моль/л.


