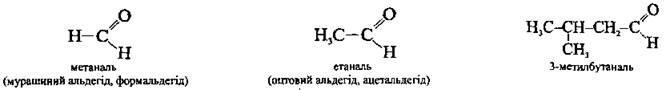Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Номенклатура альдегідів і кетонівСодержание книги
Поиск на нашем сайте
Систематичні назви альдегідів складають за назвою відповідного вуглеводню з додаванням суфікса -аль. Нумерацію ланцюга починають з карбонільного атома Карбону. Тривіальні назви складають від тривіальних назв тих кислот, на які альдегіди перетворюються в результаті окиснення. Систематичні назви кетонів нескладної будови утворюють від назв радикалів (у порядку збільшення) з додаванням слова «кетон» (радикально-функціональна). Наприклад: CH3 - CO - CH3 — диметилкетон (ацетон); CH3CH2CH2 - CO - CH3 — метилпропілкетон. У більш загальному випадку назва кетону складається за назвою відповідного вуглеводню й суфікса -он; нумерацію ланцюга починають з кінця ланцюга, що знаходиться найближче до карбонільної групи (замісна номенклатура IUPAC). Наприклад: CH3 - CO - CH3 — пропанон (ацетон); CH3CH2CH2 - CO - CH3 — 2-пентанон; CH2 = CH - CH2 - CO - CH3 — 4-пентен-2-он. Ізомерія альдегідів і кетонів Для альдегідів і кетонів характерною є структурна ізомерія. Ізомерія альдегідів: • ізомерія карбонового скелета, починаючи із C4:
• міжкласова ізомерія з кетонами, починаючи із C3:
• із циклічними оксидами, починаючи із C2:
• з ненасиченими спиртами й етерами, починаючи із C3:
Класифікація альдегідів
47.Методи одержання аліфатичних оксосполук.
48.Хімічні властивості аліфатичних альдегідів і кетонів. Хімічні властивості альдегідів Хімічні властивості альдегідів зумовлені наявністю в їхніх молекулах карбонільної групи. Полярність карбонільного зв’язку робить легким приєднання полярних реагентів. Також для альдегідів характерні реакції приєднання за рахунок розриву π-зв’язку.
49.Ненасичені альдегіди і кетони: загальна характеристика, окремі представники. Ненасичені альдегіди і кетони, залежно від взаємного розташування подвійний і карбонільної груп в молекулі, можуть бути поділені на три групи: з сполученими (CH = CH2-COCH3 - метілвінілкетон, бутен-1-3-он; CH2 = CHCHO - акролеїн, пропеналь), кумулірованними (кетени CH2 = C = O) і ізольованими (CH2 = CHCH2CH2CH2COCH3) зв'язками. Найважливішими представниками ненасичених альдегідів є акролеїн CH2 = CH-CHO і кротоновий альдегід CH3-CH = CH-CHO. Акролеї́н або акри́ловий альдегі́д (від лат. acer, acris — «гострий» і oleum — «олія», рос. акролеин, англ. acrolein, нім. Akrolein, Propenal) — С3Н4О або СН2=СНСНО, органічна сполука з їдким запахом, найпростіший ненасичений альдегід, що має дуже високу реакційну здатність завдяки наявності альдегідної групи і подвійного зв'язку. Це безбарвна летка рідина з жовтуватим відтінком, неприємним різким їдким запахом пригорілих жирів, дуже отруйна, сильно подразнює слизову оболонкуочей. У повітрі присутня у вигляді парів, які в 1,9 разів важчі за неї і добре розчиняються у воді. Легкозаймиста; добре розчиняється в органічних розчинниках; розчинність у воді 40 г в 100 мл. Акролеїн класифікують як отруйну речовину. При зберіганні він полімеризується в тверду склоподібну масу — діакрил. Для стабілізації акролеїну додають гідрохінон. На повітрі акролеїн окиснюється в пропенову кислоту. Кротоновий альдегід (англ. Crotonaldehyde) - органічна сполука з формулою CH3CH = CHCHO. Відноситься до ненасичених альдегідів. Цис-кротоновий альдегід нестійкий і легко переходить в транс-ізомер. Кротоновий альдегід являє собою безбарвну рідина з різким запахом. Розчиняється в етанолі, діетиловому ефірі, ацетоні, бензолі.
50. Ароматичні альдегіди ікетони:загальнахарактеристика,окремі представники. Аромати́чні альдегі́ди і кето́ни — сполуки, що містять альдегідну -СH=О або карбонільну групу >С=О в молекулі з одним як мінімум ароматичним ядром. Вони бувають чисто ароматичними або аліфатично ароматичними. Назви альдегідів за систематичною номенклатурою IUPAC утворюють з назви аренового залишку Ar і закінчення карбальдегід. Для С6Н5-СОН переважно застосовують напівтривіальну назву бензальдегід поряд з бензолкарбальдегідом, або бензенкарбальдегідом. Широко використовують тривіальні назви ароматичних альдегідів від назв відповідних кислот, в які вони переходять при окисненні. Назви ароматичних кетонів за систематичною номенклатурою утворюються від назв вуглеводнів, у структурі яких розміщенні арильні залишки, і закінчення -он. Для радикально-функціональної номенклатури назви складаються з назв вуглеводневих груп, перелічених за алфавітом та закінчення -кетон.
51.Сульфуровмісні органічні сполуки:загальна характеристика і класифікація сполук. Деякі сульфуровмісні органічні сполуки можна розглядати як похідні від тіокарбонових кислот. Із усіх можливих тіокарбонових кислот у вільному стані лише тритіокарбонова кислота є стійкою. Найбільш поширеними сульфуровмісними сполуками як похідними від розглянутих тіокарбонових кислот є тіоли (меркаптани (mercaptans), сульфіди, дисульфіди, тіосечовини, тіоаміди, ксантогенати, дитіокарбамати та тіурами. Деякі найбільш характерні реакції сульфуровмісних органічних сполук наведені нижче.
У молекулі бензену всі атоми Карбону рівноцінні, тому реакції заміщення, які проходять за участю будь-якого з них, призводять до утворення одного продукту. Якщо ж у молекулі бензену з’являється замісник, то він визначає місце вступу другого замісника в бензенове ядро (орієнтуюча дія замісника). Цей вплив відбувається через перерозподіл електронної густини в молекулі бензену. За впливом на напрям реакції заміщення, усі замісники, або орієнтанти, поділяють на дві групи: 1) замісники першого роду, або орто- і пара-орієнтанти, спрямовують наступний замісник в орто- та пара- положення. Це – орієнтанти насиченого типу. До них відносять електронодонорні замісники, що збільшують електронну густину в бензеновому ядрі. Вони, як правило, прискорюють реакції заміщення (винятком є галогени – F, Cl, Br та I, які дезактивують бензенове ядро). Наприклад: Alk, OH, NH2, Hal та ін. 2) замісники другого роду, або мета-орієнтанти, спрямовують наступний замісник в мета- положення. Вони – орієнтанти ненасиченого типу. Це – електроноакцепторні замісники, що дезактивують бензенове ядро, зменшуючи у ньому електронну густину і тим самим зменшують швидкість реакцій заміщення. Наприклад: NO2, CHO, COOH та ін.
34.Аліфатичні галогенопохідні: методи одержання та хім.. властивості.
|
|||||||||
|
Последнее изменение этой страницы: 2016-08-15; просмотров: 706; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.113 (0.006 с.) |