Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Этиология, патогенез, проявленияСодержание книги
Поиск на нашем сайте
Тема: Патофизиология печени
Печень – жизненно важный орган с многообразными функциями, направленными на поддержание гомеостаза в организме. Структурно-функциональная единица печени - печеночный ацинус. В печени происходят: 1. Образование желчных пигментов, синтез холестерина, синтез и секреция желчи. 2. Обезвреживание токсичных продуктов, поступающих из желудочно-кишечного тракта. 3. Синтез белков, в том числе протеинов плазмы крови, их депонирование, переаминирование и дезаминирование аминокислот, образование мочевины и синтез креатина. 4. Синтез гликогена из моносахаридов и неуглеводных продуктов. 5. Окисление жирных кислот, образование кетоновых тел. 6. Депонирование и обмен многих витаминов (A, PP, B, D, K), депонирование ионов железа, меди, цинка, марганца, молибдена и др. 7. Синтез большинства ферментов, обеспечивающих метаболические процессы. 8. Регуляция равновесия между свертывающей и антисвертывающей системами крови, образование гепарина. 9. Разрушение некоторых микроорганизмов, бактериальных и других токсинов. 10. Депонирование плазмы крови и форменных элементов, регуляция системы крови. 11. Кроветворение у плода. Печеночная недостаточность. Этиология, патогенез, проявления
Печёночная недостаточность – стойкое снижение или полное выпадением одной, нескольких или всех функций печени, приводящее к нарушению жизнедеятельности организма. Классификация Выделяют несколько видов печёночной недостаточности.
Рис. 1. Виды печёночной недостаточности.
По происхождению. • Печёночно-клеточная (паренхиматозная). Является результатом первичного повреждения гепатоцитов и недостаточности их функции. • Шунтовая (обходная). Обусловлена нарушением тока крови в печени и, в связи с этим, её сбросом (минуя печень) по портокавальным анастомозам в общий кровоток. По скорости возникновения и развития. • Острая. Развивается в течение нескольких суток. • Хроническая. Формируется в течение нескольких недель, месяцев или лет. По числу нарушенных функций: парциальная и тотальная. В зависимости от обратимости повреждения гепатоцитов. • Обратимая. Исчезновение признаков печеночной недостаточности наблюдается при прекращении воздействия патогенного агента и устранении последствий этого воздействия. • Необратимая (прогрессирующая). Развивается в результате продолжающегося влияния причинного фактора или неустранимости патогенных изменений, вызванных им.
Проявления печеночной недостаточности Печёночная недостаточность характеризуется признаками расстройств обмена веществ и функций печени. Нарушение углеводного обмена. Печень участвует в поддержании нормального уровня глюкозы в сыворотке крови путем гликогеногенеза, гликогенолиза и глюконеогенеза. Снижается способность гепатоцитов, с одной стороны, превращать глюкозу в гликоген, а с другой – расщеплять гликоген до глюкозы. Это обусловливает характерный признак печеночной недостаточности – неустойчивый уровень глюкозы крови. После приема пищи развивается гипергликемия, а натощак – гипогликемия. Нарушение белкового и ферментного обменов проявляется в изменении расщепления белков (до аминокислот), синтеза белков, дезаминирования, трансаминирования, декарбоксилирования аминокислот, образования мочевины, мочевой кислоты, аммиака, креатина. Вследствие этого возникают следующие нарушения: Гипопротеинемия – снижение уровня белка обычно отражает нарушение белково-синтетической функции печени. Гепатоциты синтезируют практически весь альбумин, до 85% глобулинов. Диспротеинемия развивается при синтезе в печени качественно измененных глобулинов (парапротеинов – макроглобулинов, криоглобулинов). Нарушение метаболизма аминокислот приводит к повышению уровня свободных аминокислот в крови и моче (аминоацидемия, аминоацидурия). Геморрагический синдром развивается вследствие нарушения синтеза факторов свертывания и ингибиторов коагуляции и фибринолиза. Увеличение остаточного азота и аммиака в крови обнаруживается при нарушении синтеза мочевины (показатель тяжелой печеночной недостаточности). Повышение содержания в крови ряда ферментов (аминотрансфераз и др.). Наибольшее диагностическое значение имеет определение в сыворотке крови активности аминотрансфераз - АлАТ и АсАТ. Их активность является наиболее надежным показателем цитолиза гепатоцитов. Из маркёров холестаза (экскреторные ферменты) наибольшее клиническое значение приобретает определение в крови активности щелочной фосфатазы. Повышение активности щелочной фосфатазы является важным показателем нарушения жёлчеоттока (холестаза). Нарушение жирового обмена. • Нарушение синтеза в гепатоцитах ЛПНП и ЛПОНП (обладающих атерогенными эффектами), а также ЛПВП (оказывающих антиатерогенное действие) нередко сопровождается развитием липидной дистрофии печени (жирового гепатоза). • Повышение в плазме крови уровня холестерина (обладающего проатерогенным свойством). Нарушение обмена гормонов. Нарушение обмена гормонов и биологически активных веществ проявляется в изменении: • синтеза гормонов (из фенилаланина образуется тирозин – предшественник тироксина, трийодтиронина, катехоламинов), транспортных белков (транскортина, связывающего 90% глюкокортикоидов); • инактивации гормонов (стероидных гормонов, катехоламинов, инсулина); • инактивации биологически активных веществ (окислительного дезаминирования серотонина и гистамина). Поражение печени и нарушение инактивации таких гормонов, как инсулин, тироксин, кортикостероиды, андрогены, эстрогены ведет к изменению их содержания в крови и развитию соответствующей эндокринной патологии. Уменьшение дезаминирования БАВ может усугубить клинические проявления аллергии при патологии печени. Нарушение обмена витаминов характеризуется: • уменьшением всасывания жирорастворимых витаминов (A, D, E, K) в результате нарушения желчевыделительной функции печени; • нарушением синтеза витаминов и образования активных форм (вит. А из каротина, активных форм витамина В6 и др.); • нарушением депонирования витаминов (В12, фолиевой, никотиновой кислот и др.) и их экскреции. В результате нарушения обмена витаминов многие патологические процессы в печени могут сопровождаться гиповитаминозами. Нарушение обмена минеральных веществ (железо, медь, хром). Например, при наследственной патологии — гемохроматозе в ткани печени накапливается железо, развиваются гепатомегалия и цирроз. Нарушения функций печени. Дезинтоксикационная функция. Характеризуется снижением эффективности процессов детоксикации в печени: • эндогенных токсинов (образующихся и накапливающихся в кишечнике — фенолов, скатолов, аммиака, путресцина, кадаверинов и патогенных продуктов метаболизма — низкомолекулярных жирных кислот, сульфатированных аминокислот и др.); • экзогенных ядовитых веществ (например, токсинов грибов и микробов; ядохимикатов; ЛС). Антимикробная функция. При печёночной недостаточности страдают фагоцитоз клетками Купфера различных микроорганизмов, транспорт IgА в жёлчь, где они оказывают бактериостатическое и бактерицидное действие. Желчеобразование и желчевыделение (с развитием желтух и нарушений пищеварения). Синдром желтухи. Синдром эндокринных расстройств. Отмечаются снижение либидо, атрофия яичек, бесплодие, гинекомастия, атрофия молочных желез, матки, нарушение менструального цикла. Возможно развитие сахарного диабета и вторичного альдостеронизма; Синдром нарушенной гемодинамики – накопление гистаминоподобных и других вазоактивных веществ, приводящее к вазодилатации (компенсаторное повышение сердечного выброса в сочетании с гипотензией). Отечно-асцитический синдром обусловливают снижение синтеза альбуминов и падение онкотического давления, а также развитие вторичного альдостеронизма. Специфический печеночный запах (fetor hepaticis) связан с выделением метилмеркаптана. Это вещество образуется из метионина, который накапливается в связи с нарушением в печени процессов деметилирования и может содержаться в выдыхаемом воздухе; «Печеночные знаки» – телеангиэктазии (сосудистые звёздочки) и пальмарная эритема. Синдром геморрагического диатеза – снижение синтеза факторов свертывания крови и частые кровотечения обусловливают возможность развития ДВС-синдрома.
Виды печеночной комы. • Паренхиматозная кома. Интоксикация организма в связи с повреждением и гибелью значительной массы печени (например, при её травме, некрозе, удалении). В результате этого нарушаются все функции печени. Наибольшее патогенное значение при этом имеет утрата дезинтоксикационной функции. • Шунтовая кома («обходная»). При сбросе крови из системы портальной вены в общий кровоток, минуя печень. Чаще возникает при циррозах в случае развития мощных коллатералей между системами воротной и нижней полой вен.
Рис. 4. Основные факторы патогенеза печёночных коматозных состояний.
Патогенез печеночной комы. • Гипогликемия. Является результатом нарушения гликогенеза и гликогенолиза. • Ацидоз (метаболический, на финальных стадиях дополнительно развивается респираторный и выделительный ацидоз). • Дисбаланс ионов в клетках, интерстициальной жидкости и в крови (в крови нарастает [K+], в клетках — [Na+], [Ca2+], [H+]). • Интоксикация организма — эндотоксинемия (особенно продуктами белкового и липидного метаболизма, а также непрямым билирубином, что обусловлено нарушением его трансформации и конъюгации с глюкуроновой кислотой). • Нарушения центральной, органно-тканевой и микрогемоциркуляции как следствие сердечной недостаточности, нарушения тонуса артериол. • Полиорганная недостаточность. Ранее всего и наиболее выраженно нарушается функции сердца, дыхательного и сосудодвигательного центров. Последнее приводит к смешанной гипоксии, прекращению сердечной деятельности, дыхания и смерти пациента.
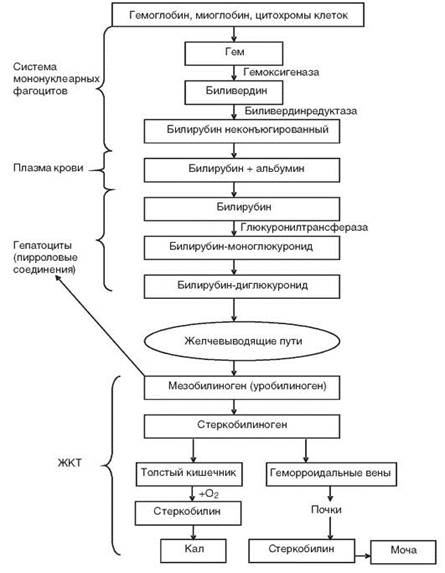
Метаболизм билирубина. • Высвобождение гема из гемоглобина, миоглобина и цитохромов. Более 80% гема образуется в результате разрушения эритроцитов и около 20% — миоглобина и цитохромов. • Трансформация протопорфирина гема в биливердин. Происходит под влиянием микросомальных оксидаз гепатоцитов. • Окисление биливердина с образованием непрямого билирубина (неконъюгированный, свободный билирубин). Непрямой билирубин, циркулирующий в крови, связан с альбуминами и поэтому не фильтруется в почках и отсутствует в моче. • Транспорт непрямого билирубина в гепатоциты, где он образует комплекс с белками и глутатион–S–трансферазами. • Диглюкуронизация билирубина в гепатоцитах с образованием растворимого в воде конъюгированного билирубина. Прямой билирубин не связан с альбумином. В связи с этим он активно («прямо») взаимодействует с диазореактивом Эрлиха, выявляющим этот пигмент. • Экскреция конъюгированного билирубина в желчевыводящие пути. Очень важным является положение о том, что в нормальных условиях транспорт билирубина через гепатоцит происходит только в одном направлении – от кровеносного к жёлчному капилляру. При повреждении гепатоцита (некроз) или препятствии для прохождения жёлчи (на уровне жёлчных ходов или ниже) возможна регургитация конъюгированного билирубина, его движение в обратном направлении – в кровеносный капилляр. Метаболизм билирубина в печени осуществляется в три этапа: 1. захват гепатоцитом билирубина из крови, 2. связывание билирубина с глюкуроновой кислотой (обеспечивает фермент глюкуронилтрансфераза), 3. выделение конъюгированного билирубина в систему жёлчных протоков. • Трансформация конъюгированного билирубина: - в уробилиноген (в верхнем отделе тонкой кишки), всасывающийся в тонкой кишке и попадающий по системе воротной вены в печень, где разрушается в гепатоцитах. - в стеркобилиноген (в основном в толстом кишечнике), большая часть которого выделяется с экскрементами, окрашивая их; другая часть всасывается в кровь геморроидальных вен, попадая в общий кровоток и фильтруется в почках (в норме придавая моче соломенно-жёлтый цвет).
Рис. 5. Метаболизм билирубина. ЖКТ – желудочно-кишечный тракт. Классификация желтух. Все желтухи в зависимости от происхождения подразделяют на две группы: печёночные и непечёночные.
Рис. 6. Виды желтух по происхождению.
Печёночные желтухи (паренхиматозные и энзимопатические) возникают при первичном повреждении гепатоцитов. Непечёночные желтухи первично не связаны с повреждением гепатоцитов. К ним относятся гемолитические (надпечёночные) и механические (подпечёночные) желтухи. Гемолитическая желтуха. Причины. Избыточное разрушение эритроцитов, обусловленное внутри- и внеэритроцитарными факторами (см. гемолитические анемии). Помимо проявлений, обусловленных гемолизом эритроцитов (анемии, гемоглобинурии), отмечается повышение содержания в крови непрямого билирубина. Это является результатом избыточного его образования из гемоглобина и неспособностью нормального гепатоцита захватить и трансформировать избыточно содержащийся в протекающей крови непрямой билирубин. Избыток непрямого билирубина в крови обусловливает окрашивание кожи и слизистых оболочек (степень окраски зависит от интенсивности гемолиза). Одновременно с эти в большей мере окрашиваются кал и моча, поскольку в них увеличивается концентрация стеркобилиногена (гиперхолия - увеличенная секреция желчи в кишечник). В случае желтухи, обусловленной массивным гемолизом эритроцитов, в крови и моче обнаруживается уробилиноген. В общий кровоток уробилиноген попадает, «проскакивая» печеночный барьер в связи с высокой концентрацией пигмента в крови портальной вены. Это обусловлено в свою очередь избытком образования прямого билирубина в печени, а следовательно – уробилиногена в тонкой кишке, откуда он всасывается в портальную вену и поступает в печень. Механическая желтуха. Механическая желтуха развивается при стойком нарушение выведении жёлчи по жёлчным капиллярам (что приводит к внутрипечёночному холестазу), по жёлчным протокам и из жёлчного пузыря. Причины. • Закрывающие желчевыводящие пути изнутри (например, конкременты, опухоли, паразиты). • Сдавливающие жёлчные пути снаружи (например, новообразования головки поджелудочной железы или большого дуоденального сосочка; рубцовые изменения ткани вокруг желчевыводящих путей; увеличенные лимфоузлы). • Нарушающие тонус и снижающие моторику стенок желчевыводящих путей (дискинезии). Патогенез. Указанные факторы обусловливают повышение давления в жёлчных капиллярах, перерастяжение (вплоть до микроразрывов) и повышение проницаемости стенок желчеотводящих путей, диффузию компонентов жёлчи в кровь. В случаях острой полной обтурации жёлчевыводящих путей возможен разрыв жёлчных капилляров. При этом жёлчь, вступая в контакт с печеночной тканью, вызывает ее повреждение и развитие воспалительного процесса, что получило название билиарного гепатита. Признаки холемии. • Высокая концентрация конъюгированного билирубина в крови (с развитием желтухи) и как следствие — в моче (придает моче тёмный цвет). • Избыток холестерина накапливается в тканях в виде ксантом (в коже кистей, предплечий, стоп). • Зуд кожи вследствие раздражения жёлчными кислотами нервных окончаний. • Артериальная гипотензия вследствие снижения базального тонуса ГМК артериол, уменьшение адренореактивных свойств рецепторов сосудов и сердца, повышения тонуса бульбарных ядер блуждающего нерва под действием жёлчных кислот. • Брадикардия вследствие прямого тормозного влияния жёлчных кислот на клетки синусно-предсердного узла. • Повышенная раздражительность и возбудимость пациентов в результате снижения активности тормозных нейронов коры больших полушарий под действием компонентов жёлчи. • Депрессия, нарушение сна и бодрствования, повышенная утомляемость (развивается при хронической холемии). Синдром ахолии — состояние, характеризующееся значительным уменьшением или прекращением поступления жёлчи в кишечник, сочетающееся с нарушением полостного и мембранного пищеварения. Признаки ахолии. • Стеаторея — наличие жира в кале, что обусловлено нарушением эмульгирования, переваривания и усвоения жира в кишечнике в связи с дефицитом жёлчи. • Дисбактериоз. • Кишечная аутоинфекция и интоксикация вследствие отсутствия бактерицидного и бактериостатического действия жёлчи. Это способствует активации процессов гниения и брожения в кишечнике и развитию метеоризма. • Полигиповитаминоз (в основном, за счёт дефицита жирорастворимых витаминов A, D, E, K). Дефицит жирорастворимых витаминов приводит к нарушению сумеречного зрения, деминерализации костей с развитием остеомаляции и переломов, снижение эффективности системы антиоксидантной защиты тканей, развитию геморрагического синдрома. • Обесцвеченный кал вследствие уменьшения или отсутствия жёлчи в кишечнике. Печеночная желтуха. К печеночной желтухе относят печеночно-клеточную (паренхиматозную) и энзимопатическую разновидности желтух. Паренхиматозная желтуха развивается при острых и хронических заболеваниях печени любой этиологии (вирусной, алкогольной, аутоиммунной), а также при тяжело протекающих инфекциях (тифы, малярия, острая пневмония), сепсисе, отравлениях грибами, фосфором, хлороформом и другими ядами. Практически при любом варианте повреждения печени нарушается жёлчеобразовательная и жёлчевыделительная функция гепатоцитов в зоне поражения. Ранними специфическими признаками поражения гепатоцитов являются высокий уровень в крови печеночных трансаминаз (АлАТ, АсАТ), легко проникающих через поврежденную клеточную мембрану. В результате поражения гепатоцитов печеночные клетки выделяют жёлчь в кровеносные сосуды (развивается холемический синдром). В крови отмечается гипербилирубинемия как за счет прямого, так и непрямого билирубина, что связано со снижением активности глюкуронилтрансферазы в поврежденных гепатоцитах и нарушением образования прямого билирубина. Моча имеет темный цвет за счет билирубинурии (прямой билирубин) и уробилинурии (нарушено превращение уробилиногена в поврежденных гепатоцитах, всасывающегося в кровь из тонкой кишки и поступающего в печень). Энзимопатические желтухи обусловлены нарушением метаболизма билирубина в гепатоцитах. Речь идет о парциальной форме печеночной недостаточности, связанной с уменьшением или невозможностью синтеза ферментов, участвующих в пигментном обмене. По происхождению эти желтухи, как правило, наследственные. Вместе с тем некоторые формы наблюдаются после перенесенных ранее заболеваний печени. В зависимости от механизма развития выделяют следующие формы энзимопатических желтух. Синдром Жильбера. В основе развития этой желтухи лежит нарушение активного захвата и транспорта непрямого билирубина из крови в печеночную клетку. Причиной её является генетический дефект синтеза соответствующих ферментов. При этом повышение уровня общего билирубина в крови обусловлено увеличением содержания в ней неконъюгированного билирубина. Интенсивность желтухи преходящая, то исчезает, то усиливается. Последнее наблюдается после продолжительного голодания либо соблюдения низкокалорийной диеты, после интеркуррентной инфекции, приема алкоголя. Синдром Криглера-Найяра. Этот вариант желтухи развивается вследствие дефицита глюкуронилтрансферазы – ключевого фермента превращения свободного билирубина в связанный (прямой). Известны две формы этого заболевания: тип I - клинически тяжелая форма, связанная с полным отсутствием глюкуронилтрансферазы (дети обычно погибают на первом году жизни из-за поражения головного мозга), и тип II, связанный с частичным ее дефицитом (заболевание протекает относительно благоприятно). Возможен приобретенный дефицит глюкуронилтрансферазы, возникающий у новорожденных в связи с ингибированием этого фермента рядом лекарственных препаратов (например, левомицетин). Синдром Дабина-Джонсона. Данный вариант желтухи возникает вследствие дефекта ферментов, участвующих в экскреции конъюгированного билирубина через мембрану гепатоцитов в жёлчные капилляры. В результате этого прямой билирубин поступает не только в жёлчные капилляры, но и частично в кровь. Клинически проявляется желтухой с умеренным увеличением содержания в крови прямого билирубина и появлением его в моче. При биопсии печени в гепатоцитах обнаруживают темный, буро-оранжевый пигмент (липохром). Синдром Ротора. Клинически сходен с синдромом Дабина-Джонсона, но в отличие от него при синдроме Ротора отсутствует накопление патологического пигмента в клетках печени.
Тема: Патофизиология печени
Печень – жизненно важный орган с многообразными функциями, направленными на поддержание гомеостаза в организме. Структурно-функциональная единица печени - печеночный ацинус. В печени происходят: 1. Образование желчных пигментов, синтез холестерина, синтез и секреция желчи. 2. Обезвреживание токсичных продуктов, поступающих из желудочно-кишечного тракта. 3. Синтез белков, в том числе протеинов плазмы крови, их депонирование, переаминирование и дезаминирование аминокислот, образование мочевины и синтез креатина. 4. Синтез гликогена из моносахаридов и неуглеводных продуктов. 5. Окисление жирных кислот, образование кетоновых тел. 6. Депонирование и обмен многих витаминов (A, PP, B, D, K), депонирование ионов железа, меди, цинка, марганца, молибдена и др. 7. Синтез большинства ферментов, обеспечивающих метаболические процессы. 8. Регуляция равновесия между свертывающей и антисвертывающей системами крови, образование гепарина. 9. Разрушение некоторых микроорганизмов, бактериальных и других токсинов. 10. Депонирование плазмы крови и форменных элементов, регуляция системы крови. 11. Кроветворение у плода. Печеночная недостаточность. Этиология, патогенез, проявления
Печёночная недостаточность – стойкое снижение или полное выпадением одной, нескольких или всех функций печени, приводящее к нарушению жизнедеятельности организма. Классификация Выделяют несколько видов печёночной недостаточности.
Рис. 1. Виды печёночной недостаточности.
По происхождению. • Печёночно-клеточная (паренхиматозная). Является результатом первичного повреждения гепатоцитов и недостаточности их функции. • Шунтовая (обходная). Обусловлена нарушением тока крови в печени и, в связи с этим, её сбросом (минуя печень) по портокавальным анастомозам в общий кровоток.
|
||||
|
Последнее изменение этой страницы: 2016-08-14; просмотров: 155; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.12.163.23 (0.012 с.) |