
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Выполнение лабораторной работы на занятииСодержание книги
Поиск на нашем сайте
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ВЫПОЛНЕНИЮ ЛАБОРАТОРНЫХ РАБОТ Подготовка к выполнению лабораторной работы Подготовка к выполнению лабораторной работы (домашняя работа) включает следующие этапы: 1. Проработать по конспектам лекций или учебникам соответствующий теоретический материал, имеющий непосредственное отношение к теме лабораторной работы. Теоретические основы каждой работы изложены кратко в настоящем пособии. 2. Ознакомиться с методикой выполнения эксперимента, т.е. с описанием опытов, схемами приборов и установок для выполнения работы. 3. Подготовить лабораторный журнал (тетрадь). Записать заголовок «Лабораторная работа», на следующей строке – название лабораторной работы. Составить краткий конспект в лабораторном журнале. Необходимо выписать главные определения, формулы с указанием всех обозначений и единиц измерения, затем привести перечень необходимых реактивов, посуды и оборудования, описать методику выполнения работы. Переписывать весь текст работы из пособия не следует. Выполнение лабораторной работы на занятии 1. После собеседования получить у преподавателя допуск к выполнению лабораторной работы. 2. Ознакомиться с лабораторной работой на рабочем месте (техникой безопасности, оборудованием, приборами, установкой и т.п.). 3. Выполнить все опыты в соответствии с методикой. Если при выполнении эксперимента возникают затруднения или вопросы, необходимо обязательно обратиться за помощью к преподавателю или лаборанту. 4. Все результаты и наблюдения аккуратно записать в рабочем журнале. При этом следует указывать всю важную информацию, например, названия, формулы используемых веществ, концентрации растворов, температуру, где это необходимо, и т.д. Записывать результаты на отдельных листках не разрешается. 5. Произвести расчеты по экспериментальным данным, если это требуется. 6. Получить у преподавателя письменное подтверждение, что работа выполнена верно. В случае получения неправильных результатов работу нужно переделать.
Оформление работы Если время позволяет, то выполнить эту часть лабораторной работы можно на занятии после выполнения эксперимента. Если же по какой-либо причине времени не хватило, оформить работу можно дома.
1. В лабораторном журнале написать уравнения химических реакций с коэффициентами. Если требуется, записать уравнения в ионном виде. 2. Оформить всю расчетную часть: сделать вычисления по формулам, составить таблицы, построить графики. При выполнении расчетов необходимо указать единицы измерения величин. 3. Графики следует строить на миллиметровой бумаге карандашом. Обязательно указать, какие величины отложены по осям координат. Каждый график должен иметь краткое название. Масштаб следует выбрать так, чтобы его было удобно читать и чтобы из графика можно было извлечь максимум полезной информации. При нанесении экспериментальных точек на график не следует на осях указывать конкретные численные значения переменных. Линию зависимости (прямую или кривую) проводят между точками насколько возможно близко ко всем нанесенным точкам, число точек по обе стороны линии должно быть почти одинаково. После согласования с преподавателем, график аккуратно приклеивается в соответствующем месте лабораторного журнала. 4. Сделать выводы. Вывод должен быть четким, конкретным и соответствовать цели лабораторной работы (содержать конкретный численный результат или выявленную закономерность). Например, «адсорбция уксусной кислоты на активированном угле описывается уравнением Фрейндлиха Защита лабораторной работы Под защитой лабораторной работы подразумевается: 1. Представление преподавателю своего лабораторного журнала (тетради) с полностью оформленной работой и проверка ее преподавателем. 2. Собеседование с преподавателем по теории и методике эксперимента, а также ответы на контрольные вопросы в конце каждой лабораторной работы. Если среди контрольных заданий есть задачи, то они должны быть выполнены в письменной форме в тетради. Сдать работу преподавателю (т.е. защитить ее на оценку) можно на том же занятии, на котором она выполнялась. Если оформление работы требует дополнительного времени (например, в ней есть большая графическая часть), то защита выполненной лабораторной работы проводится на следующем занятии. При подготовке лабораторной работы к защите следует повторить соответствующие разделы по конспекту лекций и учебнику.
ХИМИЧЕСКАЯ ПОСУДА В лаборатории используется стеклянная, фарфоровая, металлическая посуда. Наиболее часто опыты проводят в стеклянной посуде. Стеклянная химическая посуда условно делится на три группы: посуда общего назначения, мерная посуда, специальная посуда. Посуда общего назначения используется для самых разнообразных целей. Изготавливается она из обычного и термостойкого стекла. Пробирки (рис. 1) служат для проведения опытов с небольшими количествами веществ. Обычная лабораторная пробирка имеет размеры 15´150 мм и емкость около 20 мл. При проведении опыта не следует заполнять пробирку более чем на 1/3 объема. Перемешивают реактивы в пробирке легким встряхиванием, постукивая по ней. Нельзя перемешивать вещества резким встряхиванием, закрыв отверстие пробирки пальцем. Нагревают жидкость в пробирке на водяной бане или на открытом пламени, закрепив ее в пробиркодержателе. При этом нагревают не дно пробирки, а сначала верхнюю часть жидкости, затем прогревают всю пробирку. Пробирку держат отверстием от себя и от работающих рядом, чтобы в случае внезапного выброса горячей жидкости она ни на кого не попала. Химические стаканы (рис. 2) – тонкостенные сосуды цилиндрической формы. Они предназначены для выполнения различных операций – приготовления растворов, проведения некоторых химических реакций и т.д. Химические стаканы изготавливаются в соответствии с ГОСТ, емкость их бывает различной – от 50 мл до 2 л. Различаются они и по форме (высокие и низкие, с носиком и без носика). Плоскодонные и конические колбы (рис. 3) применяются для самых различных работ (приготовление растворов, фильтрование и т.д.). Небольшие конические колбы, иначе называемые колбами Эрленмейера, применяются для титрования. Емкость плоскодонных конических колб может быть различной – от 25 мл до 5 л. Изготавливают разнообразные колбы: с узким и широким горлом, с обычным цилиндрическим горлом и с отогнутыми краями, а также со специальным пришлифованным горлом. Такие колбы герметично закрываются специальными пробками стандартных размеров. Если колба изготовлена из термостойкого стекла, на ней имеется соответствующее обозначение: ТС, матовый прямоугольник или кружок. Круглодонные колбы (рис. 4) предназначены для проведения синтезов, могут использоваться при перегонке жидкостей. Они могут иметь одно, два, три, реже четыре горла стандартных размеров. Как правило, одно из них более широкое, остальные узкие. Химические воронки (рис. 5) различной емкости используются для переливания жидкостей, для фильтрования. Угол воронки чаще всего составляет 60°. Хвостовая часть воронки имеет косой срез, необходимый для того, чтобы переливаемая жидкость стекала по стенке сосуда и не разбрызгивалась. Эксикаторы (рис. 6) используются для сохранения химических веществ в сухой атмосфере. Эксикатор представляет собой толстостенный стеклянный сосуд с широкой притертой крышкой. На дно эксикатора помещают влагопоглощающее вещество, например прокаленный хлорид кальция. Сверху кладут фарфоровую решетку, на которую ставятся чашки или бюксы с веществами. Эксикатор герметично закрывается крышкой. Герметичность обеспечивается специальной смазкой, которая наносится на пришлифованные поверхности. Крышку открывают, перемещая ее в горизонтальном направлении. Эксикатор переносят, придерживая крышку.
Капельницы (рис. 7) предназначены для работы с индикаторами. Мерная посуда применяется для измерения объемов жидкостей. Она калибрована, т.е. имеет метку, отмечающую определенный объем жидкости. Калибрование точной мерной посуды производят при температуре 20°С, что указывается на посуде. Отклонение температуры на ± 5°С не вызывает значительного изменения объема. Поэтому с мерной посудой работают при температуре, отличающейся в указанных пределах от той, при которой производилась калибровка. В случае необходимости делают соответствующий пересчет. Если мерная посуда, кроме метки, отмечающей общий объем, имеет еще метки, которые делят общий объем на части, то такая посуда называется градуированной. При работе с градуированной посудой необходимо установить цену деления. Мерные (измерительные) цилиндры, мензурки позволяют грубо измерить объем жидкостей. Для точного измерения предназначены мерные колбы, бюретки, пипетки. Для правильного измерения объема жидкости мерную посуду наполняют ею так, чтобы мениск касался метки, при этом глаз должен находиться на уровне метки. Уровень смачивающих стекло прозрачных жидкостей (воды, водных растворов, спирта) устанавливают по нижнему краю вогнутого мениска, а для непрозрачных и темноокрашенных – по верхнему краю. Мерные цилиндры и мензурки (рис. 8) используют при приготовлении растворов. Мензурки в отличие от мерных цилиндров имеют коническую форму. Емкость мерных цилиндров от 10 мл до 2 л, мензурок – от 50 до 500 мл. Измерение объемов жидкостей при помощи мензурок дает меньшую точность. Мерные колбы (рис. 9) предназначены для приготовления растворов точной концентрации. Это мерная посуда на наливание, они имеют одну метку на длинном узком горлышке. Мерные колбы бывают различной емкости – от 50 мл до 2 л. Они бывают с притертой пробкой и без нее. Пипетки и бюретки (рис. 10) – это мерная посуда, используемая при проведении химического анализа. Пипетки предназначены для отбора точных объемов анализируемых растворов. Бюретки используются для титрования (см. работу 1). Фарфоровая химическая посуда также довольно часто используется при выполнении химического эксперимента. Выпарная (выпарительная) чашка (рис. 11) – круглодонная тонкостенная емкость с носиком или без. Применяется для упаривания и выпаривания растворов. Ступка (рис. 12) – толстостенная фарфоровая посуда. Нижняя внешняя поверхность ступки плоская, а внутренняя – сферическая. Ступки используют для измельчения и растирания твердых веществ с помощью пестика.
Тигли (рис. 13) применяются для прокаливания веществ. Они бывают различной емкости от 2 мл до 100 мл. В лаборатории также применяются фарфоровые стаканы, кружки и т.д.
ЛАБОРАТОРНЫЕ РАБОТЫ Работа 1 Общие понятия Раствор – гомогенная (однородная) система, состоящая из двух или более компонентов, относительные количества которых могут изменяться в широких пределах. В истинном растворе растворенные вещества равномерно распределены в виде молекул или ионов в растворителе. Обычно растворителем считают тот компонент, который в чистом виде существует в том же агрегатном состоянии, что и полученный раствор. Например, в случае раствора соли в воде растворителем является вода. Если оба компонента до образования раствора находились в одинаковом агрегатном состоянии, например жидком (спирт и вода), то растворителем чаще всего считается компонент, находящийся в растворе в относительно большем количестве. Наибольшее практическое значение имеют жидкие растворы. Растворы электролитов – это растворы диссоциирующих на ионы солей, кислот и оснований. В них растворенные вещества присутствуют в виде молекул и ионов (слабые электролиты) или только в виде ионов (сильные электролиты). Электрическая проводимость этих растворов выше, чем растворителя. Растворы неэлектролитов – это растворы веществ, не диссоциирующих в растворителе. Они практически не проводят электрический ток. Неэлектролиты в растворе диспергированы до молекул. Раствор, находящийся при данных условиях в равновесии с растворяемым веществом, называется насыщенным раствором. В нем содержится максимально возможное количество растворенного вещества при заданной температуре. Раствор, в котором при данных условиях предел растворимости не достигнут, называется ненасыщенным. Концентрация растворенного вещества в нем меньше, чем в насыщенном растворе. Раствор, в котором при данной температуре содержится большее количество растворенного вещества, чем в насыщенном растворе, называется пересыщенным. Такие системы являются метастабильными, т.е. при отсутствии внешних воздействий могут достаточно долгое время оставаться без изменений, но при введении, например, маленького кристалла растворенного вещества весь избыток его в растворе быстро выпадает в осадок, раствор переходит в устойчивое состояние и становится насыщенным. Титриметрический анализ 3.1. Сущность титриметрического метода анализа Титриметрия (титриметрический анализ) – это количественный химический метод анализа, основанный на точном измерении объема стандартного раствора (титранта), вступающего в реакцию с определяемым веществом. Стандартным называется раствор реагента с точно известной концентрацией. Стандартный раствор добавляется из бюретки по каплям к определенному объему анализируемого раствора. Этот процесс называется титрованием.
Состояние системы, когда количество добавляемого титранта эквивалентно количеству определяемого вещества, называется точкой эквивалентности, или теоретической точкой конца титрования. Для фиксирования точки эквивалентности используют различные индикаторы или инструментальные методы. Резкое изменение окраски индикатора соответствует конечной точке титрования, которая, строго говоря, не всегда совпадает с точкой эквивалентности. Титриметрия как метод анализа имеет ряд достоинств. Во-первых, этовысокая скорость и точность анализа, а также применимость для определения различных количеств веществ. Во-вторых,этим методом в одном и том же растворе часто можно определять одновременно несколько веществ. Еще одно достоинство –возможность автоматизировать титрование. В титриметрии применяются реакции, удовлетворяющие следующим требованиям. · Реакция должна протекать быстро. · Реакция должна быть стехиометрична и протекать строго по уравнению. · Она должна протекать количественно, почти до конца, т.е. константа равновесия реакции Кр ³ 108. · Основной реакции не должны мешать побочные реакции и посторонние вещества. · Должна четко фиксироваться точка эквивалентности с помощью подходящего индикатора. Вычисления в титриметрии В основе расчетов в титриметрическом анализе лежит закон эквивалентов: вещества взаимодействуют друг с другом в эквивалентных количествах. В случае реакций между растворами (титруемого вещества и титранта) его записывают следующим образом
где С1 и С2 – молярные концентрации эквивалента реагирующих веществ (нормальные концентрации), V1 и V2 – объемы растворов. По известным значениям объемов растворов и концентрации титранта рассчитывают молярную концентрацию эквивалента для исследуемого раствора (нормальность), а далее при необходимости можно найти молярную концентрацию, содержание определяемого вещества в г/л, массу определяемого вещества в образце и т.д. При серийных анализах удобно пользоваться титром стандартного раствора по определяемому веществу. Например, T(KMnO4/Fe2+) = 0.005585 г/мл означает, что одним миллилитром стандартного раствора KMnO4 можно оттитровать 0,005585 г ионов Fe2+. Цель работы. 1. Научиться готовить растворы с заданной массовой долей растворенного вещества (процентной концентрацией) из твердого вещества и разбавлением. 2. Научиться готовить растворы заданной молярной и нормальной концентрации из твердого вещества и разбавлением. 3. Освоить метод кислотно-основного титрования.
Реактивы.
Оборудование и посуда. · Бюретки. · Стаканы на 150-200 мл. · Набор ареометров. · Весы. · Цилиндры. · Пипетки на 10, 20, 25 мл. · Колбы конические для титрования на 100 или 250 мл.
Выполнение работы. Опыт №1. Приготовление раствора заданной процентной концентрации. 1.1. Приготовление раствора из твердого вещества и воды. Цель работы. 1. Определить тепловой эффект реакции нейтрализации кислоты (основания) раствором основания (кислоты). Научиться готовить растворы заданной молярной и нормальной концентрации из твердого вещества и разбавлением. 2. Определить теплоту диссоциации слабого электролита. Реактивы. · Раствор сильной кислоты (H2SO4, HCl или HNO3 – по указанию преподавателя). · Раствор уксусной кислоты (CH3COOH). · Раствор щелочи (NaOH или KOH). Концентрации растворов кислоты и щелочи должны различаться в пять раз. Оборудование и посуда. · Прибор для определения тепловых эффектов (калориметр).. · Термометр ртутный на 50-100°С. · Мерные колбы на 250 мл и 50 мл. · Стеклянные воронки 2 шт. (для кислоты и щелочи). · Термостойкий химический стакан или термостойкая колба на 200-250 мл (для подогревания воды, необходимой для настройки термометра Бекмана). · Электрическая плитка. Выполнение работы. 1. Собирают калориметр, как показано на рис. 2.1. 2. В мерную колбу на 250 мл наливают 0,1 н раствор сильной кислоты (или щелочи). В мерную колбу на 50 мл наливают соответственно 50 мл 0,5 н раствора щелочи (или кислоты соответственно). 3. 250 мл 0,1 н раствора вносят в калориметр. Закрывают сосуд Дьюара пробкой с двумя отверстиями. Одно отверстие предназначено для термометра, второе – для добавления позже раствора с большей концентрацией. 4. Вставляют термометр в пробку калориметра. 5. Производят отсчет температуры каждые 30 сек. до установления ее равномерного хода либо до постоянного значения температуры (одинаковые значения не менее 5 раз). Значения температуры заносят в таблицу 1 (см. ниже). 6. Через стеклянную трубку в пробке калориметра быстро вливают 50 мл 0,5 н раствора, закрывают трубку пробкой и перемешивают раствор. При этом не прерывают отсчет времени и продолжают отмечать температуру каждые 30 сек. Температура при реакции нейтрализации повышается. Если по какой-либо причине отсчет температуры не был произведен в очередной раз, то при записи ставится прочерк. Повышение температуры, сопровождающее реакцию нейтрализации – главный период в опыте. Он продолжается до установления вновь равномерного хода температуры. 7. Когда наблюдается равномерный ход температуры (или устанавливается ее постоянное значение) в течение двух минут, опыт прекращают. 8. Повторяют точно так же опыт с использованием раствора слабой кислоты. Таблица 1 Изменение температуры во время опыта
Обработка результатов. 1. По данным таблицы 1 для двух опытов строят графики зависимости температуры от времени и определяют Δt. Для расчета точного изменения температуры во время реакции нейтрализации вычерчивают на миллиметровой бумаге график, откладывая на оси абсцисс время, а на оси ординат – изменения температуры за каждые полминуты. График лучше строить в следующем масштабе: 1°С соответствует 5 см, а 1 мин – 1 см. Рассчитывают теплоту (энтальпию) нейтрализации сильной и слабой кислоты по формуле (2.1). Значение постоянной калориметра К указывает преподаватель. 2. Рассчитывают теплоту (энтальпию) диссоциации слабой кислоты (или слабого основания). 3. Результаты для двух определений представляют в виде таблицы 2. Таблица 2 Результаты работы
Контрольные вопросы и задачи. 1. Что является первоисточником энергии для всех живых организмов? Во что превращается эта энергия? 2. Какие реакции называются экзотермическими и эндотермическими? Приведите примеры таких реакций в организме человека. 3. Дайте формулировку закона Гесса и поясните его на конкретном примере. 4. Что называется теплотой нейтрализации? 5. Сформулируйте закон постоянства теплот нейтрализации. К каким электролитам он применим, а для каких электролитов не соблюдается и почему? 6. Одинаковый ли тепловой эффект будет при: а) нейтрализации азотной кислоты едким натром; б) азотистой кислоты едким кали? 7. При нейтрализации 100 мл 0,2М раствора соляной кислоты эквивалентным количеством гидроксида аммония в водном растворе выделилось 1,028 кДж теплоты. Определите теплоту реакции нейтрализации соляной кислоты гидроксидом аммония и вычислите теплоту диссоциации гидроксида аммония.
Цель работы. 1. Изучить химические свойства биогенных элементов и их соединений. 2. Ознакомиться с биологической ролью элементов и применением их соединений в медицине. 3. Ознакомиться с химизмом действия некоторых лекарственных препаратов. Реактивы. · Пероксид водорода Н2О2, раствор 3%-ный. · Оксид марганца (IV) MnО2. · Карбонат калия К2СО3, раствор 0,5 моль/л. · Гидрокарбонат натрия NaHCO3, раствор 1 моль/л. · Карбонат натрия Na2CO3, раствор 1 моль/л. · Соляная кислота HCl, раствор 1 моль/л. · Соляная кислота HCl, стандартный раствор 0,05 моль/л. · Оксид магния MgO. · Карбонат кальция CaCO3. · Тетраборат натрия Na2B4O7. · Хлорид алюминия AlCl3. · Метиловый оранжевый, раствор 1%-ный. · Индикаторная бумага. · Йод. · Иодид калия KJ. · Крахмальный клейстер, раствор 0,5%-ный. · Этиловый спирт С2Н5ОН. · Серная кислота H2SO4, раствор 1 моль/л. · Перманганат калия KMnO4. · Хлорид аммония NH4Cl. · Гидроксид кальция Са(ОН)2.
Оборудование и посуда. · Пробирки. · Мерная колба на 100 мл. · Бюретка на 50 (25) мл. · Колбы конические для титрования на 100 или 250 мл. · Пипетки. · Газоотводная трубка. · Спиртовка. · Кристаллизатор. · Ступка с пестиком. · Штатив. · Лучина.
Группа IA Опыт 1. Каталитическое разложения пероксида водорода Пероксид водорода – это соединение водорода, элемента IА группы, который относится к s-семейству. Пероксид водорода является важным побочным продуктом метаболизма. Обычно в митохондриях идет восстановление О2 до Н2О: О20 + 4 Н+ + 4е = 2Н2О-2. При неполном восстановлении кислорода образуется пероксид водорода: О20 + 2Н+ + 2е = Н2О2-1. Пероксид водорода, как промежуточный продукт восстановления кислорода, очень токсичен для клетки. Токсичность связана с тем, что Н2О2 взаимодействует с липидным слоем клеточных мембран и выводит их из строя. Аэробные клетки могут защитить себя от вредного действия пероксида водорода с помощью фермента каталазы, под действием которой Н2О2 превращается в воду и кислород: 2Н2О2 Освободившийся кислород принимает участие в дальнейших процессах биологического окисления. Аналогичное разложение пероксида водорода можно осуществить в лабораторных условиях под действием MnO2 в качестве катализатора. 2Н2О2 В медицинской практике пероксид водорода применяют в основном как наружное бактерицидное средство. Действие Н2О2 основано на окислительной способности пероксида водорода и безвредности продукта его восстановления – воды. При обработке ран выделяющийся кислород играет двоякую роль. Во-первых, он оказывает противомикробное, дезодорирующее и депигментирующее действие, убивая микробные тела. Во-вторых, образует пену, способствуя переходу частиц тканевого распада во взвешенное состояние и очищению ран. В качестве фармакопейного препарата используется 3%-ный водный раствор пероксида водорода. 6%-ный раствор Н2О2 применяют для обесцвечивания волос. В виде 30%-ного раствора Н2О2 применяют при лечении бородавчатых форм красного плоского лишая и для удаления юношеских бородавок. Выполнение опыта Налейте в пробирку 1–2 мл 3%-ного раствора Н2О2, внесите на кончике шпателя немного порошка MnO2. Выделяющийся газ испытайте тлеющей лучиной. Объясните наблюдаемое явление и напишите уравнение реакции. Какую роль выполняет MnO2 в этой реакции? Группа IA и IIА Опыт №2 2.1. Взаимодействие оксидов и солей щелочных и щелочноземельных металлов с соляной кислотой Металлы IA и IIA группы относятся к s-семейству. Гидрокарбонат натрия NaHCO3 используют при различных заболеваниях, сопровождающихся повышенной кислотностью - ацидозом (диабет и др.). Механизм снижения кислотности заключается во взаимодействии NaHCO3 с кислыми продуктами. При этом образуются натриевые соли органических кислот, которые в значительной мере выводятся с мочой, и углекислый газ, покидающий организм с выдыхаемым воздухом: NaHCO3(р) + RCOOH(р) ® RCOONa(р) + Н2О(ж) + СО2(г) Используют NaHCO3 и при повышенной кислотности желудочного сока, язвенной болезни желудка и двенадцатиперстной кишки. При приеме NaHCO3 протекает реакция нейтрализации избыточной соляной кислоты: NaHCO3(р) + HCl(р) = NaCl(р) + Н2О(ж) + СО2(г) желудоч. сок Следует иметь в виду, что применение NaHCO3 вызывает ряд побочных эффектов. Выделяющийся при реакции диоксид углерода раздражает рецепторы слизистой оболочки желудка и вызывает вторичное усиление секреции, кроме того, он может способствовать перфорации стенки желудка при язвенной болезни. Слишком большая доза NaHCO3 в результате гидролиза приводит к алкалозу, что не менее вредно, чем ацидоз. Среди оксидов элементов IIА-группы в качестве лекарственного препарата применяют оксид магния MgO. Основные свойства оксида магния и его нерастворимость в воде обуславливают его применение в качестве антацидного средства при повышенной кислотности желудочного сока: MgO(тв.) + 2HCl(желудоч. сок) = MgCl2(р) + Н2О(ж) Оксид магния имеет преимущество перед гидрокарбонатом натрия, так как при взаимодействии MgO с кислотой желудочного сока не происходит выделение диоксида углерода. Поэтому при действии оксида магния не наблюдается гиперсекреции. Образующийся при реакции хлорид магния переходит в кишечник, оказывает легкий послабляющий эффект, обусловленный осмотическим действием. Антацидным и адсорбирующим действием обладает карбонат кальция СаСО3. Его назначают внутрь при повышенной кислотности желудка, так как он нейтрализует соляную кислоту: СаСО3(тв.) + 2HCl (желудоч. сок) = CaCl2(р) + Н2О(ж) + СО2(г). Выполнение опыта Испытайте отношение к раствору HCl следующих веществ NaHCO3, MgO, CaCO3. Поместите в три пробирки небольшие количества перечисленных веществ. Прилейте раствор соляной кислоты. Объясните наблюдаемые явления. Напишите уравнения реакций в молекулярной, ионной и сокращенной ионной форме. 2.2. Определение временной (гидрокарбонатной) жесткости воды Растворимые соли Са и Mg обуславливают важное свойство природной воды, называемое жесткостью. Определение жесткости воды имеет большое практическое значение и широкое применение в лабораторной практике различных производств. При стирке белья жесткая вода ухудшает качество тканей и требует повышенной затраты мыла, которое расходуется на связывание катионов Са2+ и Mg2+: 2С17Н35СОО– + Са2+ = (С17Н35СОО)2Са¯ 2С17Н35СОО– + Mg2+ = (С17Н35СОО)2Mg¯. Пена образуется лишь после полного осаждения этих катионов. Правда, некоторые синтетические моющие средства хорошо моют и в жесткой воде, так как их кальциевые и магниевые соли легко растворяются. В жесткой воде плохо развариваются овощи. Очень плохо заваривается чай, и вкус его теряется. В то же время в санитарно-гигиеническом отношении эти катионы не представляют опасности, хотя при большом содержании катионов магния Mg2+ (как в море или океане) вода горьковата на вкус и оказывает послабляющее действие на кишечник человека. Однако использование жесткой воды в качестве питьевой способствует возникновению мочекаменной и желчекаменной болезней (образованию камней). Различают жесткость временную (или устранимую) и постоянную. Временная жесткость обусловлена присутствием в воде гидрокарбонатов Ca(HCO3)2, реже Mg(HCO3)2 и иногда Fe(HCO3)2. Постоянная жесткость обусловлена присутствием других растворимых солей этих металлов (хлоридов, сульфатов и др.). При кипячении воды гидрокарбонаты разлагаются с образованием труднорастворимых соединений, выпадающих в осадок, и жесткость уменьшается. Ca(HCO3)2 ® CaCO3¯ + H2O + CO2 Ca2+ + 2HCO3- ® CaCO3¯ + H2O + CO2 2Mg(HCO3)2 ® (MgOH)2CO3¯ + H2O + 3CO2 2Mg2+ + 2HCO32- ® (MgOH)2CO3¯ + H2O + 3CO2. Сохраняющаяся после кипячения воды жесткость, называется постоянной (некарбонатной). В соответствии с ГОСТ 6055-86 по значению общей жесткости (ммоль/л) различают воду: очень мягкую <1,5, мягкую 1,5–3,0, средней жесткости 3,0–6,0, жесткую 6,0–9,0, очень жесткую > 9,0. Жесткость воды хозяйственно-питьевых водопроводов не должна превышать 7 ммоль/л. Для определения жесткости воды применяют титриметрический метод (см. лабораторную работу №1). В данном опыте методом кислотно-основного титрования (метод нейтрализации) определяется временная (гидрокарбонатная) жесткость воды. Гидрокарбонаты кальция и магния титруют соляной кислотой в присутствии индикатора. Ca(HCO3)2 + 2НCl ® CaCl2 + 2H2O +2CO2 HCO3– + Н+ ® H2O +CO2 Выполнение опыта 1. Пипеткой отбирают 100 мл анализируемой воды, переносят в коническую колбу для титрования. 2. Добавляют 3-4 капли метилового оранжевого. 3. Титруют стандартным 0,1 н раствором соляной кислоты до перехода окраски из желтой в бледно-розовую. Титрование проводят 2-3 раза, разница между параллельными результатами не должна превышать 0,1 мл. Вычисляют средний объем кислоты и рассчитывают временную жесткость воды по формуле:
где Ж(Н2О) – жесткость воды, ммоль/л С(HCl) – нормальная концентрация раствора, моль/л V(HCl) – объем кислоты, пошедшей на титрование, мл Va - объем воды, взятый на титрование, мл. Множитель 1000 учитывает перевод моль в ммоль (1 моль = 1000 ммоль). Приведите необходимые расчеты и сделайте вывод о жесткости исследуемой воды.
Группа IIIA Опыт 3. Гидролиз тетрабората натрия Бор – элемент IIIA группы, р-элемент, он относится к примесным микроэлементам. Биологическое действие бора еще недостаточно изучено (его биогенность остается под вопросом). Кристаллогидрат тетрабората натрия Na2B4O7 ∙10H2O (бура) применяют как антисептик. Фармакологическое действие препарата обусловлено гидролизом соли с образованием ортоборной кислоты: Na2B4O7 + 7H2O «4H3BO3 + 2NaOH. Высокая растворимость борной кислоты в липидах обеспечивает быстрое проникновение ее в клетки через липидные мембраны. В результате происходит свертывание белков (денатурация) цитоплазмы микроорганизмов и их гибель. Таким образом, образующиеся при гидролизе щелочь и кислота вызывают свертывание белков микробных клеток. Выполнение опыта Испытайте раствор тетрабората натрия (буры) Na2B4O7*10H2O универсальной индикаторной бумажкой. Какова реакция среды в растворе? Напишите уравнение реакции гидролиза соли в ионном виде. Опыт 4. Амфотерность гидроксида алюминия По содержанию в организме человека алюминий относится к примесным микроэлементам (10–5 %). Известно, что алюминий влияет на развитие эпителиальной и соединительной тканей, на регенерацию костной ткани, на обмен фосфора. Катион Al3+ способен замещать ионы Ca2+ и Mg2+, влияя тем самым на протекание ферментативных процессов. Избыток алюминия в организме тормозит синтез гемоглобина, так как благодаря довольно высокой способности к комплексообразованию ионы алюминия блокируют активные центры ферментов, участвующих в кроветворении. Алюминий – амфотерный металл, растворяется в растворах кислот и в щелочах. Амфотерными свойствами обладают оксид (Al2O3) и гидроксид алюминия (Al(OH)3). Соли алюминия и кислородсодержащих кислот растворимы в воде, за исключением фосфата алюминия AlPO4. Это следует учитывать при назначении препаратов алюминия, в частности гидроксида алюминия при повышенной кислотности желудка. В желудке гидроксид алюминия нейтрализует соляную кислоту Al(OH)3 + 3HCl = AlCl3 + 3H2O Al(OH)3 + 3H+ = Al3+ + 3H2O Перешедшие в раствор ионы алюминия в кишечнике переходят в малорастворимую форму – фосфат алюминия, который выводится из организма. Таким образом, в присутствии ионов алюминия уменьшается усвоение фосфора. В медицинской практике также находят применение алюмокалиевые квасцы (KAl(SO4)2∙12H2O) и жженые квасцы (KAl(SO4)2). Эти соединения используются для наружного применения для полосканий, промываний, примочек при воспалительных заболеваниях кожи и слизистых, как кровоостанавливающее средство при порезах. Фармакологическое действие солей алюминия основано на том, что ионы Al3+ образуют с белками комплексы, выпада
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-14; просмотров: 330; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.139.236.144 (0.013 с.) |

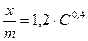 », а не так: «при выполнении лабораторной работы я ознакомился с адсорбцией уксусной кислоты».
», а не так: «при выполнении лабораторной работы я ознакомился с адсорбцией уксусной кислоты».





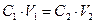 ,
, 2Н2О + О2.
2Н2О + О2. 2Н2О + О2.
2Н2О + О2.



