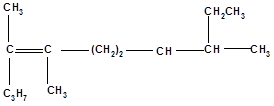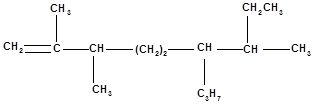Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Сполуки, що містять азот, сірку, фосфор та кремнійСодержание книги
Поиск на нашем сайте
Класифікація. Номенклатура. Нітросполуки. Методи добування: нітрування аліфатичних та ароматичних сполук, нуклеофільне заміщення галогена на нітрогрупу в галогенпохідних. Будова нітрогрупи, її електроноакцепторний характер. Кислотність та таутомерія аліфатичних нітросполук (ацинітросполуки), реакції з лугами, азотистою кислотою, карбонільними сполуками, галогеналкілами, галогенами, гідроліз в кислих розчинах. Відновлення нітросполук Проміжні продукти відновлення. Застосування нітросполук (тротил та ін.). Аміни. Класифікація. Номенклатура. Ізомерія. Методи добування первинних, вторинних та третинних амінів. Основність амінів. Залежність основності амінів від кількості та природи замісників для аліфатичних та ароматичних сполук. Реакції амінів як нуклеофільних реагентів. Взаємодія азотистої кислоти з первинними, вторинними і третинними аліфатичними та ароматичними амінами. Ізонітрильна реакція на первинні аміни. Утворення N-оксидів. Заміщення ароматичних амінів в ядро: галогенування, сульфування, нітрування. Захист аміногрупи у хімічних реакціях. Активуючий вплив аміногрупи на ядро. Застосування амінів. Поняття про діаміни. Гексаметилендіамін. Полімери типу “нейлон”. Ароматичні діазосполуки. Діазотування, умови реакції, механізм. Будова ароматичних діазосполук. Реакції діазосполук з виділенням азоту. Синтез елементорганічних сполук через діазосполуки (реакція Несмєянова). Реакція арилювання аренів та ненасичених сполук. Реакції ароматичних діазосполук без виділення азоту: відновлення до арилгідразинів, азосполучення. Умови проведення реакції азосполучення з фенолами та амінами. Азобарвники. Індикаторні властивості азобарвників (метиловий жовтогарячий). Органічні сполуки сірки, фосфору та кремнію. Класифікація. Тіоли: аліфатичні та ароматичні (меркаптани). Будова. Методи добування. Властивості: утворення солей, тіоацеталей та тіокеталей, дисульфідів, сульфокислот, приєднання до алкенів. Реакції алкілування та ацилювання. Порівняльна характеристика їх властивостей із властивостями спиртів та фенолів. Сульфіди (тіоетери), будова, добування, властивості: утворення солей сульфонію, окиснення до сульфоксидів та сульфонів. Сульфони та сульфоксиди. Будова, добування, властивості. Диметилсульфоксидякрозчинник. Поняття про тіокарбонільні сполуки, порівняння з альдегідами та кетонами. Сульфонові кислоти. Методи добування алкіл- та арилсульфокислот. Зворотність реакції сульфування аренів. Властивості сульфонових кислот. Реакції заміщення сульфогрупи на водень, гідроксильну та нітрильну групи, реакції електрофільного заміщення водню в ароматичних сульфокислотах. Естери сульфокислот, як алкилюючі реагенти. Застосування солей сульфокислот як миючих засобів. Сульфамідні препарати. Фосфорорганічні сполуки. Класифікація: фосфін та алкилфосфіни, фосфініста, фосфоніста, фосфонова кислота, фосфіноксид. Методи добування, взаємні переходи, реакція Арбузова. Фосфорорганічні інсектициди та бойові отруйні речовини. Кремнійорганічні сполуки, їх класифікація, номенклатура. Методи добування, властивості, синтез полімерів.
Гетерофункціональні похідні вуглеводнів Та природні сполуки
Галогенозаміщені кислоти. Класифікація. Добування. Фізичні та хімічні властивості. Залежність хімічних властивостей від взаємного розміщення галогену та карбоксильної групи. Хлороцтові кислоти. Гідроксікислоти. Класифікація. Номенклатура. Методи одержання. Загальні хімічні властивості. Особливості аліфатичних a-, b-, та g- оксикислот, молочна, винна, яблучна та лимонна кислоти. Ароматичні гідроксикислоти, синтез аспірину. Оксокислоти. Класифікація, ізомерія, номенклатура та будова. Гліоксилова, піровиноградна та ацетооцтова кислоти. Ацетооцтовий естер, його кето-енольна таутомерія та синтези на його основі. Амінокислоти. Класифікація. Ізомерія. Номенклатура. Добування. Фізичні та хімічні властивості амінокислот. Амфотерність та цвітер-йони. Лактами. Білки. Пептидний зв‘язок. Встановлення будови та синтез поліпептидів. Ферменти. Вуглеводи. Класифікація. Конфігурація моносахаридів. Глюкоза, фруктоза та їх хімічні властивості. Полісахариди (крохмаль, целюлоза). Етери та естери целюлози. Віскоза.
Гетероциклічні сполуки
Загальна характеристика гетероциклів.Класифікація. Номенклатура. Ароматичні гетероцикли, природа їх ароматичності. Порівняльна характеристика ароматичності бензолу та ароматичних гетероциклів. Роль гетероциклічних сполук в природі та в промисловому органічному синтезі. П’ятичленні гетероцикли з одним гетероатомом. Хімічні властивості. Електрофільне заміщення: нітрування, сульфування, галогенування, ацилування, азосполучення, формілування, меркурування. Специфічні властивості: гідрування, розщеплення, циклоприєднання до фурану, кислотність піролу. Порівняльна характеристика гетероциклів. Фурфурол. Вплив природи гетероатома на ароматичність, ненасиченість та ацидофобність П’ятичленні гетероцикли з одним гетероатомом, що конденсовані з бензольним ядром. Індол, тіонафтен, кумарон, карбазол. Синтез, властивості. Барвники на основі індиго. Полівінілкарбазол. П‘ятичленні гетероцикли з декількома гетероатомами. Піразол, імідазол, тіазол. Методи добування. Кислотно-основні властивості. Реакції електрофільного заміщення. Шестичленні гетероцикли. Піридин. Будова. Синтез піридину. Нуклеофільне заміщення: амінування, гідроксилювання (реакція Чічібабіна), алкілування. Електрофільне заміщення: нітрування, сульфування, галогенування. Радикальне заміщення з солями діазонію. Основність піридину: реакції з кислотами, алкилгалогенидами, ацилгалогенидами, утворення комплексів з оксидом сірки (VI), бромом. Піперидин. Похідні піридину та їх властивості. Поняття про алкалоїди. Шестичленні гетероцикли з одним гетероатомом, що конденсовані з бензольним ядром. Хінолін. Будова. Ароматичність. Порівняльна характеристика хіноліну, піридину, бензолу та нафталіну. Реакції електрофільного заміщення в хіноліні: нітрування, сульфування. Нуклеофільне заміщення: амінування, гідроксилювання, алкілування. Ізохінолін. Акридин. Одержання, властивості. Шестичленні гетероцикли з декількома гетероатомами. Діазини: піразин, піримідин, піридазин. Будова. Порівняльна реакційна здатність. Методи одержання. Нуклеофільне заміщення. Електрофільне заміщення в похідних діазинів. Основні властивості в порівнянні з піридином. Реакції окиснення-відновлення. Поняття про нуклеїнові кислоти.
ТАБЛИЦЯ ВАРІАНТІВ КОНТРОЛЬНИХ ЗАВДАНЬ
Продовження таблиці
Продовження таблиці
Закінчення таблиці
Завдання для контрольної роботи
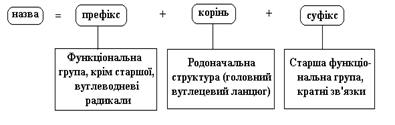
Література: [1с.190-200]. риклад 1: Назвати сполуку за систематичною (замісниковою) номенклатурою IUPAC.
Старша функціональна група
Замісник Замісник
Родоначальна структура
Перед усім треба визначити старшу групу. Розподілення функціональних груп за старшинством наведено в [1] на стор. 196. В нашому випадку – це ОН-група. У назві органічної речовини старша функціональна група позначається у суфіксі, а усі інші – у префіксі. Далі визначаємо родоначальну структуру, в аліфатичних сполуках це головний вуглецевий ланцюг. За головний вуглецевий ланцюг обирається той, котрий містить максимальне число функціональних груп, кратних зв’язків, атомів вуглецю, замісників. Назва родоначальної структури утворюється від назви нормального алкану з відповідною кількістю атомів карбону. В нашому випадку – це алкан, що містить 7 атомів карбону, – гептан. Замісником називають будь який атом, або групу атомів, котрі не входять до родоначальної структури. Поняття “замісник” включає в себе функціональну групу і радикал. Радикал являє собою залишок молекули вуглеводню, що утворюється в результаті видалення одного або декількох атомів водню. Вільну валентність у радикалах позначають рискою. За кількістю вільних валентностей розрізняють одно-, дво-, і тривалентні радикали:
СН3─СН2─ СН3─СН= ─СН2─СН2─ СН3─С≡ Одновалентний Двовалентні Тривалентний радикал радикали радикал
У залежності від того, при якому атомі вуглецю – первинному, вторинному, чи третинному – знаходиться вільна валентність, розрізняють первинні, вторинні та третинні радикали. Первинним називається атом вуглецю, який безпосередньо зв’язаний лише з одним атомом вуглецю, вторинним – з двома, третинним – з трьома.
СН3 │ СН3─СН2─СН2─СН2─ СН3─СН2─СН─СН3 СН3─С─СН3 │ │ первинний радикал вторинний радикал третинний радикал
Структурні формули і назви деяких вуглеводневих радикалів наведені в таблиці:
Визначивши родоначальну структуру, нумерують її атоми таким чином, щоб старша група дістала, по можливості менший номер. Якщо сполука не має старшої групи, або старша група міститься біля середнього атома родоначальної структури (як в нашому прикладі), нумерацію починають з того боку, до якого ближче кратні зв'язки, а в їх відсутності – замісники. Нарешті складають назву сполуки в цілому, дотримуючись такої послідовності: спочатку вказують в алфавітному порядку функціональні групи, окрім старшої, та вуглецеві радикали (префікс), потім – назву родоначальної структури (корінь), у кінці – кратні зв'язки і старшу функціональну групу (суфікс).
Подвійний зв’язок у назві позначається суфіксом –ен, потрійний - -ін. Положення замісників і кратних зв’язків вказують цифрами, які розташовують перед префіксом і після суфіксу. При наявності у молекули однакових замісників, або кратних зв’язків для їх означення використовують множні префікси ди- (два), три- (три), тетра- (чотири), пента- (п’ять) і т.і. Таким чином, для нашого приклада назва сполуки за систематичною номенклатурою IUPAC: 3-хлор-3,4-диметилгептен-1-ол-4
Приклад 2. Напишіть структурну формулу сполуки дибутилтретбутилметилметан і дайте їй назву за систематичною номенклатурою IUPAC. Розв’язання. В цьому прикладі назва сполуки наведена за раціональною номенклатурою. За раціональною номенклатурою усі речовини у певному гомологічному ряді розглядаються як похідні найпростішого представника даного ряду, зокрема в алканів – метану, в алкенів – етилену і т.п. Назва найпростішого представника гомологічного ряду зазначається в кінці назви сполуки. Таким чином, дибутилтретбутилметилметан слід розглядати як алкан, що утворився в результаті заміщення всіх 4-х атомів водню в молекулі метану на вуглеводневі радикали, а саме на два радикали бутил, один - третбутил, один - метил. Виходячи з цього структурна формула речовини матиме вигляд:
Радикали
Центральний атом Радикали
Користуючись вказівками, що викладені в попередньому прикладі, визначаємо назву сполуки за систематичною (замісниковою) номенклатурою:
Замісник (радикал Третбутил)
Замісник (радикал метил) родоначальна структура
Таким чином сполука має назву 5-метил-5- трет -бутилнонан. Приклад 3. За назвою напишіть структурну формулу речовини: 4-бром-3,3-диметилпентен-1-ол-2. Розв’язання. Як це видно з написання, назва запропонована за систематичною (замісниковою) номенклатурою, тому розділимо назву за частинами слова:
Написання формули починаємо з визначення родоначальної структури. Корінь слова “пент” тобто походить від назви алкану “пентан”, що містить 5 атомів карбону. Таким чином, записуємо ланцюг з п’яти атомів карбону: 1 2 3 4 5 С – С – С – С – С Далі визначаємо положення старшої функціональної групи і кратного зв’язка. В суфіксі назви зазначено: “-ен-1-ол-2”, тобто подвійний зв’язок розташований після першого атому карбону (-ен-1), а старша функціональна група –ОН – біля другого атому карбону (-ол-2): 1 2 3 4 5 С = С – С – С – С │ ОН Положення замісників зазначено в префіксі. Це один атом брому біля четвертого атому карбону (4-бром) і два радикали СН3- біля третього атому карбону (3,3-диметил): Н3С Br 1 2 3 │ │4 5 С = С – С – С – С │ │ ОН СН3 На останньому етапі записуємо атоми водню, що утворюють зв’язки з головним вуглецевим ланцюгом. Враховуючи, що карбон в органічних сполуках утворює чотири зв’язки, отримуємо повну структурну формулу: Н СН3 Br Н │ │ │ │ Н – С = С – С – С – С – Н, │ │ │ │ ОН СН3 Н Н
або скорочену структурну формулу: СН3 Br │ │ СН2 = С – С – СН – СН3 │ │ ОН СН3 Приклад 4. Назвіть за раціональною номенклатурою речовину: CH3-CH-CH3 | СН3--С-СН2-СН3 | C3H7 Розв’язання. За раціональною номенклатурою усі речовини у певному гомологічному ряді розглядаються як похідні найпростішого представника даного ряду. Як ми бачимо з формули, речовина належить до класу насичених вуглеводнів – алканів. Тобто її можна розглядати як похідну метану. За центральний атом вибираємо той, який має найбільше розгалуження, решту розглядаємо як радикали.
Радикали
Центральний атом Радикали
Таким чином, назва сполуки за раціональною номенклатурою: етилметилпропілізопропілметан
Завдання для самостійного розв’язування
1. а) Назвіть за систематичною номенклатурою речовину: б) За назвою напишіть структурну формулу речовини:3,3-диметилбутанол-2.
2. а) Напишіть структурну формулу сполуки т етраметилметан і назвіть її за номенклатурою IUPAC б) Назвіть за систематичною і раціональною номенклатурою речовину: CH3-CH-CH3 | С2Н5-С-СН3 | CH3 3. а) Напишіть структурну формулу сполуки етилметилпропіл- метан і назвіть її за номенклатурою IUPAC. б) За структурною формулою назвіть сполуку за раціональною і систематичною номенклатурою: CH3-CH-CH3 | СН3-С-СН2-СН3 | C3H7 4.
а) За структурною формулою назвіть сполуку за номенклатурою IUPAC: б) За назвою напишіть структурну формулу речовини:2-метилбутен-3-ол-2.
5. а) За структурною формулою назвіть сполуку за міжнародною і раціональною номенклатурою:
СН3-СН-СН2 - СН-СН2-СН-СН3 | | | CH3 CH3-CH-CH3 CH3 б) Напишіть структурну формулу сполуки дибутилтр-етбутилметан і назвіть її за номенклатурою IUPAC.
6.
а) За структурною формулою назвіть сполуку за номенклатурою IUPAC: б) Напишіть структурну формулу сполуки бутилізобутил-метан і назвіть її за номенклатурою IUPAC
7. а) Назвіть за систематичною та раціональною номенклатурою: CH3 | СН3-СН-СН2 -СН-СН2-СН-СН3 | | | CH3 CH3 CH3 б) Напишіть структурну формулу сполуки тетратретбутилметан і назвіть її за номенклатурою IUPAC.
8. а) Назвіть за систематичною та раціональною номенклатурою: CH3-CH-CH3 | СН3-СН2-СН2-СН2-С-СН2-СН2-СН2-СН3 | CH3-CH-CH3 б) Напишіть структурну формулу сполуки діізопропілметан і назвіть її за номенклатурою IUPAC.
9. а) Назвіть за систематичною номенклатурою:
б) Напишіть структурну формулу сполуки діізопропілметан і назвіть її за номенклатурою IUPAC.
10. а) Назвіть за міжнародною та раціональною номенклатурою: CH3 | CH3-C-CH3 | СН3-СН2-СН2-СН2-С-СН2-СН2-СН3 | CH3-CH-CH3 б) Напишіть структурну формулу сполуки діізопропілметан і назвіть її за номенклатурою IUPAC.
11. а) Назвіть за міжнародною та раціональною номенклатурою: CH3 | СН3-СН-СН2-СН-СН--СН3 | | CH3 CH3-C-CH3 | CH3 б) Напишіть структурну формулу сполуки метилтрипропіл-метан і назвіть її за номенклатурою IUPAC.
12. а) Назвіть за міжнародною та раціональною номенклатурою: CH3 | СН3-СН-СН2-С-СН2-СН--СН3 | | | СH3 CH3-C-CH3 CH3 | CH3 б) Напишіть структурну формулу сполуки метилпропіл-диетилметан і назвіть її за номенклатурою IUPAC.
13. а) Назвіть за міжнародною та раціональною номенклатурою: CH3 | СН3-СН-СН2-С-СН2-СН2--СН3 | | СH3 CH3-C- СН2--СН3 | CH3 б) Напишіть структурну формулу сполуки 2-етил-5-ізопропіл-1,2,3,4-тетрахлороктин-7.
14. а) Назвіть за міжнародною та раціональною номенклатурою: C2H5 | СН3-СН2-СН2-СН2-С-СН2-СН2-СН3 | CH3-C-CH3 | CH3 б) Напишіть структурну формулу сполуки, 2-етил-5-ізобутил-3-хлороктен-7-ол-2. 15. а) Назвіть за міжнародною та раціональною номенклатурою: C4H9 | СН3-СН-СН2-СН2-С-СН2-СН-СН3 | | | CH2 CH3-C-CH3 CH3 | | CH3 Н б) Напишіть структурну формулу сполуки ,3-бром -5-етил-2-метилнонен-8-ол-4. 16. а) Назвіть за міжнародною номенклатурою: Cl CH3-CН-CH3 C4H9 | | | СН3-СН-СН-СН2-С-СН-СН-СН3 | | | ОН Cl CH3 б) Напишіть структурну формулу сполуки ,3-бром-2,5-диметилоктен-7-ол-4.
17. а) Назвіть за міжнародною номенклатурою: CH3 CH3 Cl | | | СН3-СН-СН-СН2-С-СН-СН-СН3 | | | C4H9 Cl CH3 б) Напишіть структурну формулу сполуки ,2-бром-4-ізобутил-5-метилнонен-8-ол-3.
18. а) Назвіть за міжнародною номенклатурою: Cl Cl Cl | | | СН3-СН-СН- С-СН-СН-СН3 | | | Cl Cl CH3 б) Напишіть структурну формулу сполуки ,3-бром -4-ізобутил-2-метилнонен-8-ол-3.
19. а) Назвіть за міжнародною номенклатурою: CH3 | СН3 -СН2 -С-С ≡ СН | CH3 б) Напишіть структурну формулу сполуки метилетилметан і назвіть її за систематичною номенклатурою.
20. а) Назвіть за міжнародною номенклатурою: CH3 | СН3 - СН2 - СН2 -СН2 -С-С ≡ СН | CH3 б) Напишіть структурну формулу сполуки тетраетилметан і назвіть її за систематичною номенклатурою.
Алкани. Література: [1с.200-228].
Приклад. За допомогою реакції Вюрца одержіть: а) 3,6-диметилоктан б) 3,3-диметилоктан Розв’язання. Слід пам’ятати, що при взаємодії двох галогеналканів різної будови утворюється 3 різних за будовою алкани, внаслідок взаємодії двох молекул кожного галогеналкану з металічним натрієм: Оскільки суміш алканів важко розділити, зазначену реакцію доцільно використовувати для одержання симетричних алканів, тобто таких, молекулу яких можна розірвати на два однойменні радикали. В нашому прикладі – це варіант (а) - 3,6-диметилоктан. Запишемо структурну формулу цієї сполуки: CH3 CH3 | | СН3 - СН2 - СН -СН2 - СН2 - СН -СН2 - СН3 1 2 3 4 5 6 7 8 Як видно із структурної формули, ця молекула симетрична і її умовно можна розірватиміж 4-м і 5-м вуглецевими атомами на два однакових радикали. Тому для синтезу сполуки доцільно використати галоїдний алкіл з вуглецевим скелетом, що відповідає будові такого радикалу:
У разі, коли за реакцією Вюрца необхідно синтезувати алкан несиметричної будови (в нашому прикладі – це варіант (б) - 3,3-диметилоктан), використовують галогенпохідні двох різних алканів. При цьому треба враховувати наступі моменти: · в результаті реакції утвориться три різних за будовою алкани; · для того щоб краще відділити основний продукт від домішок бажано, щоб всі ці алкани суттєво відрізнялись за фізико-хімічними властивостями (максимально відрізнялися за кількістю вуглецевих атомів головного вуглецевого скелета); · вторинні і третинні галогеналкани важко і з невеликим виходом вступають в реакцію Вюрца, тому останню здійснюють, як правило, з первинними галогенпохідними алканів. Запишемо структурну формулу сполуки 3,3-диметилоктан: CH3 | СН3 - СН2 - С -СН2 - СН2 - СН2 -СН2 - СН3 1 2 | 3 4 5 6 7 8 CH3 Для того, щоб в результаті реакції Вюрца отримати продукти, що суттєво відрізняються за фізико-хімічними властивостями, необхідно використати галогенпохідні, що максимально відрізняються один від одного за кількістю вуглецевих атомів. Якщо, наприклад, розірвати молекулу між 7-им і 8-им атомами, утворяться два радикали: CH3 | СН3 - СН2 - С -СН2 - СН2 - СН2 -СН2 -та -СН3 | CH3 Реакція Вюрца, що відбувається між галогенпохідними, будова яких відповідає будові таких радикалів буде проходити за наступними схемами:
1)
2)
3)
За першою схемою утворюється основний продукт(3,3-диметилоктан) за другою і третьою – побічні продукти (3,3,12,12-тетраметилгексадекан і етан, відповідно).
Завдання для самостійного розв’язування
Визначте найраціональніші шляхи синтезу наведених далі алканів із галогенпохідних за реакцією Вюрца. Напишіть схеми реакцій. Назвіть за систематичною номенклатурою вихідні й побічні продукти. що утворюються при синтезі.
21. 3-етил-4-метилгексан; 3,3-диметилпентан. 22. 4-етил-2,4- диметилоктан; 3-етил-3-метилпентан. 23. 2,5-диметилгексан; 3,3-діетил-2-метилгептан. 24. 2-метилгексан; 2,4-диметилпентан. 25. 2,2,3-триметилбутан; 2,2-диметилбутан. 26. 3-етил-2,3-диметилгексан; 2,2,4-триметилпентан. 27. 3,3-діетил-2,5-диметилгексан; 3-етилгексан. 28. 2,6-диметилоктан; 3-метил-4-етилгептан. 29. 2,3-диметилпентан; 3-метил-4,4-діетилгептан. 30. 3,8-діетидекан; 4-етил-2,4-диметилоктан. 31. 3,4-диметилгексан;3,5-діетил-2,4-диметилгептан. 32. 2,3,4-триметилдекан; 3-етил-2-метилпентан. 33. 3-етил-3-метилгексан; 3,3-диметилгексан. 34. 2,5-диметилгексан; 3,3,4-триметилоктан. 35. 3-етилгексан; 3-етил-2-метилпентан. 36. 2,4-диметилгексан; 2-метилпентан. 37. 3-етил-3,5-диметилгептан; октан. 38. 4-етил-2,4-диметилгексан; 3,4-діетилгексан. 39. 3,6-діетил-3,6-диметилоктан; 4-етил-2-метилгексан. 40. 2,2,5,5-тетраметилгексан; 3-метил-3-етилгептан.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-07-14; просмотров: 492; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.113 (0.01 с.) |


 Розв’язання. При утворенні назв за замісниковою номенклатурою органічні сполуки розглядають як похідні найпростіших вуглеводнів, у молекулах яких один або декілька атомів водню заміщені на інші атоми або групи атомів, що називаються замісниками.
Розв’язання. При утворенні назв за замісниковою номенклатурою органічні сполуки розглядають як похідні найпростіших вуглеводнів, у молекулах яких один або декілька атомів водню заміщені на інші атоми або групи атомів, що називаються замісниками.