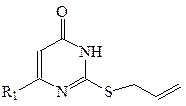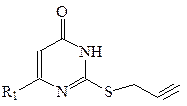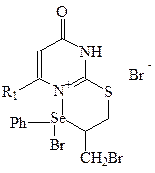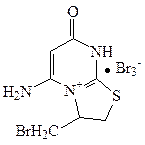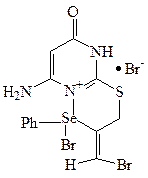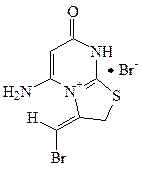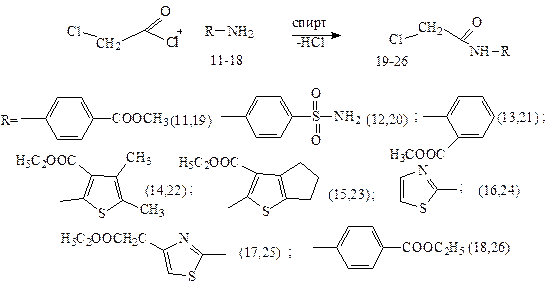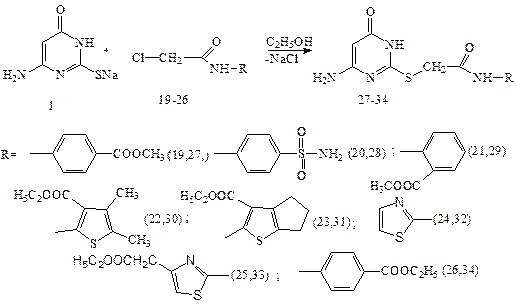Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методики проведених синтезів та фізико-хімічні характеристики отриманих сполукСодержание книги
Поиск на нашем сайте
Фенілселентрибромід одержаний по методиці з дифенілдиселеніду та брому. Вихід 71 %. Ттопл 107–108 ˚С (хлороформ). (105-106 ˚С [146]). Спектр ЯМР 1Н в СDCl3 (δ, м.ч.): 7.41 м (3Н, 3СН); 7.86 м (2H, 2СН). Спектр ЯМР 13С (СDCl3, δ, м.ч.): 129.98, 131.05, 133.12, 133.63, 134.25, 135.19. Спектр ЯМР 77Se в СDCl3 (δ, м.ч.): 870.38. Знайдено, %: C 18.03; H 1.09; Br 60.42; Se 19.78. C6H5SeBr3. Вирахувано, %: C 18.18; H 1.26; Br 60.61; Se 19.95.
4-Аміно-2-(2-пропенілтіо)-1,6-дигідропіримідин-6-он 4
До суспензії 0.030 моль 4-аміно-2-меркапто-1,6-дигідропіримідин-6-ону в 20 мл етилового спирту додають розчин 0.035 моль натрію в 15 мл етилового спирту. Реакційну суміш інтенсивно перемішують при кипінні 15 хвилин, а потім колбу охолоджують. До утвореної білої маси додають 3.8 мл (0.045 моль) алілу бромистого в 30 мл спирту і нагрівають при 60 ˚С, протягом 20 хвилин. Гарячий розчин фільтрують і залишають для кристалізації. Білий осад відфільтровують, промивають етиловим спиртом та водою. Продукт сушать на повітрі. Вихід 72 %. Ттопл 198–200 ˚С (етанол). Спектр ЯМР 1Н в ДМСО– d6 (δ, м.ч., J, Гц): 3.75 д (2Н, СН2, 7.2); 4.94 с (1Н, СН); 5.10 д (1H, СН, 9.0); 5.31 д (1H, СН, 17.1); 5.92 м (1Н, СН); 6.47 с (2H, NH2); 11.45 роз. с (1H, NН). Знайдено, %: C 45.87; H 4.90; N 22.91; S 17.44. C7H9N3OS. Вирахувано, %: C 45.90; H 4.92; N 22.95; S 17.49.
4-Аміно-2-(2-пропінілтіо)-1,6-дигідропіримідин-6-он 5
До суспензії 0.030 моль 4-аміно-2-меркапто-1,6-дигідропіримідин-6-ону в 25 мл етилового спирту додають розчин 0.035 моль натрію в 25 мл етилового спирту. Реакційну суміш охолоджують при інтенсивному перемішуванні. До утвореної білої маси додають 4 мл (0.050 моль) пропаргілу бромистого в 15 мл спирту. Реакційну суміш, обережно нагрівають (60 ˚С) протягом 40 хвилин і гарячою фільтрують. Після охолодження, утворений осад відфільтровують, промивають етиловим спиртом, водою та діетиловим етером. Продукт сушать на повітрі. Вихід 65 %. Ттопл 210–211 ˚С (етанол). Спектр ЯМР 1Н в ДМСО– d6 (δ, м.ч.): 3.14 с (1Н, СН); 3.92 д (2Н, СН2); 5.05 с (1H, СН); 6.54 с (2H, NН2); 11.39 роз. с (1H, NН). Знайдено, %: C 46.36; H 3.83; N 23.18; S 17.64. C7H7N3OS. Вирахувано, %: C 46.41; H 3.87; N 23.20; S 17.68.
6-Аміно-3-бромометил-4-бромо-8-оксо-4-феніл-2Н,3Н,8Н-піримідо[2,1- b ] [1,4,3]тіаселеназин-4 6.
До розчину 0.015 моль сполуки 4 в 15 мл безводного хлороформу або оцтової кислоти, при перемішуванні, на протязі 1 години, додають розчин 0.015 моль фенілселенійтригалогеніду в 20 мл хлоро- форму або оцтової кислоти. Додавання проводять при температурі +10 ˚С при кімнатній температурі. Перемішують реакційну суміш 3 години, а потім залишають на 20 годин. Утворений темно-жовтий осад сполуки 7 відфільтровують, промивають діетиловим етером і сушать в ексикаторі протягом 2 діб. Вихід 83%. Ттопл. 137-139 °С. Спектр ЯМР 1Н в СDCl–D6 (δ, м.ч.) 3.40, 3.51 2д (2Н, СН2); 3.94, 4.03 2д (2Н, СН2); 5.67 м (1Н, СН); 7.20 м (2Н, 2СН); 7.40 м (3Н, 3СН); 7.89 м (1Н, СН); 8.39 м (2Н, NH2). ІЧ спектр (см-1): 1720 c (C=O), 720 c (C-Se). Розраховано, %:N 8.43. C13H13Br2N3OSSe Знайдено, % N 8.40.
6-Аміно-3-[(E)-1-бромомети-ліден]-4-бромо-8-оксо-4-феніл-2Н,3Н,8Н-піримідо [2,1- b ][1,4,3]тіаселеназин-4 7
Вихід 72%. Ттопл. 161-162 °С. Спектр ЯМР 1Н в СDCl–D6 (δ, м.ч.) 4.19 с (2Н, СН2); 4.42 с (1Н, СН); 6.70 роз. с (2Н, NH2); 6.94 с (1Н, =СНBr); 7.37 м (3Н, 3СН); 7.51 м (2Н, 2СН). ІЧ спектр (см-1): 1720 c (C=O), 728 c (C-Se). Розраховано, %:N 8.47. C13H11Br2N3OSSe Знайдено, % N 8.44.
6-Аміно-3-[(E)-1-бромометиліден]-4-бромо-8-оксо-4-феніл-2Н,3Н,8Н-піримідо[2,1- b ][1,4,3]тіаселеназин-4 8
До розчину 0.015 моль сполуки 6 в 15 мл оцтової кислоти, при перемішуванні, на протязі 1 години, добавляють розчин 0.015 моль фенілселенійтригалогеніду в 20 мл оцтової кислоти. Додавання проводять при температурі +10 ˚С. Перемішують реакційну суміш 3 години, а потім залишають на 20 годин. До розчину додають 35 мл діетилового етеру і утворений темно-жовтий осад відфільтровують, промивають діетиловим етером і сушать в ексикаторі над фосфорним ангідридом протягом 2 діб. Вихід 71 %. Ттопл 160-163 ˚С (етанол). Спектр ЯМР 1Н в ДМСО– d6 (δ, м.ч., J, Гц): 4.19 с (2Н, СН2); 4.42 с (1Н, СН); 6.70 роз. с (2Н, NH2); 6.94 с (1Н, =СНBr); 7.37 м (3Н, 3СН); 7.51 м (2Н, 2СН). ІЧ спектр (см-1): 1720 c (C=O), 728 c (C-Se). Розраховано, %:N 8.47. C13H11Br2N3OSSe Знайдено, % N 8.44.
5-Аміно-3-[(E)-1-бромометиліден]-2, 3-дигідро-7Н-[1,3]тіазоло[3,2- а ] піримідин-4-іум бромід 10
В 40 мл ацетону розчиняють 0.010 моль сполуки 8. Розчин перемішують 30 хвилин, при температурі 18-20 ˚С. При цьому відбувається знебарвлення ацетонового розчину, випадає білий осад. Осад відфільтровують, промивають ацетоном та діетиловим етером. Продукт 10 сушать на повітрі протягом 2 днів. Вихід 76%. Ттопл. 192-195 °С. Спектр ЯМР 1Н в ДМСО–D6 (δ, м.ч.) 4.42 с (2Н, SCH2); 6.78 м (2Н, NH2); 7.13 с (1Н, СН); 12.35 м (1H, NH). ІЧ спектр (см-1): 1720 (C=O). Розраховано, %:N 10.00. C8H10Br4N2OS Знайдено, % N 9.58. Загальна методика одержання продуктів 19-26
В 20 мл пропанону розчиняємо (0,05 моль) відповідного аміну. До охолодженого (0-5˚С) розчину протягом 30 хвилин прикапуємо (0,05 моль) хлорангідриду хлороцтової кислоти. Утворену суспензію перемішуємо протягом 2 годин. Фільтруємо, промиваємо етанолом та діетиловим етером. Сушимо на повітрі. Далі використовуємо продукт (24-34) без додаткової очистки.
N 1-[4-піримідосульфамідо]-2-хлороацетамід 20 Вихід 65 %. Ттопл. 184-187 °С. Спектр ЯМР 1Н в ДМСО–D6 (δ, м.ч.) 3.78 д (6H, 2ОCH3); 4.31 с (2H, CH2); 5.96 с (1H, CH); 7.81 д (2H, 2СH); 7.92 д (2H, 2CH); 10.74 с (1H, NH); 11.58 м (1Н, NH). Розраховано, %:N 14.48. C14H15ClN4O5S Знайдено, % N 14.41.
Загальна методика одержання продуктів 27-34
До (0.030 моль) натрієвої солі 1 розчиненої в 45 мл етилового спирту додають (0.045 моль) відповідного реагенту 19-26 у 30 мл гарячого етилового спирту і реакційну суміш нагрівають (60+80˚С) протягом 30 хвилин. При цьому спостерігається утворення осаду NaCl. Гарячий розчин фільтрують і залишають для кристалізації. Білий осад, що випав, відфільтровують, промивають водою, етиловим спиртом. Сушать в сушильній шафі протягом 6 годин при 60 ˚С.
N 1-(4-Сульфамідофеніл)-2-(4-аміно-6-oксo-1,6-дигідро-2-піримідин сульфо) ацетамід 28 Вихід 71 %. Ттопл. 193-196 °С. Спектр ЯМР 1Н в ДМСО–D6 (δ, м.ч.) 3.99 с (2H, SCH2); 5.05 с (1H, CH); 6.50 с (2H, NH2); 7.24 с (2H, NH2);.7.75 м (4H, 4CH); 10.45 с (1H, NH); 11.49 м (1Н, NH). Розраховано, %:N 19.70. C12H13N5O4S2 Знайдено, % N 19.59. N 1-(1,3-Тіазол-2-іл)-2-(4-аміно-6-oксo-1,6-дигідро-2-піримідинсульфо) ацетамід 32 Вихід 71 %. Ттопл. 179-183 °С. Спектр ЯМР 1Н в ДМСО–D6 (δ, м.ч.) 4.10 с (2H, SCH2); 5.04 с (1H, CH); 6.46 с (2H, NH2); 7.23 д (2H, 2СH);.7.48 д (2H, 2CH); 12.08 м (2Н, 2NH). Розраховано, %:N 24.71. C9H9N5O2S2 Знайдено, % N 24.56.
|
||
|
Последнее изменение этой страницы: 2016-06-23; просмотров: 306; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.217.95 (0.006 с.) |