Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кинетика процесса конвективной сушки.
Процесс конвективной сушки характеризуется изменением во времени основных параметров влажного твердого материала и влажного воздуха. Закономерности изменения этих параметров во времени называются кинетикой процесса конвективной сушки. Концентрация влаги в твердом материале больше равновесной, влага, испаряясь, перемещается из твердой фазы в газовую. В начальный момент времени влагосодержание материала постоянно во всем объеме, а в дальнейшем, вследствие испарения, влагосодержание материала у поверхности понижается, то есть в теле возникает градиент влагосодержания. Под их действием влага перемещается от центра тела к поверхности, испаряется в виде пара диффундирует в ядро газовой фазы. Скорость сушки Вид кривой сушки для каждого твердого материала индивидуален (рис. 5.67). АВ – соответствует периоду прогрева влажного материала. ВС – период испарения поверхностной влаги. CD – период падающей скорости.
В период прогрева подводимая к телу теплота расходуется на прогрев материала от начальной температуры В периоде постоянной скорости сушки влажность материала интенсивно уменьшается по линейному закону, вся теплота идет на интенсивное поверхностное испарение влаги, и температура материала остается постоянной, практически равной температуре испарения жидкости со свободной поверхности. В периоде падающей скорости сушки испарение влаги с поверхности материала замедляется, его температура начинает подниматься и может достигнуть температуры газовой фазы
1- сушка тонких пористых материалов (бумага, тонкий картон), 2- сушка коллоидных тел, 3- сушка капиллярно-пористых тел, 4- сушка капиллярно-пористых тел сложной структуры.
Нижняя часть 4-кривой – удаление адсорбционной влаги, верхняя часть – удаление капиллярной влаги.
АДСОРБЦИЯ Адсорбцией называют процесс поглощения вещества из смеси газов, паров или растворов поверхности или объемом пар твердого тела - адсорбента. Поглощаемое вещество, находящееся в газе, паре называется адсорбтивом, а поглощенное - адсорбатом. Адсорбцию подразделяют на два вида: физическую и химическую. Физическая адсорбция обусловлена поверхностными вандервальсовыми силами, удерживающими на поверхности адсорбента несколько слоев молекул адсорбата. При химической адсорбции поглощаемое вещество вступают в химическое взаимодействие с адсорбентом с образованием на его поверхности химических соединений. Силы притяжения возникает на поверхности адсорбента благодаря тому, что силовое поле поверхностных атомов и молекул не уравновешено силами взаимодействия соседних частиц. Заполнение адсорбатом поверхности адсорбента частично уравновешивает поверхностные силы и уменьшает поверхностное натяжение. Это в конечном счете сводит к выделению тепла. Следовательно, процессы адсорбции экзотермичны. Процессы адсорбции избирательны и обратимы (десорбции). Частным случаем хемосорбции является ионный обмен между твердым ионообменным сорбентом и раствором электролита. Кинетика, а также наружное оформление ионообменных процессов близких и адсорбционным.
Адсорбенты. Адсорбенты - пористые тела, обладающие большим объемом микропор. В адсорбентах основное количество поглощенного вещества сорбируется на стенках микропор (r< Поглотительная (адсорбционная) способность адсорбентам- максимально возможная концентрация адсорбтива в станице массы или объема адсорбента. Максимально возможную в данных условиях поглотительная способность адсорбента называют равновесной активностью. Статическая активность (Аст)- количество вещества, поглощенного единицей массы адсорбента от начало до равновесия при статических условиях. Динамическая активность (Адин) - при движении смеси через слой адсорбента.
Аст > Адин. Расчеты ведут по Адин. По химическому составу адсорбенты можно разделить на углеродные и не углеродные. Углеродные - активные углероды, углеродные возможности материалы,меняют виды твердого топлива. Удельная поверхность активных углей (6 ÷17)· Не углеродные- активный оксид алюминия, алюмогели, цеолиты, глинистые породы. Силикагель- (4÷8)· Алюмогель- до 4 · Глинистые породы применяют для очистки жидкостей от различных смесей.
Равновесие при адсорбции. Равновесная концентрация
Или, в случае адсорбции газов:
Здесь у- концентрация адсорбтива в объемной фазе, р- парциальное давление адсорбтива в объемной фазе. Зависимость Равновесное зависимость описываются рядом эмпирическая и теоретических уравнений. Одна из них уравнение Лангмюра:
Здесь
Рис 6.1. Изотермы адсорбции.
1-Изотерма Лангмюра, 2,3- реальные изотермы. Отклонение 2 и 3 от 1 объясняется, что адсорбция не является мономолекулярной, а осуществляется в нескольких слоях молекул.
|
||||||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 380; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.122.162 (0.01 с.) |
 определяет изменение влагосодержания твердого материала по времени.
определяет изменение влагосодержания твердого материала по времени.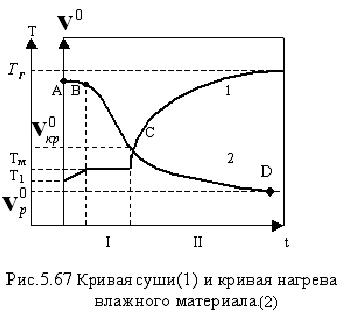
 до температуры мокрого термометра
до температуры мокрого термометра 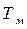 и на испарение части влаги (рис. 5.68).
и на испарение части влаги (рис. 5.68). . С уменьшением влажности материала вклад внутридиффузионного сопротивления в общее сопротивление процесса увеличивается, общее сопротивление диффузии возрастает, а скорость сушки падает. Снижается также концентрации пара у поверхности испарения, приближаясь к концентрации пара в газовой фазе.
. С уменьшением влажности материала вклад внутридиффузионного сопротивления в общее сопротивление процесса увеличивается, общее сопротивление диффузии возрастает, а скорость сушки падает. Снижается также концентрации пара у поверхности испарения, приближаясь к концентрации пара в газовой фазе.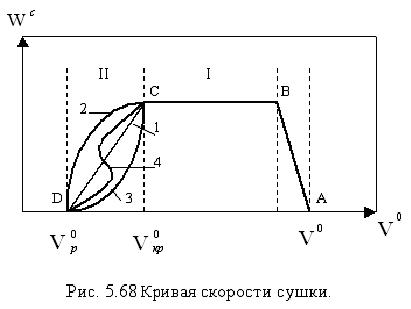
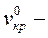 критическое влагосодержание.
критическое влагосодержание. м). Количество остальных пор, более крупных, сводимая к транспортированию адсорбента вещества к макропорам.
м). Количество остальных пор, более крупных, сводимая к транспортированию адсорбента вещества к макропорам.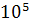
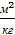
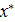 (
(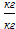 чистого адсорбента) поглощаемого вещества в адсорбенте м.б. представлена
чистого адсорбента) поглощаемого вещества в адсорбенте м.б. представлена
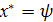 (р,Т)
(р,Т) или
или 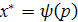 при T=const называется адсорбции.
при T=const называется адсорбции.
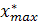 - предельная величина адсорбции, при полном затемнение внутренних пор мономолекулярным слоем адсорбата, b- константа.
- предельная величина адсорбции, при полном затемнение внутренних пор мономолекулярным слоем адсорбата, b- константа.