Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Построение диаграмм состояния двойных систем. Правило фаз.Содержание книги
Поиск на нашем сайте
Фаза (Ф) - однородная часть системы, имеющая свой химический состав, свойства и отделённая от других границей раздела. Система (С) – любое вещество (Ме или сплав) состоящее из определённой совокупности фаз, если система состоит из 1-й фазы, то она гомогенна, если из 2-х и более – гетерогенна. Компонент (К) – химически индивидуальные простые и сложные вещества образующие систему. а), б) неограниченной раст-сти компонентов в твердом состоянии; в), г) отсутствия растворимости компонентов в твердом состоянии; д), е) ограниченной растворимости компонентов в твердом состоянии. Верхняя линия на диаграмме - линия ликвидус показывает начало кристаллизации или конец плавления. Выше этой линии все сплавы находятся в однофазном(жидком) состоянии. Нижняя линия - линия солидус - конец кристаллизации или начало плавления. Ниже этой линии все сплавы также в однофазном(твердом) состоянии.
Диаграммы состояния строятся в координатах t-оси ординат и концентрация компонентов – ось абсцисс. Линия АДВ – линия ликвидус. а представляет собой геометрическое место точек соответствующих температурам, при которых из жидкости начинают выпадать кристаллы, следовательно выше линии ликвидус сплав находится в жидком состоянии. Линия СДЕ называется солидус. Она представляет собой геометрическое место точек, соответствующих температурам, при которых жидкая фаза исчезает, следовательно ниже линии солидус сплав находится в твердом состоянии. Между линиями ликвидус и солидус сплав находится в жидко- твердом состоянии, и чем ниже температура относительно линии ликвидус, тем больше кристаллов и меньше жидкой фазы в сплаве. В точке Д из жидкости одновременно начинают выпадать кристаллы компонентов (фаз). Для диаграмм этого типа компонент и фаза являются синонимами. Для диаграмм другого типа необходимо говорить только о фазах, поскольку компонент и фаза не являются синонимами. Механическая смесь, состоящая из двух или более фаз, одновременно кристаллизующаяся в жидкости называется эвтептикой. Ниже точки Д на диаграмме структура представляет собой чисто эвтептической.
Посредством правила отрезков можно определить состав фаз в любой двухфазной области и количественное их соотношение. Правило отрезков состоит из двух частей. Первая часть: для того чтобы определить состав фаз через заданную точку в двухфазной области (точка соответствует конкретной температуре) проводят горизонтальную линию до пересечения с линиями, ограничивающими эту область. Проекция точек пересечения на ось концентрации даст нам состав фаз. Вторая часть: для того чтобы определить количество фаз через заданную точку проводят горизонтальную линию до пересечения с линией, ограничивающей эту область. Отрезки между заданной точкой и точками с соответствующим составом фаз обратно пропорциональны их количеству.
|
||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 560; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.156 (0.009 с.) |

 Диаграмма состояния представляет собой графическое отображение состояния сплава в зависимости от температуры, давления и концентрации. Диаграмма есть наглядное отображение устойчивых фаз при комнатной температуре. Мера устойчивости фаз определяется законом Гиббса или правилом фаз. Правило фаз устанавливает связь между числом степеней свободы, числом фаз и компонентов. Под числом степеней свободы понимают число внешних и внутренних факторов, которые можно изменять без изменения числа фаз в системе.
Диаграмма состояния представляет собой графическое отображение состояния сплава в зависимости от температуры, давления и концентрации. Диаграмма есть наглядное отображение устойчивых фаз при комнатной температуре. Мера устойчивости фаз определяется законом Гиббса или правилом фаз. Правило фаз устанавливает связь между числом степеней свободы, числом фаз и компонентов. Под числом степеней свободы понимают число внешних и внутренних факторов, которые можно изменять без изменения числа фаз в системе. Правило фаз выполняется: с = к - ф + 2, где к – число компонентов, с – число степеней свободы, ф –число фаз, 2 – внешние факторы, т.е. изменяющаяся температура и давление, для сплавов принята несколько иная форма зависимости с = к -ф + 1 при условии постоянства давления.
Правило фаз выполняется: с = к - ф + 2, где к – число компонентов, с – число степеней свободы, ф –число фаз, 2 – внешние факторы, т.е. изменяющаяся температура и давление, для сплавов принята несколько иная форма зависимости с = к -ф + 1 при условии постоянства давления. Диаграммы состояния строят экспериментально по кривым охлаждения сплавов. На кривых охлаждения определяют критические точки – температуры перегиба или площадки на кривой, связанные с тепловым эффектом фазового превращения. По ним определяют температуру превращения.
Диаграммы состояния строят экспериментально по кривым охлаждения сплавов. На кривых охлаждения определяют критические точки – температуры перегиба или площадки на кривой, связанные с тепловым эффектом фазового превращения. По ним определяют температуру превращения.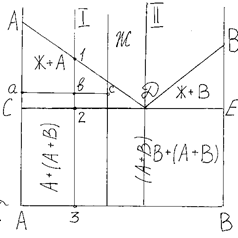 13. Диаграмма состояния для сплавов, образующих механические смеси из чистых компонентов.
13. Диаграмма состояния для сплавов, образующих механические смеси из чистых компонентов. 14. Правило отрезков.
14. Правило отрезков.