
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Значение окислительного декарбоксилирования пируватаСодержание книги Поиск на нашем сайте
Реакции пируватдегидрогеназного комплекса связывают метаболические пути гликолиза,глюконеогенеза, синтеза жирных кислот с циклом лимонной кислоты. ПДГ-комплекс имеет огромное значение в поддержании гомеостаза. Энергетический метаболизм аэробных тканей (например, мозга) очень зависит от превращения пирувата в ацетил-КоА, поэтому такие ткани более чувствительны к нарушениям ПДГ-комплекса. Большинство нарушений, связанных с недостаточностью пируватдегидрогеназной активности, обусловлены мутациями пируватдегидрогеназы. Главными последствиями таких нарушений являются энцефалопатии и церебральные молочные ацидозы. Регуляция общего пути катаболизма Ряд реакций общего пути катаболизма зависит от концентрации адениловых нуклеотидов - АТФ, АДФ и АМФ. Суммарная концентрация адениловых нуклеотидов в клетке постоянна, но относительные концентрации могут изменяться вследствие их взаимопревращений. Во многих клетках концентрации АТФ, АДФ и АМФ относятся как 100:10:1. Отсюда следует, что небольшие изменения концентрации АТФ могут приводить к значительным изменениям концентрации других нуклеотидов. Для оценки влияния система адениловых нуклеотидов на метаболические процессы пользуются величиной энергетического заряда клетки: Если весь фонд адениловых нуклеотидов представлен только АТФ, то энергетический заряд равен 1. Если в клетке имеется только АМФ, то энергетический заряд равен 0. В большинстве клеток энергетический заряд равен 0,8 - 0,9. При уменьшении клеточного заряда (уменьшении [АТФ], увеличении [АДФ], [АМФ]) скорость реакций общего пути катаболизма увеличивается. В скелетных мышцах энергетический заряд равен 0,94 как в покое, так и при интенсивной мышечной работе. В процессе дыхания пировиноградная кислота вступает в цикл трикарбоновых кислот. Это сложный замкнутый круг превращений, в результате которых образуются органические кислоты с 4, 5 и 6 атомами углерода (яблочная, молочная, фумаровая, а-кетоглутаровая и лимонная) и отщепляется углекислота. Суммарная реакция цикла выражена уравнением: СН3СО — S —КоА + ЗН2О + ЗНАД + ФАД+АДФ + Фн →2СО2 + НS-КоА + ЗНАД.Н2 + ФАДН2 + АТФ. Таким образом, окисление одной молекулы пировиноградной кислоты сопровождается образованием ЗСО2 15 молекул АТФ. Однако при распаде молекулы глюкозы образовались две молекулы пировиноградной кислоты. Следовательно, всего в аэробной фазе дыхания образуется 6 молекул СО2 и 30 молекул АТФ плюс 8АТФ в анаэробной фазе. Итого 6 молекул СО2 и 38 молекул АТФ образуется в процессе окислительно-дыхательного распада молекулы гексозы. На образование 38 молекул АТФ затрачено 38-30,6 кДж = 1162,8 кДж. Всего при сжигании 1 моль глюкозы выделяется 2824 кДж: C6H12O6 + 6O2->6CO2 + 6H2O + 2824 кДж. Эффективность процесса дыхания составляет(КПД):
(1162,8: 2880) • 100% = 40,37%. 28. Термодинамика полного окисления глюкозы. Расчет биологического окисления глюкозы. Энергетический обмен Для жизнедеятельности организма необходима энергия. Растения аккумулируют солнечную энергию в органических веществах при фотосинтезе. В процессе энергетического обмена органические вещества расщепляются и энергия химических связей освобождается. Частично она рассеивается в виде тепла, а частично запасается в молекулах АТФ. У животных энергетический обмен протекает в три этапа. Первый этап — подготовительный. Пища поступает в организм животных и человека в виде сложных высокомолекулярных соединений. Прежде чем поступить в клетки и ткани, эти вещества должны разрушиться до низкомолекулярных, более доступных для клеточного усвоения веществ. На первом этапе происходит гидролитическое расщепление органических веществ, идущее при участии воды. Оно протекает под действием ферментов в пищеварительном тракте многоклеточных животных, в пищеварительных вакуолях одноклеточных, а на клеточном уровне — в лизосомах. Реакции подготовительного этапа: белки + Н20 -> аминокислоты + Q; жиры + Н20 -> глицерин + высшие жирные кислоты + Q; полисахариды -> глюкоза + Q. У млекопитающих и человека белки расщепляются до аминокислот в желудке и в двенадцатиперстной кишке под действием ферментов — пептидгидролаз (пепсина, трипсина, хемотрипсина). Расщепление полисахаридов начинается в ротовой полости под действием фермента птиалина, а далее продолжается в двенадцатиперстной кишке под действием амилазы. Там же расщепляются и жиры под действием липазы. Вся энергия, выделяющаяся при этом, рассеивается в виде тепла.
Образующиеся низкомолекулярные вещества поступают в кровь и доставляются ко всем органам и клеткам. В клетках они поступают в лизосому или непосредственно в цитоплазму. Если расщепление происходит на клеточном уровне в лизосомах, то вещество сразу же поступает в цитоплазму. На этом этапе происходит подготовка веществ к внутриклеточному расщеплению. Второй этап — бескислородное окисление. Второй этап осуществляется на клеточном уровне при отсутствии кислорода. Он протекает в цитоплазме клетки. Рассмотрим расщепление глюкозы, как одного из ключевых веществ обмена в клетке. Все остальные органические вещества (жирные кислоты, глицерин, аминокислоты) на разных этапах втягиваются в процессы ее превращения. Бескислородное расщепление глюкозы называется гликолизом. Глюкоза претерпевает ряд последовательных превращений. Вначале она преобразуется во фруктозу, фосфорилируется — активируется двумя молекулами АТФ и превращается во фруктозо-дифосфат. Далее молекула шестиатомного углевода распадается на два трехуглеродных соединения — две молекулы глицерофосфата (триозы). После ряда реакций они окисляются, теряя по два атома водорода, и превращаются в две молекулы пировиноградной кислоты (ПВК). В результате этих реакций синтезируются четыре молекулы АТФ. Так как первоначально на активацию глюкозы было затрачено две молекулы АТФ, то общий итог составляет 2АТФ. Таким образом, выделяющаяся при расщеплении глюкозы энергия частично запасается в двух молекулах АТФ, а частично расходуется в виде тепла. Четыре атома водорода, которые были сняты при окислении глицерофосфата, соединяются с переносчиком водорода НАД+ (никотинамид-динуклеотидфосфат). Это такой же переносчик водорода, как и НАДФ+, но участвует в реакциях энергетического обмена. Обобщенная схема реакций гликолиза: С6Н1206 + 2НАД+ -> 2С3Н403 + 2НАД•2H 2АДФ -> 2АТФ Восстановленные молекулы НАД•2Н поступают в митохондрии, где окисляются, отдавая водород. В зависимости от типа клеток, ткани или организмов пировиноградная кислота в бескислородной среде может превращаться далее в молочную кислоту, этиловый спирт, масляную кислоту или другие органические вещества. У анаэробных организмов эти процессы называются брожением. Молочнокислое брожение: С6Н1206 + 2НАД+ -> 2С3Н403 + 2НАД•2Н <=> 2С3Н603 + 2НАД+ Глюкоза ПВК молочная кислота
Спиртовое брожение: С6Н1206 + 2НАД+ -> 2С3Н403 + 2НАД•2Н <=> 2С2Н5ОН + 2С02 + 2НАД+ Глюкоза ПВК этиловый спирт
Третий этап — биологическое окисление, или дыхание. Этот этап протекает только в присутствии кислорода и иначе называется кислородным. Он протекает в митохондриях. Пировиноградная кислота из цитоплазмы поступает в митохондрии, где теряет молекулу углекислого газа и превращается в уксусную кислоту, соединяясь с активатором и переносчиком коэнзимом-А (рис. 17). Образующийся ацетил-КоА далее вступает в серию циклических реакций. Продукты бескислородного расщепления — молочная кислота, этиловый спирт — также далее претерпевают изменения и подвергаются окислению кислородом. В пировиноградную кислоту превращается молочная кислота, если она образовалась при недостатке кислорода в тканях животных. Этиловый спирт окисляется до уксусной кислоты и связывается с КоА. Циклические реакции, в которых происходит преобразование уксусной кислоты, носят название цикла ди- и трикарбоновых кислот, или цикла Кребса, по имени ученого, впервые описавшего эти реакции. В результате ряда последовательных реакций происходит декарбоксилирование — отщепление углекислого газа и окисление — снятие водорода с образующихся веществ. Углекислый газ, образующийся при декарбоксилировании ПВК и в цикле Кребса, выделяется из митохондрий, а далее из клетки и организма в процессе дыхания. Таким образом, углекислый газ образуется непосредственно в процессе декарбоксилирования органических веществ. Весь водород, который снимается с промежуточных веществ, соединяется с переносчиком НАД+, и образуется НАД•2Н. При фотосинтезе углекислый газ соединяется с промежуточными веществами и восстанавливается водородом. Здесь идет обратный процесс.
Общее уравнение декарбоксилирования и окисления ПВК: 2С3Н403 + 6Н20 + 10НАД+ -> 6С02 + 10НАД• Н. Проследим теперь путь молекул НАД•2Н. Они поступают на кристы митохондрий, где расположена дыхательная цепь ферментов. На этой цепи происходит отщепление водорода от переносчика с одновременным снятием электронов. Каждая молекула восстановленного НАД•2Н отдает два водорода и два электрона. Энергия снятых электронов очень велика. Они поступают на дыхательную цепь ферментов, которая состоит из белков — цитохромов. Перемещаясь по этой системе каскадно, электрон теряет энергию. За счет этой энергии в присутствии фермента АТФ-азы синтезируются молекулы АТФ. Одновременно с этими процессами происходит перекачивание ионов водорода через мембрану на наружную ее сторону. В процессе окисления 12 молекул НАД-2Н, которые образовались при гликолизе (2 молекулы) и в результате реакций в цикле Кребса (10 молекул), синтезируются 36 молекул АТФ. Синтез молекул АТФ, сопряженный с процессом окисления водорода, называется окислительным фосфорилированием. Этот процесс был впервые описан русским ученым В. А. Энгельгардтом в 1931 г. Конечным акцептором электронов является молекула кислорода, поступающая в митохондрии при дыхании. Атомы кислорода на наружной стороне мембраны принимают электроны и заряжаются отрицательно. Положительные ионы водорода соединяются с отрицательно заряженным кислородом, и образуются молекулы воды. Вспомним, что кислород атмосферы образуется в результате фотосинтеза при фотолизе молекул воды, а водород идет на восстановление углекислого газа. В процессе энергетического обмена водород и кислород вновь соединяются и превращаются в воду.
Обобщенная реакция кислородного этапа окисления: 2С3Н403 + 4Н + 602 -> 6С02 + 6Н20; 36АДФ -> 36АТФ. Итак, выход молекул АТФ при кислородном окислении в 18 раз больше, чем при бескислородном.
Суммарное уравнение окисления глюкозы на двух этапах: С6Н1206 + 602 —> 6С02 + 6Н20 + Е —> Q (тепло). 38АДФ —> 38АТФ Таким образом, при расщеплении глюкозы на двух этапах образуется суммарно 38 молекул АТФ, причем основная часть — 36 молекул — при кислородном окислении. Такой выигрыш энергии обеспечил преимущественное развитие аэробных организмов по сравнению с анаэробными. Эффективность энергетического обмена. Общее количество энергии, выделившееся в процессе энергетического обмена, составляет 2880 кДж/моль. Из них часть рассеивается в виде тепла, а часть запасается в 38 молекулах АТФ. Энергия, запасенная в 1 моль АТФ, составляет 30,6 кДж/моль. В 38 молекулах АТФ запасается 38 • 30,6= 1162,8 кДж/моль. Эффективность процесса дыхания составляет: (1162,8: 2880) • 100% = 40,37%. Таким образом, при аэробном окислении глюкозы запасается в виде АТФ 40,37% энергии. При анаэробном окислении образуются лишь две молекулы АТФ. Рассчитаем эффективность этого процесса. Общее количество энергии спиртового брожения составляет 210 кДж/моль. Эффективность спиртового брожения: (2 •30,6: 210) • 100% = 29,14%. Общее количество энергии при молочнокислом брожении (гликолиз в мышцах) составляет 150 кДж/моль. Эффективность молочнокислого брожения: (2 • 30,6: 150) • 100% = 40,8%. 29. Этапы унификации энергетических субстратов в процессах катаболизма. ЦТК начинается с подготовительного этапа – окислительное декарбоксилирование ПВК до ацетил –КоА. ПВК является одним из рех конечных продуктов гидролиза при гликолизе – анаэробного процесса распада глюкозы. Ацетил – КоА – при окислении аминокислот и жирных кислот, т.е. не только углеводов. Таким образом, в качестве энергетического субстрата могут выступать все основные запасные вещества – углеводы, белки, жиры. Наиболее важный процесс деградации жирных кислот – β – окисление, которое происходит в митохондриях. При этом жирные кислоты активируются в цитоплазме и присоединяются к ацетил – КоА, а затем с помощью транспортной системы попадают в митохондриальный матрикс, где разрушаются в β – окислении до ацетил –КоА, который в свою очередь полностью окисляется до СО2 в ЦТК. Таким образом, β – окисление тесно связано с ЦТК и дыхательной цепью. Так при каждом цикле такого окисления образуется 1 молекула ФАДН2 и 1 молекула НАДН2. В дыхательной цепи ФАДН2 через КоА дает 2 молекулы АТФ, а НАДН2 – 3 молекулы АТФ. А весь цикл дает 5 молекул АТФ. При β – окислении пальмитиновой кислоты происходит 7 циклов; в итоге 35 молекул АТФ. 8 молекул ацетил – КоА. Сгорая в ЦТК, каждая дает 12 молекул АТФ; в итоге 96 молекул АТФ. Таким образом, при полном окислении: 35+96=131 молекула АТФ, но на активирование пальмитиновой кислоты ушла 1 молекула, поэтому 130 молекул АТФ. 130 АТФ*35,4= 4602 кДж\моль*Е При сгорании пальмитиновой кислоты образуется 9797 кДж энергии. η=4602/9797 * 100%=47% 47 % энергии идет на синтез АТФ, остальная часть энергии рассеивается в виде теплоты
30.Энергетическая сущность окислительного фосфорилирования. Коэффициент Р/О. Окислительное фосфорилирование осуществляет в живых клетках синтез молекул АТФ из АДФ и фосфорной кислоты за счет энергии окисления молекул органических веществ (субстратов). В результате о.ф. в клетка накапливается АТФ – макроэргическое соединение, расходуемое затем на обеспечение энергией различных процессов жизнедеятельности. Основные субстраты о.ф. – органические кислоты, образующиеся в цикле трикарбоновых кислот. Энергия, образующаяся при прохождении потока электронов по дыхательной цепи, используется для сопряженного фосфорилирования АДФ. Соотношение окисления и фосфорилирования определяется коэфф Р/О – количество моль фосфорилированного АДФ на ½ моль кислорода. Коэфф Р/О зависит от точки вхождения восстановительных эквивалентов в цепь транспорта электронов. Для НАДН2 и субстратов (малат), которые окисляются НАДН-дегидрогеназами. Р/О=3. Для ФАДН2, когда происходит превращение сукцината в фумарат в ЦТК Р/О=2. Т.е. Цепь транспорта электронов функционирует как протонная (Н+)-помпа, осуществляя перенос протонов из матрикса ч/з внутреннюю мембрану в межмембранное пространство. Перенос протонов приводит к возникновению разности концентрации Н+ с двух сторон митохондриальной мембраны: более высокая концентрация будет снаружи и более низкая – внутри. Электрохим потенциал способен заставлять протоны двигаться в обратном направлении, но мембрана непроницаема для них кроме отдельных участков, называемых протонными каналами. Обратный перенос протонов в матрикс является экзоорганическим процессом, высвобождающаяся при этом энергия используется на фосфорилирование АДФ. Этот процесс катализирует Н+-АТФ-синтетаза. Дыхательная цепь является частью процесса окислительного фосфорилирования.
31. Современное представление о строении и переносе электронов в дыхательной цепи митохондрий. Последовательность расположения компонентов дыхательной цепи определяется величиной их RedOx-потенциала и способностью переносить только электроны (e) либо одновременно и электроны, и протоны (p). Электроны переносятся от элементов с более низкими стандартными потенциалами (т.е. от более активных восстановителей) к элементам с более высокими стандартными потенциалами. I комплекс – НАДН2:CoQ-оксидоредуктаза (ФМН-зависимая, с FeS-центрами). Принимает на стороне митохондриального матрикса 2 Н (2 e + 2 p) от НАДН2, имеющего самый низкий стандартный потенциал (Е0= - 0,32 В), окисляя его до НАД, высвобождает 2 p в межмембранное пространство МТХ, а 2 e передает дальше по e-транспортной цепи – на III комплекс. II комплекс – сукцинат-дегидрогеназа (ФАД-зависимая, с FeS-центрами), принимает 2 e и 2 p от ФАДН2 с Е0= - 0,15 В (окисляя его до ФАД) на стороне митохондриального матрикса и передает их напрямую на CoQ III комплекса, минуя I комплекс. III комплекс – CoQН2:cyt c-оксидоредуктаза (с FeS-центром; включает в себя убихинон, FeS-белок и цитохромы b, c1, c), принимает e от комплексов I и II и передает на IV комплекс e-транспортной цепи, а также высвобождает в межмембранное пространство 2 p, полученных от II комплекса либо захваченных из митохондриального матрикса сопряжено с переносом пары e от I комплекса. IV комплекс – цитохромоксидаза (комплекс цитохромов a, a3), переносит e с cyt c III комплекса на конечный акцептор – О2, восстанавливая его до Н2О с Е0= + 0,82 В в митохондриальном матриксе. НАДН2-дегидрогеназа и CoQ – способны переносить как e, так и р. Поэтому являются 2 точками сопряженной перекачки р. Механизм третьей точки сопряжения не ясен. В итоге переносятся по цепи 2 e и с одной стороны внутренней митохондриальной мембраны на другую – 6 р. В случае, когда донор e – ФАДН2, только 4 р, т.к. минуется первая точка сопряжения. 32. Современные представления о механизме сопряжения окисления и фосфорилирования в биосистемах. В начале исследования этого механизма выдвигаемые гипотезы формировались в две группы: химическую и конформационную. Сторонники химической гипотезы, к которым относилось подавляющее число исследователей, отталкивались от прецедента субстратного фосфорилирования, которое реализуется на предварительных стадиях гликолиза. Это обычная ферментативная реакция между водорастворимыми субстратами. Конформационная гипотеза опиралась на представление о том, что процесс окисления НАДН может привести к формированию локальных напряжений внутренней мембраны митохондрий, запасающих часть энергии, выделяемой в процессе окисления. Затем, возвращаясь к исходному состоянию, мембрана подобно расправляющейся пружине может передать свободную энергию участникам реакции фосфорилирования. Такие изменения структуры митохондриальной мембраны могли бы быть опосредованы, например, каким-либо мембранно-связанным белком. Затем появилась альтернативная гипотеза, получившая название хемиосмотической. В 1961 году английский биохимик П. Митчел высказал предположение, что для сопряжения окисления НАДН2 с синтезом АТФ из АДФ и Ф необходима целостность внутренней мембраны митохондрий, т. е. она должна чётко отделять внутреннее пространство митохондрии («матрикс») от цитоплазмы клетки. Это была качественно новая идея. То, что многие ферменты в клетке нормально функционируют только в тесном контакте с мембраной или даже встроены внутрь мембраны, было известно, но топология мембранной системы никогда не считалась важной для протекания биохимических реакций.
|
|||||||||
|
Последнее изменение этой страницы: 2016-04-23; просмотров: 2409; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.178.65 (0.01 с.) |


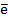 и
и  от НАДН2 И ФАДН2 проходят через 3 или 2 участка сопряжения, соответственно. Т.е при переносе 1 пары
от НАДН2 И ФАДН2 проходят через 3 или 2 участка сопряжения, соответственно. Т.е при переносе 1 пары 


