
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кафедра органической, физической и коллоидной химииСодержание книги
Поиск на нашем сайте
МОСКОВСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ ТЕХНОЛОГИЙ И УПРАВЛЕНИЯ (образован в 1953 году) ____________________________________________________ Кафедра органической, физической и коллоидной химии
Дистанционное Обучение Зимон А.Д., Бондарев Ю.М., Зарубин Д.П., Козлова Л.В., Павлов А.Н. КОЛЛОИДНАЯ ХИМИЯ НАНОЧАСТИЦ
Рабочая программа, методические указания и контрольные задания для студентов технологических специальностей всех форм обучения
Москва - 2007
УДК 547
© Авторы: Зимон А.Д., Бондарев Ю.И., Зарубин Д.П., Козлова Л.В., Павлов А.Н. Коллоидная химия наночастиц. Методические указания. –М., МГУТУ, 2007
Настоящее методическое пособие предназначено для студентов технологических специальностей всех форм обучения МГУТУ, и является основным документом для этих категорий студентов в их самостоятельной работе над коллоидной химией наночастиц. Оно содержит: 1) программу курса, определяющую объём знаний, необходимый для сдачи экзамена или зачёта, 2) контрольные задания (теоретические вопросы и задачи), выполнение которых необходимо для допуска к экзамену или зачёту, 3) методические рекомендации и справочные данные, призванные облегчить изучение дисциплины и выполнение контрольных заданий.
Рецензент: Антипов Владимир Николаевич. к.х.н., доцент, и.о. зав. кафедрой физической и коллоидной химии Московского государственного университета прикладной биотехнологии
Редактор: Свешникова Н.И.
© Московский государственный университет технологий и управления, 2007 109004, Москва, Земляной вал, 7 Содержание
Программа курса коллоидной химии наночастиц Цели и задачи дисциплины Цели преподавания дисциплины: коллоидной химии наночастиц являются фундаментальными науками в системе естественных наук, объединяющими, углубляющими и завершающими химическое образование специалистов-технологов для пищевой промышленности. Знания, полученные при изучении коллоидной химии наночастиц, являются базовыми для последующего изучения ряда специальных дисциплин. Задачи изучения дисциплины: - знать фундаментальные законы и основополагающие понятия коллоидной химии наночастиц; - иметь теоретические основы для глубокого понимания современных сложных - овладеть методами исследования и приобрести экспериментальные навыки
РАЗДЕЛ 1
Классификация и поверхностные свойства наночастиц Классификация наночастиц Диапазон размеров наночастиц: наименьший, определяющий возможность образования фазовой границы между дисперсной фазой и дисперсионной средой. Предельный размер, соответствующий размеру некоторых физических величин (протяженности дислокации, длиной свободного пробега электронов). Разнообразие и многообразие форм наночастиц, как дисперсной фазы. Трехмерные, двухмерные (нановолокна, нанопоры, нанотрубки, нанокапилляры), одномерные в виде пленок и адсорбционных слоев. Наноструктуры из наночастиц и в объеме (в том числе металлические наночастицы в полимерах) и порах твердого тела. Классификация систем наночастиц по агрегатному состоянию дисперсной фазы и дисперсионной среды.
Дисперсная фаза наночастиц Структура, форма и размер дисперсной фазы наночастиц. Неравновесный процесс образования наночастиц. Разнообразие форм частиц данной фазы в зависимости от условий получения (давление, температура и т.д.). Изменение плотности наночастиц за счет пустот, пор и газовых полостей. Различная ориентация кристаллов, способствующих понижению плотности на границе раздела фаз. Многокомпонентная и многофазная структура наночастиц. Особенности строения кристаллических и аморфных наночастиц. Монодисперсность и полидисперсность наночастиц. Теоретические распределения наночастиц по размерам – нормальное или логнормальное (логарифмическое нормальное). Зависимость полидисперсности наночастиц от их свойств, способов получения, «времени жизни» и других факторов. Значительная удельная поверхность наночастиц за счет пористости, различной плотности, геометрической неоднородности, кристаллической структуры.
Поверхностная энергия Дополнительный избыток поверхностной энергии наночастиц, обусловленный их размерами, условием образования (высокие или низкие температуры, значительная скорость процесса, воздействие мощных источников излучения) и изменением атомно-кристаллической структуры материалов. Возникновение неоднородной деформации и неоднородного распределения компонентов и фаз на поверхности. Увеличение смещения атомов, дефектность. Сокращение расстояния между атомами на плоскости. Поверхностная релаксация и избыточная поверхностная энергия. Избыточная энергия как энергия дефектов, пропорциональная их числу. Свободная поверхностная энергия в виде энергии Гиббса, ее поверхностное и объемное слагаемые. Удельная свободная поверхностная энергия. Поверхностное натяжение. Зависимость поверхностного натяжения от размеров наночастиц: расчёт по формуле Толмана и упрощенной формуле Русанова. Причины роста удельной поверхностной энергии по мере снижения размеров частиц. Увеличение доли атомов на поверхности частиц. Неравновесное состояние поверхности наночастиц. Изменение удельной свободной поверхностной энергии с течением времени и ее связь с энергией Гиббса. Способы определения удельной свободной поверхностной энергии наночастиц по кинетике испарения и температуры плавления.
РАЗДЕЛ 2 Поверхностные явления Адсорбция Влияние избытка поверхностной энергии на адсорбцию. Повышенная адсорбционная активность наночастиц и значительно адсорбционная емкость. Увеличение скорости адсорбционного процесса. Зависимость адсорбционного потенциала от размера частиц. Изменение свойств поверхности наночастиц в результате адсорбции. Каталитическая активность наночастиц и связь ее с избытком поверхностной энергии. Применение наночастиц для чистки воды.
Адгезия Причины повышенной адгезии наночастиц. Влияние избытка поверхностной энергии на адгезионное взаимодействие. Экспериментальное определение силы адгезии наночастиц путем моделирования и в сопоставлении с силой трения. Расчетные значения сил адгезии по теории Дерягина – Мюллера – Топорова (ДМТ). Связь силы адгезии с равновесной работой адгезии и поверхностным натяжением.
Адгезия нанокапель и особенности смачивания ими. Уравнения Юнга для нанокапель. Зависимость краевого угла от размера нанокапель. Возможность расчета этой зависимости. Сопоставление экспериментальных данных и расчетных по значению краевого узла наноразмерных капель. Линейное натяжение нанокапель и горизонтальная сила, приложенная трехфазовому контакту. Смачивание нитей нанокаплями и тонкой упругой пленки. Кинетика растекания нанокапель.
РАЗДЕЛ 3 Оптические свойства. Влияние дискретной кристаллической структуры наночастиц на рассеяние и поглощение света. Оптические свойства в зависимости от размера наночастиц. Отклонение от закона Бугера-Ламберта-Бера при пропускании света через слой наночастиц.
РАЗДЕЛ 4 Получение наночастиц РАЗДЕЛ 5 Устойчивость. Два вида устойчивости наночастиц – агрегативная и седиментационная. Возможно образование систем с фиксированным положением наночастиц в матрице, полимерной. Структуры образуются из наночастиц. Особенности седиментационной и агрегативной устойчивости в жидкой среде. Отклонение от теории ДЛФО и особенности расклинивающего давления с учетом того, что радиус наночастиц может быть меньше толщены прослойки между частицами. Расчет энергии межмолекулярного взаимодействия в зависимости от отношения между радиусом наночастиц и прослойки между ними. Особенности определения константы Гамакера. Снижение энергии межмолекулярного взаимодействия с уменьшением размеров наночастиц. Расчет электростатической компоненты расклинивающего давления с учетом перекрытия двойных электрических слоев. Агрегативная неустойчивость. Связь электрокинетических явлений с величиной дзета – потенциала. Коагуляция и нарушение агрегативной и седиментационной устойчивости. Зависимость этих процессов от свойств наночастиц растворителя и внешнего воздействия.
Рекомендуемая Литература
Основная 1. Зимон А.Д. «Коллоидная химия». Изд – 5 М. Апрель 2007 344с. 3. Зимон А.Д., Вегера А.В. «Коллоидная химия наносистем» М. МГУТУ. 2004.с.24. Специальная 1. Сергеев Г.Б. «Нанохимия». М. Изд. МГУ. 2003. 287с. 2. Андриевский Р.А., Рагуля А.В. «Наноструктурные материалы». М. Академия. 2003. 312с. 3. Сб. «Наномикросистемная техника». Ред. Мальцев П.Г. М. Техносфера. 2005. 580с. 4. Сб. «Коллоидно-химические основы нанонауки». Ред. Шпак А.П., Ульберг З.Р. Киев. Академпериодика. 2005. 466с.
ОРГАНИЗАЦИОННО-МЕТОДИЧЕСКИЕ ДАННЫЕ ПО ДИСЦИПЛИНЕ «КОЛЛОИДНАЯ ХИМИЯ НАНОЧАСТИЦ»
ТЕМАТИЧЕСКИЙ ПЛАН ЛЕКЦИЙ 1. Для студентов ДФО.
1. Классификация наночастиц 2 2. Поверхностная энергия 2 3. Адсорбция и адгезия 2 4. Свойства наночастиц 2 5.Получение наночастиц 2 6. Устойчивость наносистем 2 ---------------- Итого: 12 часов
2. Для студентов ВФО и ЗФО
1. Особенности наносистем и классификация 2 2. Поверхностная энергия и поверхностные 2 явления 3. Получение наночастиц и их устойчивость 2
___________ Итого: 6 часов
ТРЕБОВАния к выполнению контрольных заданий
Контрольные задания для студента любой формы обучения состоят из 5 теоретических вопросов и 5 задач. Задания выполняются в виде домашней письменной контрольной работы в соответствии с индивидуальными вариантами. (Варианты перечислены в конце руководства). Выбор варианта осуществляется по двум последним цифрам шифра студенческого билета или зачётной книжки. Например, если последние две цифры шифра 8 и 1, то следует выполнять 81-ый вариант заданий, если 0 и 1, то – вариант 1, если 0 и 0, то вариант 00 (в списке вариантов следует после № 99). Контрольные задания выполняются в отдельной тетради, ясным и разборчивым подчерком. Общим требованием к форме выполнения является: 1) указание шифра студенческого билета, наряду с фамилией, именем, отчеством и другими данными, позволяющими определить личную принадлежность работы, 2) указание номера выбранного варианта 3) указание номеров заданий (теоретических вопросов и задач) в соответствии с нумерацией в настоящем руководстве, и 3) письменное повторение формулировки задания. (То есть, формулировка, данная в руководстве, должна быть выписана вместе с номером задания перед ответом или решением). Ответы на вопросы и решения задач даются в той последовательности номеров заданий, какая указана в перечне вариантов. В конце контрольной работы необходимо указать список литературы, использованной при самостоятельном изучении предмета, с точным библиографическим описанием её. (В качестве примера, смотри библиографическое описание Рекомендуемой литературы). Контрольная работа подписывается студентом с указанием даты её окончания. Ответ на теоретический вопрос должен быть подробным, однако его объём, как правило, не должен превышать две страницы ученической тетради. Более развёрнутые ответы должны быть завершены краткими выводами, суммирующими основные положения ответа. Решение задачи должно содержать как математические формулы в общем виде, так и промежуточные результаты вычислений (выкладки), так чтобы ход решения задачи был очевиден.
В конце решения задачи должен быть дан краткий ответ с числовыми результатами, выраженными, как правило, в единицах СИ. Количество цифр в числовых (окончательных) результатах должно быть таким, какое подразумевается условием задачи. Графики выполняются вручную на бумаге с типографской сеткой, с указанием шкал и единиц измерений по осям координат. Каждый график должен иметь размер не менее 10×10 см. Не принимаются графики, выполнение с помощью компьютера на бумаге без сетки.
ОБЩИЕ методические указания по изучению дисциплины «Коллоидная химия наночастиц» ( самостоятельная работа студентов )
Изучение дисциплины "Коллоидная химия наночастиц" проходит в соответствии с рабочей программой. Фундаментом для изучения спецкурса являются знания, приобретённые студентами в курсах физической и коллоидной химии. Студентам необходимо овладеть классификацией наночастиц, методами их получения, в также основными физико-химическими методами изучения свойств наносистем. Самостоятельная работа студентов в межсессионный период предполагает изучение учебной литературы и выполнение контрольной работы, на что студентам ДФО отводится 26 часов, студентам ВФО 18 часов, студентам ЗФО 16 часов и студентам ЗФО (с) 12 часов. Для студентов технологических специальностей читаются лекции и проводятся лабораторные работы. Заканчивается курс зачетом.
Контрольные задания
Теоретические вопросы
1. Высокодисперсные системы как объекты коллоидной химии. Наночастицы - представители высокодисперсных систем 2. Новые качества наночастиц. Обоснование минимального и максимального размера наночастиц. Разнообразие и многообразие форм наночастиц. Трёхмерные, двухмерные и одномерные наночастицы. 3. Классификация наночастиц по агрегатному состоянию. Особенности кристаллических и аморфных наночастиц. Разнообразие структур и форм наночастиц. Структура и фазовое состояние наночастиц различных модификаций. 4. Причины повышенной удельной поверхности наночастиц. Полидисперсность наночастиц. Геометрическая неоднородность наночастиц. Распределение наночастиц по размерам: нормальное и логарифмическое нормальное. 5. Зависимость избыточной поверхностной энергии Гиббса G S от размера частиц. Поверхностные и объёмные слагаемые величины G S. 6. Влияние экстремальных условий образования наночастиц на поверхностные явления.. Избыточная поверхностная энергия как энергия дефектов кристаллических наночастиц. 7. Поверхностное натяжение s и его зависимость от размера наночастиц. Формула Толмана для s как функции размера наночастиц. Тоже по упрощённой формуле Русанова. 8. Способы определения поверхностного натяжения наночастиц. Связь между неравновесной и равновесной удельной свободной поверхностной энергией наночастиц. 9. Изменение удельной свободной поверхностной энергии с течением времени. 10. Влияние избытка поверхностной энергии на процесс адсорбции наночастицами. Повышенная адсорбционная активность (ёмкость) наночастиц. Увеличение скорости адсорбционного процесса. 11. Зависимость адсорбционного потенциала от размера частиц. Применение наночастиц для очистки воды. Особенности применения наночастиц в качестве катализатора. 12. Причины повышенной адгезии наночастиц. Влияние избытка поверхностной энергии на адгезионное взаимодействие наночастиц. Определение адгезии наночастиц путём моделирования 13. Расчётное значение силы адгезии наночастиц по теории Дерягина- Мюллера – Топорова (ДМТ). Связь силы адгезии с равновесной работой сил адгезии и поверхностном натяжении. 14. Уравнение Юнга для нанокапель. Зависимость краевого угла смачивания от размера нанокапель. Линейное натяжение нанокапель. 15. Смачивание нитей нанокаплями. Смачивание тонкой упругой плёнки. Стадии растекания нанокапель. Качественные особенности диффузии наночастиц. 16. Сопоставление диффузии наночастиц с ионной и молекулярной диффузией. Три вида диффузии в отношении кристаллических наночастиц. 17. Соотношение межкристаллической, поверхностной и межфазовой диффузии 18. Соотношение коэффициента диффузии для трёх её различных видов кристаллических тел. Особенности структуры аморфных наночастиц. 19. Влияние свойств наночастиц на броуновское движение. Зависимость броуновского движения от свойств наночастиц, дисперсионной среды и их взаимного влияния. 20. Осмотическое давление, его математическое выражение для наночастиц. Осмос через мембраны с наноразмерными порами. 21. Структура двойного электрического слоя с учётом дискретности кристаллической поверхности наночастиц. Соизмеримость адсорбционной и особенно диффузной части двойного электрического слоя с размерами самих наночастиц. Разделение электронного поля на наночастиц, находящегося в виде золя. 22. Электролитические явления в наноразмерных капиллярах. Электроосмос в зависимости от соотношения размера частиц и радиуса нанокапель. Линейная скорость электроосмоса в наноразмерных капиллярах. 23. Влияние дискретной кристаллической структуры наночастиц на рассеяние и поглощение света. Оптические свойства в зависимости от размера наночастиц. Отклонение от закона Бугера-Ламберта-Бера при пропускании света через слой наночастиц. 24. Классификация способов получения наночастиц. Диспергирование и конденсационные способы получения наночастиц. Специфические способы получения наночастиц. 25. Элементарные процессы и стадии механического диспергирования. Физические и химические способы получения наночастиц. Варианты процесса диспергирования. 26. Образование наночастиц конденсационными способами. Жидкостное восстановление и радиолиз. 27. Стадия метода молекулярного наращивания. Получение наночастиц кристаллизацией из раствора. Особенности получения частиц путём золь-гель перехода. 28. Классификация методов определения размеров наночастиц. Принцип работы сканируемых зондовых приборов. 29. Особенности двух видов устойчивости наночастиц. Системы с фиксированным положением наночастиц. 30. Седиментационная устойчивость золя и аэрозоля. Отклонение от теории ДЛФО для наночастиц. 31. Расчёт энергии межмолекулярного взаимодействия, в зависимости от отношения между радиусом наночастиц и прослойкой между ними. Зависимость энергии межмолекулярного взаимодействия от размеров наночастиц. 32. Особенности расклинивающего давления применено к наночастицам. Определение константы Гамакера 33. Расчёт электростатической компоненты расклинивающего давления для наночастиц. Связь электрической компоненты расклинивающего давления с величиной дзета-потенциала. Структурная компонента расклинивающего давления. 34. Условия коагуляции в зависимости от расстояния между наночастицами. Агрегативная устойчивость с учётом суммарного взаимодействия составляющих расклинивающего давления. 35. Коагуляция и нарушение агрегатной и седиментационной устойчивости наночастиц. Влияние растворителя и внешнего воздействия на коагуляцию наночастиц. 36. Механические свойства отдельных наночастиц (твёрдость, прочность и др.) и объектов из множества наночастиц. 37. Свободнодисперсные и связнодисперсные системы из наночастиц. Два типа структур связнодисперсных наночастиц – способные течь и обладающие прочностью. 38. Предел текучести связнодисперсных систем. Определение предела текучести кристаллических наночастиц по закону Холла-Петча. Предел текучести кристаллических наночастиц в зависимости от их микротвёрдости. 39. Особенности модуля Юнга и деформации для наночастиц. Упругие и прочностные свойства наночастиц. 40. Самопроизвольно образующиеся наночастицы. Прямые и обратные мицеллы. 41. Адсорбционный монослой ПАВ. Локальная концентрация и образование островковой наноразмерной структуры 42. Механизм образования двойного электрического слоя. Противоионы и потенциалопределяющие ионы. 43. Электрокинетические явления. 44. Электрокинетический потенциал. Его зависимость от концентрации противоионов. 45. Электрофорез. Скорость электрофореза и электрофоретическая подвижность. 46. Уравнения Гельмгольца – Смолуховского. Условиях его применимости. 47. Электрофоретическая подвижность и её связь с дзета- потенциалом. 48. Электроосмос. 49. Поверхностная проводимость и её влияние на потенциал течения. 50. Коэффициент эффективности диафрагмы и его вычисление. 51. Особенности электрокинетических явлений в наноразмерных капиллярах. 52. Энергия взаимодействия сферических наночастиц. 53. Уравнения для расчета энергии притяжения и энергии отталкивания сферических наночастиц. 54. Структурная составляющая расклинивающего давления. 55. Составляющие поверхностных сил в классической теории ДЛФО. Их характеристика. 56. Электростатическая составляющая расклинивающего давления. Её зависимость от расстояния в области низких потенциалов. 57. Энергия электростатического отталкивания в области низких и больших значениях потенциалов. 58. Энергия молекулярного притягивания на примере взаимодействия плоских пластин и наночастиц. 59. Молекулярная составляющая расклинивающего давления. Ее расчет для модели плоских пластин и сферических наночастиц. 60. Теория ДЛФО. Энергия взаимодействия для плоских пластин и сферических наночастиц в зависимости от расстояния. 61. Кривая потенциальной энергии для дисперсных наносистем с разным характером устойчивости. 62. Адсорбционно-сольватный и структурно-механический факторы устойчивости наносистем. 63. Стабилизация лиофобных нанодисперсных систем. Коллоидная защита. 64. Энтропийный фактор устойчивости наносистем. 65. Устойчивость лиофобных наносистем. Теория устойчивости ДЛФО. 67. Потенциальная кривая взаимодействия наночастиц. Взаимодействие частиц в первичном и вторичном минимумах. 68. Факторы стабилизации наносистем. 69. Влияние электролитов на поверхностные силы и устойчивость наносистем. 70. Влияние ПАВ на поверхностные силы и устойчивость лиофобных наносистем. 71. Поверхностные силы в коллоидных нанодисперсных системах. Их составляющие.
Задачи
Тема: адгезия наночастиц
23-32. Вычислить силу адгезии наночастицы жидкости к плоской поверхности твёрдого материла, зная константу Гамакера А двух данных фаз, радиус частицы r и величину зазора h между частицей и поверхностью, указанные в следующей таблице (для своего номера задачи):
Приложение 1. Уравнения коллоидной химии наночастиц
Приложение 2. Примеры решения задач
Пример 1. (Тема: распределение частиц по размерам) В образце наночастиц кремния Si найдено приблизительно нормальное распределение по размерам, со средним диаметром` х = 8.0 нм и со стандартным отклонением s = 1.9 нм. Определить долю числа частиц, диаметры которых больше 10 нм. Решение. Вычислим аргумент z стандартной функции Гаусса, приняв m =` х = 8.0 нм и s = 1.9 нм: z = (x – m)/ s = (10 нм – 8.0 нм)/(1.9 нм) = 1.05. По графику стандартной кумулятивной вероятности (рис. 1 в приложении 1) найдем F (1.05) = 0.85. Это – доля частиц, диаметр которых меньше или равен 10 нм. Так как доля частиц во всем диапазоне диаметров равна 1, то доля частиц с диаметрами больше 10 нм равна 1 – F (1.05) = 1 – 0.85 = 0.15.
Пример 2. (Тема: устойчивость нанодисперсных систем) Рассчитать энергию взаимодействия пары сферических частиц гидрозоля серебра с одинаковыми радиусами 32 нм, находящихся на расстоянии между их поверхностями h = 10 нм по следующим данным: константа Гамакера A * = 1·10–19 Дж, параметр Дебая i = 1·108 м–1, jd = 40 мВ, относительная диэлектрическая проницаемость e r = 80. Решение. Потенциальная энергия взаимодействия двух шарообразных частиц равна:
= 1.2·10–19 Дж.
Пример 3. (Тема: электрокинетические свойства наночастиц) Вычислить дзета-потенциал полистирольного латекса с радиусом монодисперсных частиц 61.0 нм, для которых обнаружена электрофоретическая подвижность 3.04·10–8 м2/(В·с) при 23 °С в водной среде с ионной силой 0.01 моль/л, вязкостью 0.894 мПа·с и относительной диэлектрической проницаемостью 78.5. Решение. Ответ следует из уравнения Генри. Чтобы воспользоваться им, вычислим сначала параметр ia: ia = (Ионная сила здесь переведена в СИ, 0.01 моль/л = 0.01 моль/0.001 м3 = 10 моль/м3). Затем вычислим функцию Генри по формуле Охсима:
В заключение, вычисляем по уравнению Генри:
Приложение 3. Единицы физических величин
Физическая величина – это произведение численного значения (числа) и единицы измерения. В СИ (официальное название: Le Système International d'Unités) определены семь основных единиц измерения и две дополнительные (таблица 1.1). Все остальные физические величины выводятся из основных с помощью умножения или деления в соответствии с физическими законами (формулами). Например, линейная скорость движения определяется уравнением v = dl/d t. Она имеет размерность (длина/время) и единицу измерения СИ (производную от основных единиц СИ) м/с. Некоторые из производных единиц имеют собственные наименования и обозначения (таблица 1.2). Для удобного обращения с большими или малыми численными значениями, в СИ применяются стандартные десятичные приставки, определяющие кратные и дольные десятичные производные. (Наиболее употребимые из них перечислены в табл. 1.3). Например, 1 нанометр (обозначается 1 нм) означает 10–9 долю метра, то есть 1 нм = 10–9 м. 1 миллипаскаль (1 мПа) означает 10–3 паскаля. Основная единица массы “килограмм” уже имеет приставку кило-. В этом случае любые другие десятичные производные образуются от десятичной производной “грамм”. Например, 1 миллиграмм, 1 мг, означает 10–3 г или 10–6 кг. (Грамм является основной единицей массы в СГС и десятичной дольной единицей СИ). Если над единицей измерения с десятичной приставкой производится математическое действие, например возведение в степень, то действие относится ко всему обозначению. Например, 1 дм3 означает 1 (дм)3, но не 1 д(м)3.
Таблица 1.1 Основные и дополнительные единицы СИ
* определение СИ: " Моль – это количество вещества, в котором содержится столько названных единиц, сколько содержится атомов в 0.012 кг изотопа 12С. " Можно сказать иначе, моль – это количество вещества, в котором содержится N A (число Авогадро) единиц вещества, которые должны быть ясно указаны. Например, в качестве единиц вещества могут рассматриваться формульные единицы AlCl3, 1/3AlCl3, ионы, электроны, мицеллы, частицы лиофобного золя, аэрозоля, эмульсии и т.д.
Табл. 1.2 Некоторые производные единицы СИ, имеющие собственные наименования
Таблица 1.3 Некоторые десятичные (дольные и кратные) приставки к единицам СИ
Согласно грамматическим правилам СИ, обозначение десятичной приставки и обозначение исходной единицы пишутся слитно и не сопровождаются точкой как указанием на сокращение наименования, однако знак пунктуации должен стоять, если этого требуют грамматические правила текста, в котором обозначение встречается. Например, если обозначение сантиметра, см, стоит в конце предложения, то точка должна стоять как обычно, см. Произведение двух разных единиц может быть записано тремя следующими способами (на примере вязкости): Па×с, Па·с, Па с (с пробелом между множителями). Отношение двух единиц может быть записано либо через дробь (например, Н/м), либо как произведение тремя способами: Н×м–1, Н·м–1 и Н м–1. Отношение трёх и более единиц измерения должно записываться в соответствии с обычными правилами математики (не допускается применение трёхэтажных дробей, знаменатель должен быть ясно определён, при необходимости с применением скобок). СИ является рекомендуемой и наиболее удобной системой единиц в теоретических вычислениях и в коммуникациях (передаче информации) в области точных наук. Однако во многих частных случаях удобным оказывается использование других единиц измерения. Например, при экспериментальных исследованиях с использованием высоких давлений удобно применять единицу измерения “бар”, а при использовании вакуума – “миллиметр ртутного столба” (аналогично тому, как при исчислении возраста человека используются не секунды или гигасекунды, а годы, тогда как для аналогичных целей в социальной истории применяются столетия). По определениям СИ, некоторые из таких единиц допускаются для “временного” применения, и применяются фактически (см. таблицу 1.4). Многие единицы из прошлой практики не рекомендованы к применению и, фактически, почти не применяются в современных измерениях, однако их так же полезно знать, так как многие источники информации (энциклопедии, справочники, другие публикации) используют их. Например, в большинстве справочных изданий по физической химии вязкость жидкостей указывается в сантипуазах, а не в единицах СИ Па·с. Важнейшие из таких единиц перечислены в табл. 1.5.
Табл. 1.4 Единицы измерения не входящие в СИ, но используемые наряду с
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 215; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.15.164.56 (0.019 с.) |



 .
.
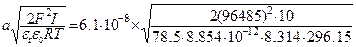 =20.12.
=20.12. = 1.35.
= 1.35. = 0.0434 В = 43.4 мВ.
= 0.0434 В = 43.4 мВ.


