Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Обробка експериментальних данихСодержание книги
Поиск на нашем сайте
3. Обробка експериментальних даних 3.1. Основні закономірності в рентгеноелектронних спектрах 3.1.1 Елементний склад
Використовуючи рентгеноелектронні спектри, можна виконувати елементний аналіз речовини: наявність певного елемента виявляється по наявності лінії, що відповідає його К- (або іншої внутрішньої) оболонці. Так, наприклад, кисень має лінію, пов’язану з 1s-електронами в області ~530 - 534 еВ, атом фтору ~ 684 - 686 еВ. Не зважаючи на наявність деякого розкиду в енергетичному положенні 1s-рівня елементу (± 5 еВ) в різних хімічних сполуках, але різниця енергій ls-ліній сусідніх елементів набагато більша цього розкиду. Наприклад, у кисня й фтора це ~ 150 еВ. Отже, величини енергії зв’язку можна використовувати для визначення якісного складу матеріалу. Експериментальні значення енергії зв’язку для ряду хімічних елементів наведено в табл. 1.
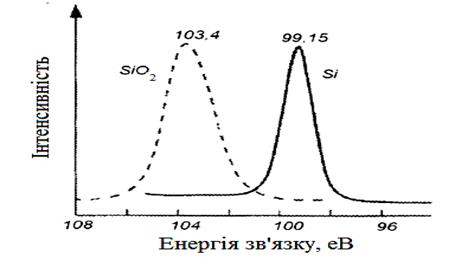
3.1.2. Хімічний зсув Незважаючи на сталість енергії остовних рівнів атома, в різних речовинах є певна різниця в енергіях зв'язку для даного атома при переході від однієї речовини до іншої. Як випливає з експериментальних даних, енергія зв'язку Езв електронів остову дещо змінюється при зміні характеру хімічного оточення атома, спектр якого вивчається. Будь-які зміни в хімічному оточенні елемента будуть впливати на просторовий перерозподіл заряду валентних електронів даного атома й викликатимуть зміни потенціалу, помітні для внутрішнього електрона. Зміни енергії зв'язку для електронного рівня одного й того ж самого елементу в різних сполуках прийнято називати хімічним зсувом. Зсув енергії внутрішніх електронів в залежності від хімічного оточення продемонстрований на рис. 7 для лінії Si 2p. Виміряна енергія зв’язку Si 2p "зміщується" більш ніж на 4 еВ при переході від Si до SiО2.
Рисунок 7 – Хімічний зсув енергії зв’язку лінії Si 2p в кремнії та його оксиді.
Зсув енергії рівня зазвичай вимірюється щодо вільного елементу. Середня точність експериментальних значень Езв ~ ± (0,1-0,2) еВ для твердих тіл і близько (± 0,04) еВ для газів. Для ілюстрації залежності енергії зв'язку електрона в атомі від хімічного оточення часто використовують рентгеноелектронний 1s-спектр вуглецю в трифторацетаті (див. рис. 8).
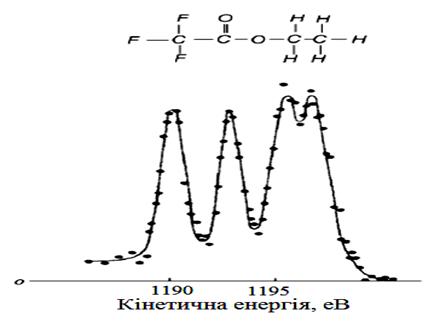
Рисунок 8 – Ретгеноелектронний С 1s-спектр в трифторацетаті.
Чотири максимуми C1s спектру майже рівної інтенсивності представляють чотири типи оточення атомів вуглецю в цій молекулі: С-F, С-О, С=О, С-Н.
|
|||||
|
Последнее изменение этой страницы: 2024-06-27; просмотров: 7; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.217.190.139 (0.008 с.) |