
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Ацетилен пропускають через амонійний розчин монохлориду міді.Содержание книги
Поиск на нашем сайте
Спостереження:
Рівняння реакції:
Дослід 6. Горіння ацетилену Ацетилен збирають у циліндр, заповнений водою, методом витіснен-ня. Зібраний ацетилен підпалюють.
Спостереження: Рівняння реакції: Висновок: Техніка безпеки
1. Всі досліди проводити у витяжній шафі. 2. При попаданні бромної води на шкіру уражене місце промити аміачним розчином. 3. Висушування ацетиленіду срібла проводити у захисних окулярах у витяжній шафі з опущеним захисним склом, оскільки висушений продукт вибухає.
Контрольні запитання та завдання
1. Запропонуйте метод добування пропіну із ацетилену. 2. За допомогою яких якісних реакцій можна відрізнити 1-бутин від 2-бутину? 3. За якими якісними реакціями можна відрізнити метилацетилен від метилетилену? Наведіть рівняння реакцій. 4. Наведіть рівняння реакцій взаємодії етилацетилену з воднем, бромом, амідом натрію, водою в умовах реакції Кучерова. 5. Які речовини утворюються при окисненні 1-пентину? Лабораторна робота № 5
Тема: Хімічні властивості алкілгалогенідів
Мета роботи: Вивчити хімічні властивості алкілгалогенідів, провести відповідні хімічні досліди. Тривалість виконання: 4 год.
Теоретична частина
Найважливішою властивістю алкілгалогенідів є рухливість атома га-логену, характерними реакціями для них є реакції нуклеофільного замі-щення (SN) та відщеплення (елімінування, Е). В залежності від будови галогенопохідного реакції заміщення можуть відбуватися за механізмом SN1 (третинні галогенопохідні) або SN2 (переважно первинні галогенопо-хідні). При гідролізі (реакція SN) дигалогенопохідних та тригалогенопо-хідних утворюються відповідно альдегіди (кетони) і кислоти. В реакціях елімінування відбувається відщеплення галогеноводнів (згідно правила Зайцева) і утворення відповідних алкенів [1, с.281-308].
Експериментальна частина
Дослід 1. Заміщення галогену на гідроксил дією лугу До 0,5 мл хлороформу в пробірці додають 2 мл 10 %-го розчину гідроксиду натрію та обережно нагрівають суміш до початку кипіння, безперервно збовтуючи. Суміш охолоджують, зливають частину водного шару в іншу пробірку. До злитого розчину додають азотної кислоти до кислої реакції та доливають кілька крапель розчину нітрату срібла.
Спостереження:
Рівняння реакції:
Дослід 2. Дія спиртового розчину лугу на етилбромід (Дослід проводити у витяжній шафі!)
виділяється, пропускають в окремі пробірки з бромною водою та 0,5 %-им розчином перманганату калію (досліди 3 та 4). Спостереження:
Рівняння реакції:
Дослід 3. Взаємодія продукту реакції з бромною водою Газ, який виділяється в досліді 2 пропускають в пробірку з бромною водою. (Дослід проводити у витяжній шафі!) Спостереження:
Рівняння реакції:
Дослід 4. Взаємодія продукту реакції з розчином перманганату калію Газ, який виділяється в досліді 2, пропускають в пробірку з розчи-ном перманганату калію. Спостереження:
Рівняння реакції:
Дослід 5. Взаємодія продукту реакції з нітратом срібла Після припинення нагрівання пробірки в досліді 2 розчин в пробірці підкислюють азотною кислотою і додають краплю нітрату срібла.
Спостереження:
Рівняння реакції:
Висновок: Техніка безпеки
1. Нагрівати суміш хлороформу з розчином лугу потрібно безперевно струшуючи. Отвір пробірки направляти в бік від себе і студентів, які працюють поряд. 2. При попаданні розчину лугу на шкіру промити уражене місце великою кількістю води та нейтралізувати 1 %-им розчином оцтової кислоти. 4. При попаданні кислоти на шкіру уражене місце промити великою кількістю води та нейтралізувати 1 %-им розчином гідрокарбонату натрію. 3. Дослід з бромною водою проводити у витяжній шафі. При попаданні бромної води на шкіру промити уражене місце розчином аміаку. Контрольні запитання та завдання
1. Як одержати 2,2-дибромопропан із первинного пропілброміду? 2. Яка речовина утворюється при гідролізі 2,2-дибромопентану? 3. Як змінюється активність алкілгалогенідів зі збільшенням розгалуженості вуглецевого ланцюга? 4. Наведіть механізм взаємодії 2-бромо-2-метилбутану та 2-бромобутану з водним розчином NaOH.
Лабораторна робота №6 Тема: Хімічні властивості спиртів Мета роботи: Вивчити хімічні властивості спиртів ( одноатомних, двохатомних та трьохатомних), провести хімічні досліди, вивчити якісні реакції. Тривалість виконання: 4 год.
Теоретична частина
Властивості спиртів пов’язані з наявністю в молекулі функціональ-ної групи - ОН. Спирти проявляють слабкокислотні властивості. Взаємо-дія етилового спирту з натрієм (дослід 2) підтверджує ці властивості. Цей дослід дає змогу зробити також висновок про те, що спирти є слабшими кислотами, ніж вода. Двохатомні та трьохатомні спирти є сильнішими кислотами і тому можуть утворювати солі з основами. Спирти окисню-ються до карбонільних сполук (первинні спирти можна окиснити до кис-лот). Для спиртів також характерні реакції нуклеофільного заміщення. Слід звернути увагу на те, що гідроксильна група заміщується тільки після протонування (через проміжне утворення оксонієвої солі). Для первинних спиртів реалізується механізм SN2, а для третинних - SN1. Утворення спир-тами оксонієвих солей свідчить про те, що спирти здатні проявляти також властивості основ. Спирти за рахунок неподіленої пари електронів атома оксигену групи ОН можуть бути нуклеофілами (прикладом такої реакцій-ної здатності є реакція естерифікації). [1, c.309-356].
Експериментальна частина
Дослід 1. Виявлення води у спирті У пробірку наливають 1 мл етилового спирту і додають декілька кристаликів безводного сульфату міді. Які відбуваються зміни?
Спостереження:
Рівняння реакції:
Дослід 2. Відношення спиртів до індикаторів У дві пробірки поміщають по 3 краплі води і додають в одну пробір-ку кілька краплин етилового спирту в іншу - ізоамілового. Перевіряють се-редовище за допомогою індикатора (універсальний індикатор, фенолфта-леїн). Спостереження:
Дослід 3. Утворення етилату натрію та його гідроліз У пробірку наливають 2 мл етанолу, додають шматочок очищеного металічного натрію і закривають пробкою з газовідвідною трубкою. Після повного розчинення металічного натрію утворений алкоголят розкладають водою. Додають у розчин фенолфталеїн і спостерігають за зміною кольору.
Спостереження:
Рівняння реакцій:
Дослід 4. Окиснення етанолу перманганатом калію Наливають в пробірку 1 мл етанолу, додають 1 мл розчину перман-ганату калію і нагрівають. Альдегід, що утворюється, розпізнають за ха-рактерним запахом.
Спостереження:
Рівняння реакції:
Дослід 5. Утворення гліколяту та гліцерату міді У три окремі пробірки наливають по 2 мл 10 %-го розчину лугу і додають кілька крапель розчину сульфату міді. Утворюється осад гідрок-сиду міді (II). До отриманого осаду додають в першу пробірку кілька кра-пель етилового спирту, в другу – етиленгліколю і в третю – гліцерину. Реакційну суміш в пробірках енергійно струшують.
Спостереження:
Рівняння реакцій:
Дослід 6. Утворення ізопентилацетату (ізоамілацетату) Змішують у пробірці 2 мл концентрованої оцтової кислоти, 2 мл ізоамілового спирту та 0,5 мл концентрованої сірчаної кислоти, кидають шматочки невипаленої порцеляни (центри кипіння). Суміш перемішують та обережно нагрівають, весь час струшуючи. Продукт реакції виливають у пробірку з холодною водою. Ізоамілацетат спливає на поверхню води, пахне грушевою есенцією.
Спостереження:
Рівняння реакції: Висновок:
Техніка безпеки
1. Для досліду 3 потрібно взяти суху пробірку (усі реагенти отримують у лаборанта). Додавати воду до реакційної суміші лише тоді, коли весь натрій прореагує. 2. При попаданні розчину лугу на шкіру уражене місце промити великою кількістю води та нейтралізувати 1 %-им розчином оцтової кислоти. 3. Нагрівати суміш оцтової кислоти, ізоамілового спирту та концентрованої сірчаної кислоти безперевно струшуючи. Отвір пробірки направляти в бік від себе і студен-тів, які працюють поряд. Після виконання цього досліду реакційну суміш з залишка-ми ізоамілацетату вилити у спеціально відведений посуд (в раковину не виливати)! 4. При попаданні кислоти на шкіру уражене місце промити великою кількістю води та нейтралізувати 1 %-им розчином гідрокарбонату натрію. Контрольні запитання та завдання
1. Отримайте за допомогою реакції Гріньяра пропіловий, ізобутиловий, трет. бути-ловий спирти. 2. Напишіть приклади реакцій естерифікації. Наведіть механізм реакції. 3. Охарактеризуйте хімічні властивості алілового та пропаргілового спиртів. 4. Наведіть відмінності у реакційній здатності одноатомних та трьохатомних спиртів. 5. Наведіть механізм дегідратації 2-бутанолу. 6. Наведіть механізм пінакон-пінаколінового перегрупування.
Лабораторна робота №7
|
|||||||||
|
Последнее изменение этой страницы: 2016-04-18; просмотров: 465; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.146.107.152 (0.011 с.) |

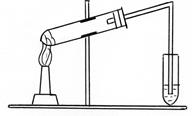 Рис.6
Рис.6



