Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кровоснабжение головного и спинного мозгаСодержание книги
Поиск на нашем сайте
Нормальная деятельность ЦНС наитеснейшим образом связана с ее постоянно адекватным и хорошо регулируемым кровоснабжением. Высокая чувствительность нервной ткани к изменениям, в первую очередь POj, РСОз и содержания глюкозы, объясняет, почему нарушения функции ЦНС чаще всего связаны с цереброваскулярной патологией. Кровоснабжение головного мозга. Головной мозг человека даже в условиях функционального покоя характеризуется непрерывно протекающими 336 энергоемкими процессами аэробного характера, требующими высокого потреблен ия моз говой тканью кислорода (3—4 мл/100 г/мин) и глюкозы (У мг/100 г/миьф Известно, что нервная ткань практически не ооладает ни субстратом для анаэробных окислительных процессов, ни запасами кислорода, а, значит, для нормального функционирования мозга необходима высокая интенсивность его кровоснабжения. В связи с этим головной мозг, в среднем имеющий массу 1400—1500 г (примерно 2 % от общей массы тела), в состоянии функционального покоя получае т около 750 мл/ми н кр ови, что соответствует примерно 15 % общего сердечного выброса. Ан-к-р.мияд-гкорпе ть кровот ока при этих условиях составляет в ср еднем 50— 65 мл/100 г/мин, однако следует отметить, что серое иеше ст- вб~об еспечивается к ровью интенсивнее, чем белое, что связано с его более высокой клеточной активностью. У детей 1-го года жизни величина суммарного мозгового кровотока иа 50 — 55 % больше, а в старческом возрасте примерно на 20 % меньше, чем у человека в зрелом возрасте. В функциональном отношении в сосудистой системе головного мозга можно выделить две взаимосвязанные гемодинамические подсистемы: а) макроциркуляция, образующая русло для общего суммарного мозгового кровотока; б) микроциркуляция, структурно-функциональной единицей которой в головном мозге является сосудистый модуль — относительно автономный в гемодинамическом отношении комплекс микрососудов, снабжающий кровью отдельные функционально специализированные популяции нервных клеток. Сосуды макроциркуляции располагаются практически на поверхности мозга и характеризуются многочисленными анастомозами. В отличие от них в сосудах микроциркуляции мозга отмечается практически полное отсутствие анастомозов, поэтому ишемия нервной ткани, вызванная тромбозом или стойким спазмом внутримозговых микрососудов, как правило, не компенсируется и сопровождается нарушением тех функций организма, которые регулировались обескровленным нервным центром. Регуляция мозгового кровообращения. Главной целью регуляции мозгового кровообращения является гемодинамическое обеспечение оптимальных физико-химических условий для нормального функционирования мозга. При этом в норме должны соблюдаться следующие условия: а) минимизация отклонений физического и химического гомеостаза внутренней среды мозга при сдвигах системной гемодинамики и ликвородинамики; б) минимизация отклонений физического и химического гомеостаза внутренней среды мозга при изменениях газового состава крови и ЦСЖ; в) перераспределение кровотока между областями мозга; г) адекватное кровоснабжение функционально специализированных нейронных ансамблей при изменении их метаболической активности. Эти условия создаются путем реализации основных сосудистых регуляторных процессов в системе мозгового кровообращения, краткая характеристика которых представлена в табл. 6.2. Снижение_интенсмвнос.ти кровоснабжения головного мозга чревато развитием дефицита кисло рода и гдюкозы, что может привести к нарушениям деятельности мозга. Однако в здоровом организме благодаря надежным механизмам ауторегуляции мозгового кровотока питание мозга остается практически неизменным при падении среднего АД вплоть до 50 мм рт. ст. Мозг расположен в ригидном костном образовании — черепе (исключение составляют дети грудного возраста, у которых имеются роднички, придающие некоторую подвижность стенкам черепной коробки). Поскольку в полости черепа, помимо мозгового вещества, содержатся кровь и ЦСЖ, являющиеся практически несжимаемыми средами, регуляция кровенапол- Таблица 6.2. Основные регуляторные процессы в системе мозгового кровообращения
нения мозга тесно связана с регуляцией в нем объема ЦСЖ. Изменение количества крови в сосудистой системе мозга сопровождается противонаправленным изменением количества ликвора и наоборот. Благодаря этому их общий объем в полости черепа остается постоянным. При избыточности же кровоснабжения мозга может произойти излишняя гидрата- цйптервнои^тканй’с последующим развитием отека мозга. Основной причино й из быточности кровоснабжения головного мозга_может служить увеличение перфузионного давления в сосудах мозга, вызванное повышением среднего АД. В норме вследствие развития ауторегуляторных сосудистых реакций мозг предохранен от избыточности кровенаполнения при повышении давления вплоть до 160— 170 мм рт. ст. Основным механизмом развития ауторегуляторных реакций мозговых сосудов при этом считается миогенный. Помимо способности к развитию ауторегуляторных сосудистых реакций, предохранение головного мозга от высокого перфузионного давления и избыточности пульсации кровотока осуществляется и за счет особенностей ангиоархитектоники сосудистой системы мозга. В частности, эту функцию достаточно эффективно выполняют многочисленные изгибы (сифоны) по ходу сосудистого русла, которые способствуют сглаживанию пульсирующего характера кровотока. В активно работающем мозге возникает потребность в увеличении интенсивности кровоснабжения. Благодаря явлению функциональной- (рабоч ей) ги перемии такая возросшая'потребность мозга в питании полностью удовлетворяется." Объясняется это специфическими особенностями работы Мбзга И морфрфункциональной организации мозгового кровообращения. Являясь регулятором всех соматических и висцеральных функций, и главным органом взаимодействия организма с внешней средой, мозг активен постоянно,‘тто общий уровень его активности и степень акхивноста отдельных областей, зон и даже микроучастков мозга различны. При повышении активности всего организма (усиленная физическая работа, эмоциональный стресс и др.) суммарный мозговой кровоток может возрасти примерно на 20—25 %, однако эта гиперемия не оказывает повреждающего механического действия на окружающие ткани, поскольку пиальные сосуды расположены на поверхности больших полушарий в сравнительно широких ликворных каналах и обладают свободным пространством для такого кровенаполнения. В свою очередь многообразные текущие виды деятельности человека характеризуются развитием процесса активации в строго соответствующих нервных центрах, где и формируются доминантные очаги, клеточные элементы которых увеличивают свою метаболическую активность и, следовательно, нуждаются в усиленном кровоснабжении. В этих случаях нет необходимости в увеличении всего мозгового кровотока, а лишь требуется его внутримозговое перераспределение в пользу нуждающихся участков или даже микроучастков мозга. Эта потребность реализуется путем развития локальной функциональной гиперемии только в активированных отделах мозга. Ведущая роль в развитии локальной функциональной гиперемии в мозге отводится местным факторам регуляции сосудистого тонуса, приводящим к дилатации мозговых микрососудов и тем самым создающим условия для увеличения интенсивности кровотока. Совокупность этих факторов подразделяют на 2 группы в зависимости от их расположения по отношению к ГМК сосудистой стенки. Первую группу образуют факторы, действующие на сосудистую стенку со стороны окружающих сосуд тканей (факторы экстравазарного происхождения), к которьгм относятся: а) уровень осмолярности периваскулярного пространства; б) величина pH, связанная с изменениями РО2, РСО2 и концентрации кислых метаболитов в интерстициальном пространстве; в) биологически активные вещества и нейропептиды тканевого происхождения; г) оксид азота нейроглиального происхождения. Вторую группу составляют факторы интравазарного происхождения, порождаемые физико-химическими характеристиками кровотока, изменениями газового состава крови и содержания в ней биологически активных веществ. Сосудорасширяющее действие факторов интравазарного происхождения опосредуется через эндотелиальные клетки сосудистой стенки, которые путем выделения оксида азота, простациклина и фактора гиперполяризации снижают сократительную способность ГМК. Методы исследования мозгового кровообращения. К непрямым методам оценки кровообращения в мозге, позволяющим лишь косвенно судить о состоянии мозговой гемодинамики, относятся методы оценки кровообращения в сетчатке глаза (офтальмотонометрия, офтальмодинамометрия, окулосфигмография) и реоэнцефалография. К группе методов, выявляющих качественные изменения направленности таких характеристик мозгового кровообращения, как ширина просвета сосудов, объем крови в них и скорость кровотока, однако не позволяющих оценивать эти изменения количественно, относятся церебральная рентгеноконтрастная ангиография, каротидная ангиография и вертебральная ангиография. Современные неинвазивные количественные методы измерения мозгового кровотока подразделяют на 3 группы: методы измерения общего кровотока в мозге, кровотока в небольших областях мозга и локального мозгового кровотока в глубинных структурах мозга. Среди этих методов наиболее доступными, информативными и относительно простыми в исполнении являются различные варианты ультразвуковой допплерографии (каротидная допплерография, вертебральная допплерография, транскраниальная допплерография и допплеросонография). Высокой информативностью в оценке микрогемодинамики в корковых и глубинных структурах мозга, цереброваскулярного резерва обладают радиоизотопный метод с применением изотопов, не диффундирующих из сосудистого русла в ткань мозга, методы однофотонной эмиссионной компьютерной томографии, магнитно-резонансной томографии, позитронной эмиссионной томографии (ПЭТ). Особую ценность при исследовании цереброваскулярного резерва представляет ПЭТ, который одновременно с определением величины кровотока в мозговых структурах позволяет установить уровень клеточного метаболизма кислорода и глюкозы, т.е. оценить условия циркуляторно-метаболического гомеостаза в мозговой ткани. При определении цереброваскулярного резерва с помощью ПЭТ чаще всего используют функциональный тест в виде ингаляционной пробы с вдыханием в течение 1—2 мин газовой смеси, содержащей 5—7 % СО2. Этот функциональный тест активирует механизмы вазодилататорной регуляции мозговых сосудов, ответственные за адекватное метаболическое обеспечение деятельности мозга. Кровоснабжение спинного мозга осуществляется корешковыми артериями, берущими начало главным образом от подключичных и позвоночных отделов аорты. Конструкция кровоснабжения ткани спинного мозга характеризуется сегментарностью. Внутримозговые артерии, отходящие от поверхностной сети вглубь мозга, ветвятся и образуют капиллярную сеть, которую подразделяют на 3 группы: 1) капилляры, идущие в продольной плоскости параллельно нервным волокнам и питающие белое вещество; 2) капилляры желатинозной субстанции, образующие продольные сети; 3) капилляры серого вещества спинного мозга. Капилляры спинного мозга, аналогично капиллярам головного мозга, имеют стенки, состоящие из плотного слоя эндотелиальных клеток, и тесно контактируют с сосудистыми ножками глиальных клеток. Это обстоятельство свидетельствует о функционировании гематоэнцефалического барьера и на уровне спинного мозга. Общая объемная скорость кровотока в спинном мозге у человека в условиях функционального покоя составляет в среднем 30—32 мл/100 г/мин. Однако распределение кровотока по различным отделам спинного мозга и в пределах каждого из сегментов неодинаково. Наибольшая объемная скорость кровотока наблюдается в шейном (в среднем 34 мл/100 г/мин) и поясничном (в среднем 34 мл/100 г/мин) отделах, тогда как в грудном отделе кровоток наименьший и составляет в среднем 29 мл/100 г/мин. Во всех сегментах спинного мозга кровоснабжение серого вещества выше, чем белого вещества, что объясняется более высокими энергоемкими процессами, протекающими в соме нервных клеток. При изменениях системного АД кровоток в спинном мозге благодаря механизмам его ауторегуляции меняется незначительно. Верхняя граница ауторегуляции кровотока достигает 170 мм рт. ст. Сведения относительно значений нижней границы ауторегуляции кровотока в спинном мозге отсутствуют, однако можно предположить, что она в спинном мозге ниже, чем в головном, поскольку нейроны спинного мозга менее чувствительны к недостаточности питания. Легочное кровообращение Важнейшей особенностью организации кровоснабжения легких является ее двухкомпонентный характер, поскольку легкие получают кровь из сосудов малого круга кровообращения и бронхиальных сосудов большого круга кровообращения. Функциональное назначение сосудистой системы малого круга кровообращения состоит в обеспечении газообменной функции, тогда как бронхиальные сосуды удовлетворяют собственные метаболические потребности легочной ткани. Капилляры легких образуют на поверхности альвеол очень густую сеть, и при этом на одну альвеолу приходится несколько капилляров. В связи с тем что стенки альвеол и капилляров тесно контактируют, образуя как бы единую альвеолярно-капиллярную мембрану, создаются наиболее благоприятные условия для эффективных вентиляционно-перфузионных взаимоотношений. В условиях функционального покоя у человека капиллярная кровь находится в контакте с альвеолярным воздухом в течение примерно 0,75 с. При тяжелой физической работе продолжительность контакта укорачивается и составляет в среднем 0,35 с. В результате слияния капилляров образуются характерные для легочной сосудистой системы безмышечные посткапиллярные венулы, трансформирующиеся в венулы мышечного типа и далее в легочные вены. Особенностью сосудов венозного отдела являются их тонкостенность и слабая выраженность ГМК. Структурные особенности легочных сосудов, в частности артерий, определяют большую растяжимость сосудистого русла, что создает условия для более низкого сопротивления (приблизительно в 10 раз меньше, чем в системе большого круга кровообращения), и, следовательно, более низкого кровяного давления. В связи с этим система малого круга кровообращения относится к области низкого давления. Давление в легочной артерии составляет в среднем 15—25 мм рт. ст., а в венах — 6—8 мм рт. ст. Градиент давления равен примерно 9—17 мм рт. ст., т.е. значительно меньше, чем в большом круге кровообращения. Несмотря на это, повышение системного АД или же значительное увеличение кровотока (при активной физической работе) существенно не влияет на трансмуральное давление в легочных сосудах из-за их большей растяжимости. Большая растяжимость легочных сосудов определяет еще одну важную функциональную особенность этого региона, заключающуюся в способности депонировать кровь и тем самым предохранять легочную ткань от отека при увеличении минутного объема кровотока. Распределение кровотока в легких характеризуется неравномерностью кровоснабжения верхних и нижних долей, так как низкое внутрисосудистое давление определяет высокую зависимость легочного кровотока от гидростатического давления. Так, в вертикальном положении человека верхушки легкого расположены выше основания легочной артерии, что практически уравнивает АД в верхних долях легких с гидростатическим давлением. По этой причине капилляры верхних долей слабо перфузируются, тогда как в нижних долях благодаря суммированию АД с гидростатическим давлением кровоснабжение намного обильнее. Описанная особенность легочного кровообращения играет важную роль в установлении неодинаковых перфузионно-вентиляционных отношений в различных долях легкого. Интенсивность кровоснабжения легких зависит от циклических изменений плеврального и альвеолярного давления в различные фазы дыхательного цикла. Во время вдоха, когда плевральное и альвеолярное давление уменьшается, происходит пассивное расширение крупных внелегочных и внутрилегочных сосудов, сопротивление сосудистого русла дополнительно снижается и интенсивность кровоснабжения легких в фазу вдоха увеличивается. , Регуляция легочного кровообращения. Местная регуляция легочного кровотока в основном представлена метаболическими факторами, ведущая роль среди которых принадлежит POj и РСОг- При снижении РО2 и/или повышении РСОг происходит вазоконстрикция легочных сосудов. Нервная регуляция легочного кровотока осуществляется в основном симпатическими сосудосуживающими волокнами. Система легочного кровообращения выделяется среди всех сосудистых регионов наибольшей функциональной взаимосвязью с регуляцией гемодинамики в большом круге кровообращения. Известно, что рефлексы саморегуляции кровообращения с баро- и хеморецепторов каротидного синуса сопровождаются активными изменениями легочного кровотока. В свою очередь рецепторы сосудов малого круга кровообращения являются рефлексогенной зоной, порождающей рефлекторные изменения в сердечно-сосудистой системе. Гуморальная регуляция легочного кровообращения в значительной степени обусловлена влиянием таких биологически активных веществ, как ангиотензин II, адреналин, норадреналин, ацетилхолин, брадикинин, серотонин, гистамин, простагландины, которые вызывают свои сосудистые эффекты в зависимости от состояния эндотелия легочных сосудов. Методы исследования легочного кровообращения. Ангиография легких — рентгенологическое исследование легочных сосудов после их контрастирования. При общей ангиографии легких контрастное вещество вводят обычно в локтевую вену или в полость правого сердца. При селективной ангиографии легких контрастное вещество вводят в одну из ветвей легочного ствола. Несомненными преимуществами обладают радиоизотопные методы изучения легочного кровообращения, которые дают возможность количественной оценки кровотока в легких и его распределения по зонам легочной ткани, а также позволяют определять изменения легочного кровотока в динамике. Усовершенствование в последнее десятилетие ультразвуковых технологий в области получения изображений привело к появлению неинвазивных количественных ультразвуковых методов исследования кровообращения в легких. Кроме того, неинвазивный метод внутрисосудистого ультразвукового исследования позволяет измерить поперечное сечение легочных сосудов, анализировать их внутреннее строение, локализацию и характер поражения сосудов легких. 6.3. ЛИМФООБРАЩЕНИЕ 6.3.1. Строение лимфатической системы Лимфатическая система человека и теплокровных животных состоит из следующих образований: • лимфатических капилляров, представляющих собой замкнутые с одного конца эндотелиальные трубки, пронизывающие практически все органы и ткани; • внутриорганных сплетений посткапилляров и мелких, снабженных клапанами, лимфатических сосудов; • экстраорганных отводящих лимфатических сосудов, впадающих в главные лимфатические стволы, прерывающихся на своем пути лимфатическими узлами; • главных лимфатических протоков — грудного и правого лимфатического, впадающих в крупные вены шеи. Лимфатические капилляры и посткапилляры представляют собой часть лимфатической системы; в них под влиянием изменяющихся градиентов гидростатического и коллоидно-осмотического давлений образуется лимфа. Стенки лимфатических капилляров и посткапилляров представлены одним слоем эндотелиальных клеток, прикрепленных с помощью коллагеновых волокон к окружающим тканям. В стенке лимфатических капилляров между эндотелиальными клетками имеется большое количество пор, которые при изменении градиента давления могут открываться и закрываться. Внутри- и внеорганные лимфатические сосуды, лимфатические стволы и протоки выполняют преимущественно транспортную функцию, обеспечивая доставку образовавшейся в лимфатической системе лимфы в систему кровеносных сосудов. Лимфатические сосуды являются системой коллекторов, представляющих собой цепочки лимфангионов. Лимфангион является морфофункциональной единицей лимфатических сосудов и состоит из мышечной «манжетки», представленной спиралеобразно расположенными гладкими мышечными клетками и двух клапанов — дистального и проксимального. Крупные лимфатические сосуды конечностей и внутренних органов сливаются в грудной и правый лимфатический протоки. Из протоков лимфа поступает через правую и левую подключичную вены в общий кровоток. 6.3.2. Образование лимфы Лимфа образуется из тканевой (интерстициальная) жидкости, накапливающейся в межклеточном пространстве в результате преобладания фильтрации жидкости над реабсорбцией через стенку кровеносных капилляров. Движение жидкости из капилляров и внутрь их определяется соотношением гидростатического и осмотического давления, действующего через эндотелий капилляров. Осмотические силы стремятся удержать плазму внутри кровеносного капилляра для сохранения равновесия с противоположно направленными гидростатическими силами. Вследствие того что стенка кровеносных капилляров не является полностью непроницаемой для белков, некоторое количество белковых молекул постоянно просачивается через нее в интерстициальное пространство. Накопление белков в тканевой жидкости увеличивает ее осмотическое давление и приводит к нарушению баланса сил, контролирующих обмен жидкости через капиллярную мембрану. В результате концентрация белков в интерстициальной ткани повышается и белки по градиенту концентрации начинают поступать непосредственно в лимфатические капилляры. Кроме того, движение белков внутрь лимфатических капилляров осуществляется посредством пиноцитоза. 6.3.3. Состав лимфы В состав лимфы входят клеточные элементы, белки, липиды, низкомолекулярные органические соединения (аминокислоты, глюкоза, глицерин), электролиты. Клеточный состав лимфы представлен в основном лимфоцитами. В лимфе грудного протока их число достигает 8 109/л. Эритроциты в лимфе в норме встречаются в ограниченном количестве, но их число значительно возрастает при травмах тканей; тромбоциты в норме не определяются. Макрофаги и моноциты встречаются редко. Гранулоциты могут проникать в лимфу из очагов инфекции. Ионный состав лимфы не отличается от ионного состава плазмы крови и интерстициальной жидкости. В то же время по содержанию и составу белков и липидов лимфа значительно отличается от плазмы крови. В лимфе человека содержание белков составляет в среднем 2—3 %. Концентрация белков в лимфе зависит от скорости ее образования: увеличение поступления жидкости в организм вызывает рост объема образующейся лимфы и уменьшает концентрацию белков в ней. В лимфе в небольшом количестве содержатся все факторы свертывания, антитела и различные ферменты, имеющиеся в плазме. Холестерин и фосфолипиды находятся в лимфе в виде липопротеинов. Содержание свободных жиров, которые находятся в лимфе в виде хиломикронов, зависит от количества жиров, поступивших в лимфу из кишечника. После приема пищи в лимфе грудного протока содержится большое количество липопротеинов и липидов, всосавшихся в желудочно-кишечном тракте. Между приемами пиши содержание липидов в грудном протоке минимально. 6.3.4. Движение лимфы Скорость и объем лимфообразования определяются процессами микроциркуляции и взаимоотношением системной и лимфатической циркуляции. Так, при минутном объеме кровообращения, равном 6 л, через стенки кровеносных капилляров в организме человека фильтруется около 15 мл жидкости. Из этого количества 12 мл жидкости реабсорбируется. В интерстициальном пространстве остается 3 мл жидкости, которая в дальнейшем возвращается в кровь по лимфатическим сосудам. Если учесть, что за 1 ч в крупные лимфатические сосуды поступает 150—180 мл лимфы, а за сутки через грудной лимфатический проток проходит до 3 л лимфы, которая в дальнейшем поступает в общий кровоток, то значение возврата лимфы в кровь становится весьма ощутимым. Движение лимфы начинается с момента ее образования в лимфатических капиллярах, поэтому факторы, которые увеличивают скорость фильтрации жидкости из кровеносных капилляров, также увеличивают скорость образования и движения лимфы. Факторами, повышающими лимфообразование, являются увеличение гидростатического давления в капиллярах, возрастание общей поверхности функционирующих капилляров (при повышении функциональной активности органов), увеличение проницаемости капилляров, введение гипертонических растворов. Роль лимфообразования в механизме движения лимфы заключается в создании первоначального гидростатического давления, необходимого для перемещения лимфы из лимфатических капилляров и посткапилляров в отводящие лимфатические сосуды. В лимфатических сосудах основной силой, обеспечивающей перемещение лимфы от мест ее образования до впадения протоков в крупные вены шеи, являются ритмические сокращения лимфангионов. Лимфангионы, которые можно рассматривать как трубчатые лимфатические микросердца, имеют в своем составе все необходимые элементы для активного транспорта лимфы: развитую мышечную «манжетку» и клапаны. По мере поступления лимфы из капилляров в мелкие лимфатические сосуды происходит наполнение лимфангионов лимфой и растяжение их стенок, что приводит к возбуждению и сокращению гладких мышечных клеток мышечной «манжетки». Сокращение гладких мышц в стенке лимфангиона повышает внутри него давление до уровня, достаточного для закрытия дистального клапана и открытия проксимального. В результате происходит перемещение лимфы в следующий центрипетальный лимфангион. Заполнение лимфой проксимального лимфангиона приводит к растяжению его стенок, возбуждению и сокращению гладких мышц и перекачиванию лимфы в следующий лимфангион. Таким образом, последовательные сокра-
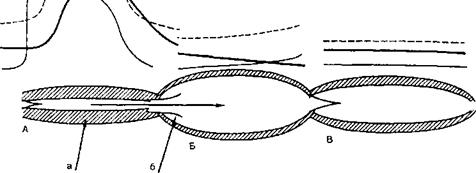
Рис. 6.16. Механизм движения лимфы по лимфатическим сосудам. А — лимфангион в фазе сокращения; Б — лимфангион в фазе заполнения; В — лимфангион в состоянии покоя; а — мышечная манжетка лимфангиона; б — клапан; 1 ~ потенциал действия миоцита лимфангиона; 2 — сокращение стенки лимфангиона; 3 — давление в просвете лимфангиона. Стрелкой показано направление движения лимфы.
щения лимфангионов приводят к перемещению порции лимфы по лимфатическим коллекторам до места их впадения в венозную систему. Работа лимфангионов напоминает деятельность сердца. Как в цикле сердца, в цикле лимфангиона имеются систола и диастола. По аналогии с гетеро- метрической саморегуляцией в сердце, сила сокращения гладких мышц лимфангиона определяется степенью их растяжения лимфой в диастолу. И наконец, как и в сердце, сокращение лимфангиона запускается и управляется одиночным потенциалом действия (рис. 6.16). Стенка лимфангионов имеет развитую иннервацию, которая в основном представлена адренергическими волокнами. Роль нервных волокон в стенке лимфангиона заключается не в инициации сокращения, а в модуляции параметров спонтанно возникающих ритмических сокращений. Кроме этого, при общем возбуждении симпатико-адреналовой системы могут происходить тонические сокращения гладких мышц лимфангионов, что приводит к повышению давления во всей системе лимфатических сосудов и быстрому поступлению в кровоток значительного количества лимфы. Гладкие мышечные клетки высокочувствительны к некоторым гормонам и биологически активным.веществам. В частности, гистамин, увеличивающий проницаемость кровеносных капилляров и приводящий тем самым к росту лимфообразования, увеличивает частоту и амплитуду сокращений гладких мышц лимфангионов. Миоциты лимфангиона реагируют также на изменения концентрации метаболитов, РО2 и повышение температуры. В организме, помимо основного механизма, транспорту лимфы по сосудам способствует ряд вспомогательных факторов. Во время вдоха усиливается отток лимфы из грудного протока в венозную систему, а при выдохе он уменьшается. Движения диафрагмы влияют на ток лимфы — периодическое сдавление и растяжение диафрагмой цистерны грудного протока усиливают заполнение ее лимфой и способствуют продвижению по грудному лимфатическому протоку. Повышение активности периодически сокращающихся мышечных органов (сердце, кишечник, скелетные мышцы) влияет не только на усиление лимфооттока, но и способствует переходу тканевой жидкости в капилляры. Сокращения мышц, окружающих лимфатические сосуды, повышают внутрилимфатическое давление и выдавливают лимфу в направлении, определяемом клапанами. При иммобилизации конечности отток лимфы ослабевает, а при активных и пассивных ее движениях — увеличивается. Ритмическое растяжение и массаж скелетных мышц способствуют не только механическому перемещению лимфы, но и усиливают собственную сократительную активность лимфангионов в этих мышцах. 6.3.5. Функции лимфатической системы Наиболее важной функцией лимфатической системы является возврат белков, электролитов и воды из интерстициального пространства в кровь. За сутки в составе лимфы в кровоток возвращается более 100 г низкомолекулярного белка, профильтровавшегося из кровеносных капилляров в интерстициальное пространство. Через лимфатическую систему переносятся многие продукты, всасывающиеся в желудочно-кишечном тракте, и прежде всего жиры. Некоторые крупномолекулярные вещества поступают в кровь исключительно по системе лимфатических сосудов. Лимфатическая система действует как транспортная система по удалению эритроцитов, оставшихся в ткани после кровотечения, а также по удалению и обезвреживанию бактерий, попавших в ткани. В реализации этой функции активную роль играют лимфатические узлы, расположенные по ходу сосудов, которые продуцируют лимфоциты и другие важнейшие факторы иммунитета. При возникновении инфекции в каких-либо частях тела региональные лимфатические узлы воспаляются в результате задержки в них бактерий или токсинов. В синусах лимфатических узлов, расположенных в корковом и мозговом слоях, содержится эффективная фильтрационная система, которая позволяет практически стерилизовать поступающую в лимфатические узлы инфицированную лимфу.
|
|||||||||||||||
|
Последнее изменение этой страницы: 2021-06-14; просмотров: 103; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.015 с.) |