
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Гуморальная регуляция деятельностиСодержание книги
Поиск на нашем сайте Сердца Изменения работы сердца наблюдаются при действии на него ряда биологически активных веществ, циркулирующих в крови. Катехоламины (адреналин^, норадреналин) увели чивают силу и учащ ают ритм перпечных сокращений, что имеет важное-биолой«£СКП£_значение. При физических нагруз ках иди. -.эмоциональном напряжен ии мозговой слой надпоч ечник ов выбрасывает в кровь большое копичггтво адренали- на, что приводит ^..усилению сердечной деятельности, крайне необходимому в данных услов иях. указанный эффект лозникает-В-результате стимуляции._катехоламинами рецепторов миокарда, вызывающей активацию.. Ферм ента аденилатцикла- зы. которая ус коряет образование 3'.5' -циклического алено зинмонофо с- Фата (UAIVHP). Он активирует фос форилазу, вызывающу ю расще пление внутримышечного гликогена ^образование глюкозы (источника энергии для сокращающегося миокарда). Помимо этого, катехоламины повышают проницаемость клеточных мембран для ионов Са2+, способствуя, с одной стороны, усилению поступления их из межклеточного пространства в клетку, а с другой — мобилизации ионов Са2+ из внутриклеточных депо. Активация аденилатциклазы отмечается в миокарде и при действии глюкагона — гормона, выделяемого А-клетками панкреатических островков, что также вызывает положительный инотропный эффект. Кардиотропный эффект других гормонов, как правило, носит не прямой, а опосредованный характер. Положительное инотропное влияние на сердце оказывают ангиотензин, кортикостероиды. Гормоны щитовидной железы увеличивают ЧСС. Интеграция механизмов регуляции Деятельности сердца Описанные регуляторные системы сердца на внутрисердечном уровне (клеточный и органный), выраженные влияния на него нервных и гуморальных факторов составляют в организме человека и животных единый механизм, обеспечивающий адекватные реакции сердца на постоянно меняющиеся условия. Для сердца, прекращение деятельности которого даже на секунды ведет к потере сознания, а при продолжающейся остановке и к гибели организма, наличие надежной системы сохранения и быстрого изменения параметров его деятельности приобретает особый смысл. Отмечая, что высокая надежность функционирования организма основана на дублировании механизмов осуществления функций, Дж. Баркрофт писал: «Меня всегда удивляет, что в организме имеется только одно сердце!». Наиболее ярко взаимодействие многоуровневого каскада регуляторных механизмов прослеживается при формировании ритма сердца. Сложившиеся представления о механизмах формирования ритма сердца состоят в следующем: ритм сердца рождается в самом органе в его специализированных структурах, обладающих способностью к автоматизму (внутрисердечный генератор ритма); автономная нервная система оказывает на ритм сердца корригирующее влияние, при котором симпатический нерв учащает сердцебиения, парасимпатический — урежает. Экспериментальным обоснованием для таких представлений явились опыты с перерезкой и искусственной стимуляцией экстракардиальных (парасимпатический и симпатический) нервов. Показано, что эффект обусловлен увели- 302 чением скорости спонтанной деполяризации клеток водителя ритма при стимуляции симпатического нерва и, наоборот, уменьшением скорости деполяризации под влиянием парасимпатического. В последние годы получены данные, позволяющие критически переосмыслить факты и представления о механизмах формирования ритма сердца. Так, классический феномен, наблюдаемый при стимуляции периферического конца блуждающего нерва, проявляющийся в урежении сердцебиений вплоть до остановки сердца, нельзя считать адекватной моделью для понимания процессов нервной регуляции ритма сердца. Прежде всего реакции резкого торможения деятельности сердца не наблюдается в процессе естественной регуляции, при которой никогда не возбуждаются сразу все эфферентные волокна блуждающего нерва, как при искусственной сверхпороговой стимуляции нерва. С другой стороны, при искусственной стимуляции нерв обычно раздражают непрерывным потоком импульсов, в естественных же условиях по нерву идут импульсы, сгруппированные в «залпы» («пачки»). Система новых научных фактов позволила сформулировать принципиально новые представления о механизме формирования ритма сердца в целостном организме: наряду с существованием внутрисердечного генератора ритма сердца имеется и генератор ритма сердца в ЦНС — в эфферентных структурах сердечного центра продолговатого мозга. Возникающие там нервные сигналы в форме «залпов» импульсов поступают к сердцу по блуждающим нервам и, взаимодействуя с внутрисердечными ритмогенными структурами, вызывают генерацию возбуждения в сердце в точном соответствии с частотой залпов (В.М. Покровский). Таким образом, по функциональному значению сигналы, приходящие из ЦНС, являются пусковыми — каждый залп импульсов сопровождается одним сокращением сердца. Факты, положенные в основу таких представлений, могут быть объединены в 2 группы. Первую группу составляют данные, полученные при искусственной стимуляции периферического конца перерезанного на шее блуждающего нерва залпами импульсов. Вторую группу представляют факты, полученные в наблюдениях, демонстрирующих возможность усвоения сердцем ритма залпов импульсов, сформированного в ЦНС. При стимуляции периферического конца перерезанного блуждающего нерва «залпами» импульсов, следовавших с постепенно возрастающей частотой, ритм сердцебиений урежается. При этом, когда нарастающая частота следования «залпов» становится равной частоте сердцебиений, наступает синхронизация вагусного и сердечного ритмов. Теперь сердце на каждый «залп» импульсов отвечает отдельным сокращением, наступающим через определенный промежуток времени. Для каждой характеристики залпа существует соответствующий диапазон, в пределах границ которого сердце воспроизводит поступающую по нерву частоту сигналов в форме залпов импульсов (рис. 6.13). Описанный феномен был исследован на многих видах животных (обезьяны, кошки, кролики, собаки, белые крысы, морские свинки, нутрии, голуби, утки, лягушки). Оказалось, что он воспроизводится у всех исследованных животных и подчиняется общим закономерностям, что свидетельствует о его общебиологической значимости. Биоэлектрические механизмы реализации феномена управления ритмом сердца изучались в экспериментах на животных с компьютерным картированием области синоатриального узла. В 64 точках регистрировали биоэлектрическую активность, и компьютер строил изохронную карту распространения возбуждения по синоатриальной области. Оказалось, что в исходном состоянии, а также при брадикар- -|гЛг'-——-—|ГЛ/'—-——^Лг>———•—|^Дг— тл------------------------------ гл------------------------------ «I--------- 1
ТУГ УГГ---------- 1
■-V Рис. 6.13. Воспроизведение сердцем ритма стимуляции блуждающего нерва залпами импульсов. а — до стимуляции нерва; б, в — соответственно верхняя и нижняя границы диапазона синхронизации. 1 — отметка стимуляции нерва залпами импульсов; 2 — электрокардиограмма, регистрируемая при помощи биполярного электрода, находящегося на конце зонда, введенного в правое предсердие (зубец Р усилен). дии, вызванной традиционным раздражением блуждающего нерва, первоначальный очаг возбуждения определялся в форме точки и располагался под одним из электродов. При феномене управления ритмом сердца, достигаемом залповой стимуляцией блуждающего нерва, очаг инициации возбуждения становился широким и охватывал не 1, а 2—11 точек. Таким образом, электрофизиологическим маркером факта воспроизведения сердцем ритма сигналов, поступающих по блуждающим нервам, явилось резкое расширение зоны одновременно возбуждающихся элементов (зоны инициации возбуждения) в области синоатриального узла. Эти факты свидетельствуют о существовании надежного общебиологического феномена, проявляющегося в том, что при поступлении к синоатриальному узлу залпов импульсов по блуждающему нерву в узле в ритме этих залпов генерируется ритм сердца. Для выяснения условий реализации обнаруженного феномена в целостном организме были созданы приемы, которые позволили наблюдать формирование ритма сердца в организме посредством сигналов, генерированных в ЦНС и переданных к сердцу по блуждающим нервам. Основой для этого послужила тесная связь центральных механизмов формирования ритма сердца и частоты дыхания (ЧД). Обычно человек и животные дышат существенно реже, нежели сокращается сердце. В то же время дыхание среди всех вегетативных функций обладает уникальной особенностью — возможностью произвольного управления. В целях создания заданной величины учашения ритма сердца взрослым людям предлагалось дышать в такт миганиям лампочки фотостимулятора, частота которых на 5—10 % превышала исходную частоту сердцебиений; через 20—30 сердечных циклов наступала синхронизация ЧД и ЧСС. При этом диапазон 304 управляемой ЧСС составил 10—20 синхронных кардиореспираторных циклов. Эти синхронные с дыханием биения сердца явились результатом сигналов, пришедших к сердцу по блуждающим нервам. В эксперименте этот факт был проанализирован у животных.Так как у животных невозможно произвольное учащение дыхания, в опытах на собаках использовали иную модель. У собак выражено учащение дыхания при перегревании. Для получения тахипноэ животных помещали в термокамеру, температуру в которой поддерживали на уровне 38 °C. Через 1,0—1,5 ч ЧД у собак достигала ЧСС, и вскоре ритмы дыхания и сердцебиения синхронизировались при частоте около 180 уд/мин. Далее в ходе опытов ЧД могла увеличиваться или уменьшаться, что приводило к синхронному изменению ЧСС. Ширина диапазона синхронной ЧСС и ЧД составила 50 в 1 мин. Если во время синхронизации сердечного и дыхательного ритмов перерезали предварительно выведенный под кожу шеи блуждающий нерв, то синхронизация прекращалась. Аналогичный эффект наблюдался при введении животному атропина, который нарушает передачу возбуждения с окончаний блуждающего нерва на сердце. Наблюдения на людях и эксперименты на животных показали, что при высокой частоте возбуждения дыхательного центра происходит вовлечение в эту ритмику и сердечных эфферентных нейронов в продолговатом мозге. Сигналы, сформированные в форме залпов импульсов, поступают по блуждающим нервам к сердцу, которое сокращается в ритме этих залпов. Совершенно очевидно, что рассмотренные модели с синхронизацией дыхательного и сердечного ритмов являются лишь способом демонстрации скрытой, не выявляющейся при обычном наблюдении, возможности формирования сердечного ритма за счет возникающих в центре дискретных сигналов, приходящих к сердцу по блуждающим нервам. В естественных условиях сердечные центры имеют собственную периодику. В основу дальнейших исследований был положен синтез фактов, полученных в острых опытах с картированием синоатриального узла, показавших, что электрофизиологическим маркером воспроизведения сердцем ритма сигналов, поступающих по блуждающим нервам, является резкое увеличение зоны инициации возбуждения в синоатриальном узле, а также фактов, свидетельствующих о возможности формирования сигналов в блуждающих нервах в строгом соответствии с ритмом дыхания — факты выявления сердечно-дыхательного синхронизма у животных и человека. После подшивания зонда с электродами над областью синоатриального узла в хронических опытах на собаках посредством картирования устанавливалась область инициации возбуждения в синоатриальном узле. Оказалось, что во время хирургического вмешательства под наркозом очаг инициации возбуждения определяется одной точкой. После выхода животного из наркоза и установления адекватных отношений со средой (общение с персоналом, прием пищи и др.) очаг инициации расширился, что на основании предыдущих наблюдений позволило думать о включении центрального ритмовождения. Атропинизация животных или перерезка предварительно выведенных под кожу блуждающих нервов, т.е. прекращение поступления сигналов по ним, приводили к уменьшению зоны инициации возбуждения вновь до одной точки. Тот факт, что резкое уменьшение зоны инициации возбуждения в синоатриальном узле связано именно с прекращением в блуждающих нервах сигналов, синхронных с сокращениями сердца, обнаружен также у этих животных при сердечно-дыхательном синхронизме, вызванном термотахипноэ. Во время синхронизма зона инициации возбуждения в синоатриальном узле резко увеличивалась. Картирование области синоатриального узла при становлении центрального ритмовождения у человека полностью воспроизводит закономерности, выявленные в хронических опытах на животных. На рис. 6.14 представлены фрагменты картирования области синоатриального узла, выполненного с целью диагностики восстановления центрального ритмовождения сердца у человека, перенесшего кардиохирургическую операцию.
Ориентиры расположения крупных вен и отделов сердца: НВП — нижняя полая вена, ВПВ — верхняя полая вена, ПЖ — правый желудочек, ПУ — правое ушко. От области синоатриального узла посредством зонда, несущего 6 платиновых отводящих электродов, информация через аналогоцифровой преобразователь поступала в компьютер, который, используя специальную программу, фиксировал динамику очага инициации возбуждения в узле. Картирование, выполненное непосредственно после операции, выявило очаг инициации только под одним электродом (рис. 6.14, а), что свидетельствовало о генерации возбуждения в синоатриальном узле. На 2-е сутки очаг охватывал уже площадь между двумя электродами (рис. 6.14, б), на 4-е сутки утром — тремя (рис. 6.14, в), днем — пятью (рис. 6.14, г) и вечером — шестью электродами (рис. 6.14, д), что демонстрировало включение и становление центрального ритмовождения. Описанная динамика очага инициации возбуждения коррелировала с восстановлением общего состояния пациента и восстановлением возможности получения сердечно-дыхательного синхронизма при дыхании в такт мигания лампочки фотостимулятора. Совокупность накопленных фактов свидетельствует о существовании наряду с генератором ритма в самом сердце генератора ритма в ЦНС. Внутрисердечный генератор является фактором жизнеобеспечения, сохраняя насосную функцию сердца тогда, когда ЦНС находится в состоянии глубокого торможения. Центральный генератор организует адаптивные реакции сердца в естественных регуляторных реакциях организма. Воспроизведение сердцем центрального ритма обеспечивается спецификой электрофизиологических процессов во внутрисердечном пейсмекере. Наличие двух уровней ритмогенеза обеспечивает надежность и функциональное совершенство системы формирования ритма сердца. 6.1.4. Эндокринная функция сердца Миоциты предсердий образуют атриопептид, или натрийуретический гормон. Стимулируют секрецию этого гормона растяжение предсердий притекающей кровью, изменение уровня натрия в крови, содержание в крови вазопрессина, а также влияния экстракардиальных нервов. Натрийуретический гормон обладает широким спектром физиологической актив ности. Он повышает экскрецию почками ионов Na+ и СГ, подавляя их реабсорбцию в канальцах нефронов. Повышение диуреза осуществляется посредством увеличения клубочковой фильтрации и подавления реабсорбции воды в канальцах. Натрийуретический гормон подавляет секрецию ренина, ингибирует эффекты ангиотензина II и альдостерона. Натрийуретический гормон расслабляет гладкие мышечные клетки мелких сосудов, способствуя тем самым снижению артериального давления, а также гладкую мускулатуру кишечника. 6.2. ФУНКЦИИ СОСУДИСТОЙ СИСТЕМЫ 6.2.1. Основные принципы гемодинамики. Классификация сосудов Гемодинамика описывает механизмы движения крови в сердечно-сосудистой системе. Согласно законам гидродинамики, количество жидкости (Q), протекающее через любую трубу, прямо пропорционально разности давлений в начале (Р|) и в конце (Р2) трубы и обратно пропорционально сопротивлению (R) току жидкости: Если применить это уравнение к сосудистой системе, то следует иметь в виду, что давление в конце данной системы, т.е. в месте впадения полых вен в сердце, близко к нулю. В этом случае уравнение можно записать так: где Q — количество крови, изгнанное сердцем в минуту; Р — величина среднего давления в аорте; R — величина сосудистого сопротивления. Из этого уравнения следует, что Р = Q • R, т.е. давление (Р) в устье аорты прямо пропорционально объему крови, выбрасываемому сердцем в артерии в 1 мин (Q) и величине периферического сопротивления (R). Давление в аорте (Р) и минутный объем крови (Q) можно измерить непосредственно. Зная эти величины, вычисляют периферическое сопротивление — важнейший показатель состояния сосудистой системы. Периферическое сопротивление сосудистой системы складывается из множества отдельных сопротивлений каждого сосуда. Любой из таких сосудов можно уподобить трубке, сопротивление которой (R) определяется по формуле Пуазейля: R = где L — длина трубки; г| — вязкость протекающей в ней жидкости; п — отношение окружности к диаметру; г — радиус трубки. Сосудистая система состоит из множества отдельных трубок, соединенных параллельно и последовательно. При последовательном соединении трубок их суммарное сопротивление равно сумме сопротивлений каждой трубки: R = R, + R2 + R3 +... + Rn. При параллельном соединении трубок их суммарное сопротивление вычисляют по формуле: */ri + 7r2 + 7r3 + + 7Rn Точно определить сопротивление сосудов по этим формулам невозможно, так как геометрия сосудов изменяется вследствие сокращения сосудистых мышц. Вязкость крови также не является величиной постоянной. Например, если кровь протекает через сосуд диаметром меньше 1 мм, вязкость крови значительно уменьшается. Чем меньше диаметр сосуда, тем меньше вязкость протекающей в нем крови. Это связано с тем, что в крови наряду с плазмой имеются форменные элементы, которые располагаются в центре потока. Пристеночный слой представляет собой плазму, вязкость которой намного меньше вязкости цельной крови. Чем тоньше сосуд, тем большую часть площади его поперечного сечения занимает слой с минимальной вязкостью, что уменьшает общую величину вязкости крови. Теоретический расчет сопротивления капилляров невозможен, так как в норме открыта только часть капиллярного русла, остальные капилляры являются резервными и открываются по мере усиления обмена веществ в тканях. Из приведенных уравнений видно, что наибольшей величиной сопротивления должен обладать капилляр, диаметр которого 5—7 мкм. Однако вследствие того что огромное количество капилляров включено в сосудистую сеть, по которой осуществляется ток крови, параллельно их суммарное сопротивление меньше, чем суммарное сопротивление артериол. Основное сопротивление току крови возникает в артериолах. Систему мелких артерий и артериол называют сосудами сопротивления, или резистивными сосудами. Артериолы представляют собой тонкие сосуды (диаметр 15—70 мкм). Стенка их содержит толстый слой циркулярно расположенных гладкомышечных клеток, при сокращении которого просвет сосуда может значительно уменьшаться. При этом резко повышается сопротивление артериол. Изменение сопротивления артериол меняет уровень давления крови в артериях. При увеличении сопротивления артериол отток крови из артерий уменьшается и давление в них повышается. Снижение тонуса артериол увеличивает отток крови из артерий, что приводит к уменьшению артериального давления. Наибольшим сопротивлением среди всех участков сосудистой системы обладают именно артериолы, поэтому изменение их просвета является главным регулятором уровня общего артериального давления. Артериолы — «краны сердечно-сосудистой системы» (И.М. Сеченов). Открытие этих «кранов» увеличивает отток крови в капилляры соответствующей области, улучшая местное кровообращение, а закрытие резко ухудшает кровообращение данной сосудистой зоны. Итак, артериолы играют двоякую роль: участвуют в поддержании необходимого организму уровня АД и в регуляции величины местного кровотока через тот или иной орган или ткань. Величина органного кровотока соответствует потребности органа в кислороде и питательных веществах, определяемой уровнем рабочей активности органа. В работающем органе тонус артериол уменьшается, что обеспечивает повышение притока крови. Чтобы АД при этом не снизилось, в других, неработающих, органах тонус артериол повышается. Суммарная величина общего периферического сопротивления и уровень артериального давления остаются примерно постоянными, несмотря на непрерывное перераспределение крови между работающими и неработающими органами. О сопротивлении в различных сосудах можно судить по разности давления крови в начале и в конце сосуда: чем выше сопротивление току крови, тем большая сила затрачивается на ее продвижение по сосуду и, следовательно, тем значительнее снижение давления на протяжении данного сосуда. Как показывают прямые измерения давления крови в разных сосудах, давление на протяжении крупных и средних артерий падает всего на 10 %, а в артериолах и капиллярах — на 85 %. Это означает, что 10 % энергии, затрачиваемой желудочками на изгнание крови, расходуется на продвижение крови в крупных и средних артериях, а 85 % — на продвижение крови в артериолах и капиллярах. Зная объемную скорость кровотока (количество крови, протекающее через поперечное сечение сосуда), измеряемую в миллилитрах в секунду, можно рассчитать линейную скорость кровотока, которая выражается в сантиметрах в секунду. Линейная скорость (V) отражает скорость продвижения частиц крови вдоль сосуда и равна объемной (Q), деленной на площадь поперечного сечения кровеносного сосуда: Линейная скорость, вычисленная по этой формуле, есть средняя скорость. В действительности линейная скорость различна для частиц крови, продвигающихся в центре потока и у сосудистой стенки. В центре сосуда линейная скорость максимальна, около стенки сосуда она минимальна в связи с тем, что здесь особенно велико трение частиц крови о стенку. Объем крови, протекающей в 1 мин через аорту или полые вены и через легочную артерию или легочные вены, одинаков. Отток крови от сердца соответствует ее притоку. Из этого следует, что объем крови, протекший в 1 мин через всю артериальную и всю венозную систему большого и малого круга кровообращения, одинаков. При постоянном объеме крови, протекающей через любое общее сечение сосудистой системы, линейная скорость кровотока не может быть постоянной. Она зависит от общей ширины данного отдела сосудистого русла. Это следует из уравнения, выражающего соотношение линейной и объемной скорости: чем больше общая площадь поперечного сечения сосудов, тем меньше линейная скорость кровотока. В кровеносной системе самым узким местом является аорта. При разветвлении артерий, несмотря на то что каждая ветвь сосуда уже той, от которой она произошла, наблюдается увеличение просвета суммарного русла, так как сумма просветов артериальных ветвей больше просвета разветвившейся артерии. Наибольшее расширение русла отмечается в капиллярной сети: сумма просветов всех капилляров примерно в 500—600 раз больше просвета аорты. Соответственно этому кровь в капиллярах движется в 500—600 раз медленнее, чем в аорте. В венах линейная скорость кровотока снова возрастает, так как при слиянии вен друг с другом суммарный просвет кровяного русла суживается. В полых венах линейная скорость кровотока достигает половины скорости в аорте. В связи с тем что кровь нагнетается сердцем отдельными порциями, кровоток в артериях имеет пульсирующий характер, поэтому линейная и объемная скорости непрерывно меняются: они максимальны в аорте и легочной артерии в момент систолы желудочков и уменьшаются во время диастолы. В капиллярах и венах линейная скорость кровотока постоянна. В превращении пульсирующего кровотока в постоянный имеют значение свойства артериальной стенки. Непрерывный ток крови по всей сосудистой системе обусловливают выраженные упругие свойства аорты и крупных артерий. В сердечно-сосудистой системе часть кинетической энергии, развиваемой сердцем во время систолы, затрачивается на растяжение аорты и отходящих от нее крупных артерий. Последние образуют эластическую, или компрессионную, камеру, в которую поступает значительный объем крови, растягивающий ее; при этом кинетическая энергия, развитая сердцем, переходит в энергию эластического напряжения артериальных стенок. Когда систола заканчивается, растянутые стенки артерий стремятся спадаться и проталкивают кровь в капилляры, поддерживая кровоток во время диастолы. С позиций функциональной значимости для системы кровообращения сосуды подразделяют на несколько групп. Д Упруго-растяжимые — аорта с крупными артериями в большом круге кровообращения, легочная артерия с ее ветвями — в малом круге, т.е. сосуды эластического типа. Д Сосуды сопротивления (резистивные сосуды) — артериолы, в том числе и прекапиллярные сфинктеры, т.е. сосуды с хорошо выраженным мышечным слоем. Д Обменные (капилляры) — сосуды, обеспечивающие обмен газами и другими веществами между кровью и тканевой жидкостью. Д Шунтирующие (артериовенозные анастомозы) — сосуды, обеспечивающие «сброс» крови из артериальной в венозную систему сосудов, минуя капилляры. Д Емкостные — вены, обладающие высокой растяжимостью. Благодаря этому в венах содержится 75—80 % крови. Процессы, обеспечивающие непрерывность циркуляции (кругооборот) крови по системе последовательно соединенных сосудов, называют системной гемодинамикой. Процессы, протекающие в параллельно подключенных к аорте и полым венам сосудистых руслах, обеспечивающие кровоснабжение органов, называют регионарной, или органной гемодинамикой. 6.2.2. Движение крови по сосудам
|
||
|
Последнее изменение этой страницы: 2021-06-14; просмотров: 79; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.137 (0.018 с.) |


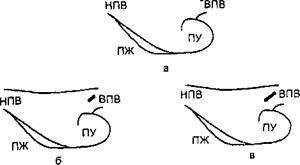
 Рис. 6.14. Динамика очага инициации возбуждения в синоатриальном узле сердца человека при восстановлении центрального ритмовождения (объяснение в тексте).
Рис. 6.14. Динамика очага инициации возбуждения в синоатриальном узле сердца человека при восстановлении центрального ритмовождения (объяснение в тексте).


