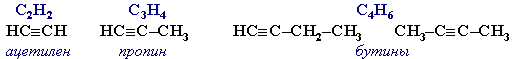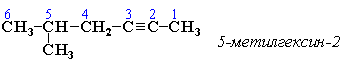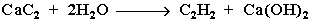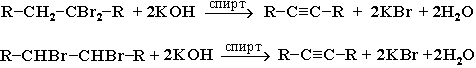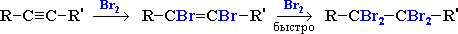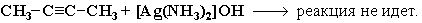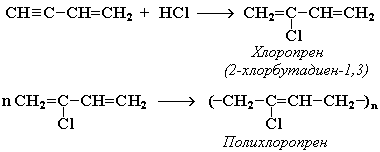Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема 2.5 Алкины (ацетиленовые углеводоролы)Содержание книги
Поиск на нашем сайте Алкины (ацетиленовые углеводороды) – непредельные алифатические углеводороды, молекулы которых содержат тройную связь C≡C. В образовании такой связи участвуют атомы углерода в sp -гибридизованном состоянии Общая формула гомологического ряда алкинов СnН2n-2. Простейшие представители:
Строение молекулы ацетилена: Тройную связь C≡C осуществляют 6 общих электронов:
Каждый из атомов углерода имеет по две sp -гибридных орбитали, направленных друг к другу под углом 180°, и две негибридных р -орбитали, расположенных под углом 90° по отношению друг к другу и к sp -гибридным орбиталям: π-Cвязи располагаются во взаимно перпендикулярных плоскостях:
σ-Cвязи, образуемые sp –гибридными орбиталями углерода, располагаются на одной прямой (под углом 180° друг к другу). Поэтому молекула ацетилена имеет линейное строение:
Номенклатура алкинов По систематической (международной) номенклатуре ИЮПАК названия ацетиленовых углеводородов производят от названий соответствующих алканов (с тем же числом атомов углерода) путем замены суффикса –ан на –ин: 2 атома С → эт ан → эт ин; 3 атома С → проп ан → проп ин и т.д. Главная цепь выбирается таким образом, чтобы она обязательно включала в себя тройную связь (т.е. она может быть не самой длинной). Нумерацию углеродных атомов начинают с ближнего к тройной связи конца цепи. Цифра, обозначающая положение тройной связи, ставится обычно после суффикса –ин. Например:
Изомерия алкинов Структурная изомерия 1. Изомерия положения тройной связи (начиная с С4Н6):
2. Изомерия углеродного скелета (начиная с С5Н8):
3. Межклассовая изомерия с алкадиенами и циклоалкенами, начиная с С4Н6:
Пространственная изомерия в алкинах относительно тройной связи не проявляется, т.к. заместители могут располагаться только одним способом – вдоль линии связи. Способы получения алкинов Ацетилен и его гомологи являются важнейшими исходными продуктами в производстве многих органических веществ и материалов. Их получают в больших количествах, используя ряд промышленных и лабораторных методов: 1. Пиролиз метана:
2. Пиролиз этана или этилена:
3. Гидролиз карбида кальция:
4. Дегидрогалогенирование дигалогеналканов спиртовым раствором щелочи (щелочь и спирт берутся в избытке):
5. Удлинение цепи (алкилирование ацетиленидов) при действии на ацетилениды алкилгалогенидами:
Физические свойства алкинов Температуры кипения и плавления ацетиленовых углеводородов увеличиваются с ростом их молекулярной массы. При обычных условиях алкины С2Н2 - С4Н6 – газы, С5Н8 - С16Н30 – жидкости, с С17Н32 – твердые вещества. Температуры кипения и плавления алкинов выше, чем у соответствующих алкенов. Алкины плохо растворимы в воде, лучше – в органических растворителях. Химические свойства алкинов Свойства алкинов сходны со свойствами алкенов, что обусловлено их ненасыщенностью, поэтому для них характерны реакции электрофильного присоединения. Примеры реакций присоединения к алкинам: 1. Гидрирование В присутствии металлических катализаторов (Pt, Ni) алкины присоединяют водород с образованием алкенов (разрывается первая π-связь), а затем алканов (разрывается вторая π-связь):
2. Галогенирование Электрофильное присоединение галогенов к алкинам протекает медленнее, чем для алкенов (первая π-связь разрывается труднее, чем вторая):
Алкины обесцвечивают бромную воду (качественная реакция на кратную связь). 3. Гидрогалогенирование Присоединение к несимметричным алкинам определяется правилом Марковникова:
Гидрохлорирование ацетилена используется в одном из промышленных способов получения винилхлорида:
Винилхлорид является исходным веществом (мономером) в производстве поливинилхлорида (ПВХ). Особые реакции алкинов 1. Гидратация (реакция Кучерова): Присоединение воды происходит в присутствии катализатора соли ртути (II) и идет через образование неустойчивого непредельного спирта, который изомеризуется в уксусный альдегид (в случае ацетилена):
или в кетон (в случае других алкинов):
2. Полимеризация: - Димеризация под действием водно-аммиачного раствора CuCl:
- Тримеризация ацетилена над активированным углем приводит к образованию бензола (реакция Зелинского):
3. Образование солей: Замещение атома водорода у углерода с тройной связью на металл, проявление слабокислотных свойств; при этом образуются соли - ацетилениды:
При взаимодействии ацетилена (или R–C≡C–H) с аммиачными растворами оксида серебра или хлорида меди (I) выпадают осадки нерастворимых ацетиленидов:
Образование серовато-белого осадка ацетиленида серебра (или красно-коричневого – ацетиленида меди RC≡CCu) служит качественной реакцией на концевую тройную связь. Если тройная связь находится не на конце углеродной цепи, то кислотные свойства отсутствуют (нет подвижного атома водорода) и ацетилениды не образуются:
4. Окисление алкинов: · При жестком окислении (нагревание, концентрированные растворы, кислая среда) происходит расщепление углеродного скелета молекулы алкина по тройной связи и образуются карбоновые кислоты:
· Мягкое окисление без разрыва σ-связи С–С происходит при действии разбавленного раствора перманганата калия, который при этом обесцвечивается. Данная реакция доказывает ненасыщенность алкинов и является качественной на кратную связь, в этих условиях из ацетилена образуется щавелевая кислота:
· Полное окисление алкинов происходит при их сгорании до CO2 и H2O. Горение ацетилена сопровождается выделением большого количества тепла (Q = 1300 кДж/моль):
Температура ацетиленово-кислородного пламени достигает 2800-3000 °С. На этом основано применение ацетилена для сварки и резки металла. Ацетилен образует с воздухом и кислородом взрывоопасные смеси. Применение алкинов Ацетилен используется для получения самых разнообразных веществ: для синтеза винилхлорида, являющегося мономером для получения высокомолекулярного продукта – поливинилхлорида; для получения винил ацетилена – важного промежуточного продукта в производстве синтетического хлоропренового каучука; для производства уксусного альдегида, из которого получают уксусную кислоту; а также для автогенной сварки. Схема реакции получения хлоропренового каучука из винилацетилена:
|
||
|
Последнее изменение этой страницы: 2021-06-14; просмотров: 187; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.007 с.) |