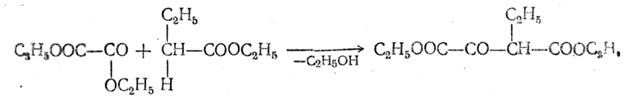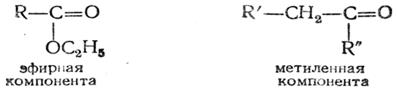Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Бета-Кетонокислоты. Ацетоуксусная кислота и ацетоуксусный эфир
Ацетоуксусная кислота и ацетоуксусный эфир. Простейшая из β-кетонокислот, ацетоуксусная СН3—СО—СН2—СООН. подобно другим β-кетонокислотам, отличается непрочностью. Уже при слабом нагревании она даже в водных растворах разлагается на ацетон и двуокись углерода. Еще менее прочны ее соли с тяжелыми металлами, разлагающиеся с образованием ацетона даже при обыкновенной температуре. Ацетоуксусная кислота содержится в моче больных диабетом. Чрезвычайно большой теоретический интерес и большое значение для синтезов имеет этиловый эфир ацетоуксусной кислоты, обыкновенно называемый просто ацетоуксусным эфиром. Он образуется при конденсации двух молекул уксусноэтилового эфира, причем конечный результат реакции можно выразить уравнением
Конденсация происходит под влиянием алкоголята натрия или металлического натрия, а также амида натрия NH2Na, Аналогичным образом могут конденсироваться и другие сложные эфиры, а также смеси двух эфиров, причем если одним из компонентов смеси является эфир муравьиной кислоты, получаются эфиры β-альдегидокислот. В подобную конденсацию не могут вступать эфиры α,α-двузамещенных гомологов уксусной кислоты. Например, конденсация щавелевого эфира с эфиром масляной кислоты протекает нормально с образованием оксалилмасляного эфира
но не идет с изомасляным эфиром (СН3)2СН—СООС2Н5. Кроме конденсации этилацетата, ацетоуксусный эфир может получаться также алкоголизом дикетена:
Оба способа используются в промышленном масштабе, Ацетоуксусный эфир представляет собой жидкость с приятным фруктовым запахом, кипящую с небольшим разложением при 181° С, немного растворимую в воде, смешивающуюся со спиртом и эфиром. Плотность свежеперегнанного ацетоуксусного эфира несколько изменяется при стоянии, но через несколько часов становится постоянной (d 420 = 1,0282). Другие физические свойства ацетоуксусного эфира также становятся постоянными лишь после многочасового стояния. Сложноэфирная конденсация Образование ацетоуксусного эфира из двух молекул уксусноэтилового эфира представляет собой частный случай сложноэфирных конденсаций, которые могут протекать как между двумя молекулами сложных эфиров, так и между молекулой сложного эфира и молекулой другого карбонилсодержащего соединения. При таких конденсациях одно из веществ, участвующих в реакции, рассматривают как эфирную компоненту, а другое — как метиленную компоненту:
Эфирная компонента вместо группы —ОС2Н5 может содержать группу —NHR. В метиленной компоненте R" может означать —ОС2Н5, — NHR, —Н, —С n Н 2n + 1. Для объяснения механизма этих реакций предлагались различные схемы. Клайзен, очень, много занимавшийся изучением этих реакций, предложил такую схему:
По этой схеме процесс сводится к присоединению алкоголята натрия к карбонильной группе первой молекулы сложного эфира, после чего с образовавшимся продуктом реагирует вторая молекула сложного эфира, причем происходит отщепление двух молекул спирта. В конечном счете образуется натриевое производное β-оксикротонового эфира, который может быть выделен действием разбавленных кислот. Выделенный β-оксикротоновый эфир быстро изомеризуется (частично, как мы увидим далее) в эфир соответствующей кетонокислоты:
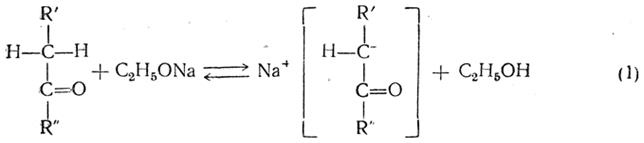
Арндт и Эйстерт дали развернутую, по-видимому, наиболее обоснованную формулировку механизма сложноэфирных конденсаций на основе современных электронных представлений. По их мнению, механизм процесса заключается в следующем. Щелочной конденсирующий агент образует с метиленной компонентой, способной отщеплять протон, ионогенно построенную соль, образованную анионным остатком метиленной компоненты и катионом Na+ (из C2H5ONa, NH2Na, Na):
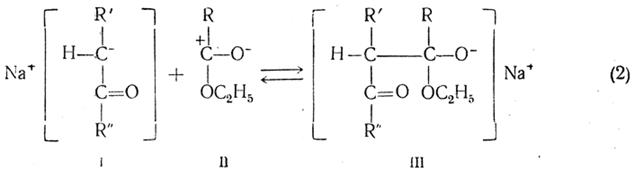
Для успешного протекания реакции достаточно, чтобы такая соль образовалась хотя бы из весьма малой доли метиленной компоненты. Вторым этапом конденсации является также обратимое образование комплекса:
При этом углеродный атом метиленной компоненты, несущий свободную электронную пару, присоединяется к положительно заряженному углеродному атому эфирной компоненты. В анионе комплекса III второй атом водорода метиленной компоненты находится уже под влиянием двух соседних «карбонильных» группировок и, следовательно, стремится к отщеплению в виде протона, а группа —ОС2Н5 в эфирной компоненте, как и вообще в полуацеталях, связана весьма слабо. Поэтому от комплекса III легко отщепляется молекула спирта:
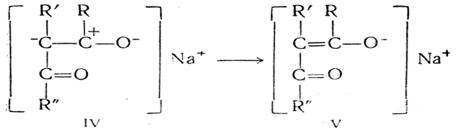
В заключение анион IV должен перегруппировываться в анион енольной формы ацетоуксусного эфира V:
Этот анион содержит сопряженную систему двойных связей О=С—С=С. По Арндту и Эйстерту, стремление образовать такую сопряженную систему является движущей силой протекания сложноэфирных конденсаций, придающей процессу необратимость. С точки зрения этих представлений, становится понятным, почему у метиленной компоненты должно быть по меньшей мере два атома водорода при углеродном атоме, соседнем с карбонильной группой. Понятно также, почему сложноэфирные конденсации не идут с соединениями, содержащими сульфонные группы —SO2— рядом с метиленовой группой. Как мы уже ранее видели, в сульфонных группах, в противоположность кетонным (карбонильным), атомы кислорода связаны не двойными, а семиполярными связями:
По этой причине в такого рода соединениях не может возникнуть сопряженная система связей О=S—С=С, аналогичная О=С—С=С, что, по Арндту и Эйстерту, является необходимым условием для протекания сложноэфирной конденсации.
|
||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 104; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.110.119 (0.008 с.) |