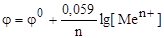Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Электродные потенциалы и гальванические элементыСодержание книги
Поиск на нашем сайте
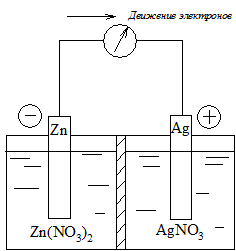
Система, состоящая из металла, погруженного в раствор электролита, называется электродом. Гальваническим элементом называется многофазная система, состоящая по меньшей мере из двух электродов (полуэлементов). В качестве примера рассмотрим цинк-серебряный гальванический элемент (рис. 1), состоящий из цинкового и серебряного полуэлементов. Гальванический элемент (рис.1) состоит из растворов, содержащих ионы Zn2+ и Ag+, разделенных пористой диафрагмой для того, чтобы обеспечить протекание тока без смешения растворов. В каждый из растворов опущен электрод из соответствующего металла. Границу раздела фаз металл – раствор обозначают символом «/», а электролитический контакт растворов – «//». Таким образом, схему рассматриваемого элемента можно представить в виде
Рис. 1. Схема цинк-серебряного гальванического элемента В цинковом полуэлементе протекает реакция окисления, электрод называют анодом. При протекании тока масса анода уменьшается за счет его растворения. Zn «Zn2+ + 2e. В серебряном полуэлементе протекает реакция восстановления, электрод называют катодом. При протекании тока масса катода увеличивается за счет осаждения на его поверхности металла. 2 Ag+ + 2e «Ag Суммарная реакция получается сложением полурекций: Zn + 2Ag+ «Zn2+ + 2 Ag Направление протекания самопроизвольного процесса, можно определить из величин электродных потенциалов полуэлементов. Электродный потенциал это разность потенциалов гальванического элемента, состоящего из исследуемого электрода и электрода сравнения, при условии, что ток во внешней цепи стремится к нулю. Измеренную в таких условиях разность потенциалов называют электродвижущей силой (коротко – э.д.с.). Стандартным электродом сравнения служит стандартный водородный электрод. Это газовый электрод, состоящий из платиновой проволоки, покрытой слоем платиновой черни, находящийся в атмосфере водорода под давлением 1,013×105 Па (1 атм) и погруженный в раствор с активностью ионов Н+ равной 1,0 моль/дм3. В соответствии с международным соглашением потенциал такого электрода условно принят за нуль при любых температурах.
Таким образом, для измерения электродного потенциала необходимо собрать гальванический элемент, состоящий из исследуемого электрода (всегда записывают справа) и стандартного водородного электрода (всегда записывают слева). Например, для цинкового электрода
Э.д.с. такого гальванического элемента, называют стандартным электродным потенциалом если измерения проводят при стандартных условиях (активности всех компонентов равны 1,00 моль/дм3, Т = 298 К)
Уравнение Нернста. Потенциал электрода зависит от состава электролита и температуры в соответствии с уравнением Нернста:
где φ – потенциал в Вольтах, φо-стандартный электродный потенциал; aок, aвос – активности потенциалопределяющих ионов в окисленном и восстановленном состоянии; n – число электронов, принимающих участие в данной электродной реакции; F = 96480 Кл/моль (постоянная Фарадея); R - универсальная газовая постоянная; Т – температура, К. При Т = 298 К для металлических электродов уравнение Нернста имеет вид:
Опыт 1. Изготовление и изучение работы медно-цинкового Реактивы и оборудование. Гальванометр или цифровой вольтметр; химические стаканы на 50 см3; медная и цинковая пластины; электролитический мост, электрические провода, раствор ZnSO4 1,0 М; раствор CuSO4 1,0 М. Выполнение работы. Собрать медно-цинковый гальванический элемент (элемент Даниэля) в соответствии со схемой Zn/ZnSO4//CuSO4/Cu. Конструкция прибора схематично представлена на рис. 1. Для этого в стаканы налить растворы солей меди и цинка, поместить в них соответствующие электроды и соединить растворы электролитическим мостом. Подключить во внешнюю цепь вольтметр и наблюдать протекание электрического тока. Запись данных опыта. Зарисовать прибор, составить схему гальванического элемента (см. рис 1), рассчитать ЭДС гальванического элемента по плану: 1. Определить стандартные потенциалы меди и цинка (табл. П. 1), записать уравнения электродных процессов и суммарную реакцию. 2. Указать катод и анод, их заряды, направление движения электронов во внешней цепи и ионов в растворе. 3. Рассчитать э.д.с. стандартного медно-цинкового гальванического элемента.
|
|||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 138; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.133.155.48 (0.009 с.) |

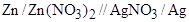
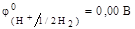
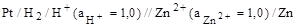
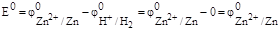 .
.