Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Фазовые переходы и равновесие. Химическое равновесие в гомогенных и гетерогенных системах. Константа равновесия.
В химических реакциях исходные вещества не всегда полностью превращаются в продукты реакции. Это происходит потому, что по мере накопления продуктов реакции могут создаваться условия для протекания обратимой реакции в противоположном направлении. Например, если смешать пары йода с водородом при температуре 200 ° С, то произойдет реакция:
Однако известно, что йодистый водород уже при нагревании до 180 °С начинает разлагаться на йод и водород:
Понятно, что в этих условиях не произойдет ни полного разложения НI, так как продукты реакции способны вновь реагировать между собой, ни полного образования йодистого водорода. Обратимая химическая реакция – это реакция, в ходе которой происходят превращения как в прямом, так и в обратном направлениях, При написании уравнений обратимых реакций вместо знака равенства ставят две противоположно направленные стрелки. Уравнение рассмотренной выше обратимой реакции запишется следующим образом:
Реакцию, протекающую слева направо, называют прямой (константа скорости прямой реакции k 1), справа налево — обратной (константа скорости обратной реакции k 2). В обратимых реакциях скорость прямой реакции вначале имеет максимальное значение, а затем уменьшается вследствие уменьшения концентрации исходных веществ, расходуемых на образование продуктов реакции. И наоборот, обратная реакция в начальный момент имеет минимальную скорость, которая увеличивается по мере увеличения концентрации продуктов реакции. Следовательно, скорость прямой реакции уменьшается, а обратной — увеличивается. Наконец, наступает такой момент, когда скорости прямой и обратной реакций становятся равными. Химическое равновесие – состояние системы, в котором скорость прямой реакции (υ1) равна скорости обратной реакции (υ2). При химическом равновесии концентрации веществ остаются неизменными. Химическое равновесие имеет динамический характер: прямая и обратная реакции при равновесии не прекращаются. Положение равновесия можно определить, зная скорости прямой и обратной реакций. Уравнение обратимой реакции имеет вид
Согласно закону действующих масс, скорости прямой реакции u1 и обратной u2 соответственно запишутся следующим образом:
В равновесии скорости прямой и обратной реакций равны: k 1[ A ] m ·[ B ] n = k 2[ C ] p ·[ D ] q. Состояние химического равновесия количественно характеризуется константой равновесия, представляющей собой отношение констант прямой (k 1) и обратной (k 2) реакций. Преобразуем эту формулу и получим:
Константа равновесия (Кр или К) зависит от температуры и природы реагирующих веществ. Чем больше константа равновесия, тем больше равновесие сдвинуто в сторону образования продуктов прямой реакции, т. е. численное значение константы равновесия характеризует тенденцию к осуществлению реакции или, другими словами, характеризует выход данной реакции. Так, при К >> 1 выход реакции велик (равновесие смещено в сторону прямой реакции), так как при этом
Понятно, что при К << 1 выход реакции мал (.равновесие смещено в сторону обратной реакции).
|
|||||
|
Последнее изменение этой страницы: 2021-05-11; просмотров: 150; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.21.162.87 (0.006 с.) |
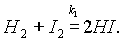
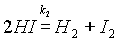 .
.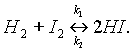
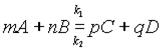 .
.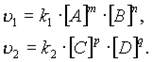
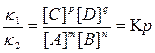 .
.