
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Факторы, влияющие на скорость химических реакций.
Природа реагирующих веществ. Большую роль играет характер химических связей и строение молекул реагентов. Реакции протекают в направлении разрушения менее прочных связей и образования веществ с более прочными связями. Так, для разрыва связей в молекулах H2 и N2 требуются высокие энергии; такие молекулы мало реакционноспособны. Для разрыва связей в сильнополярных молекулах (HCl, H2O) требуется меньше энергии, и скорость реакции значительно выше. Реакции между ионами в растворах электролитов протекают практически мгновенно. Концентрация. С увеличением концентрации (числа частиц в единице объема) чаще происходят столкновения молекул реагирующих веществ – скорость реакции возрастает. Один из основных законов физической химии устанавливает зависимость скорости химической реакции от концентраций реагирующих веществ и соотношение между концентрациями (или активностями) продуктов реакции и исходных веществ в состоянии химического равновесия. Норвежские ученые К. Гульдберг и П. Вааге, сформулировавшие этот закон в 1864–67, назвали «действующей массой» вещества его количество в единице объема, т. е. концентрацию, отсюда – наименование закона. Закон действующих масс: При постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, равных стехиометрическим коэффициентам в уравнении реакции. В общем случае, если в реакцию вступают одновременно m молекул вещества А и n молекул вещества В, т. е. m А + n В → С, уравнение скорости реакции имеет вид:
где k – коэффициент пропорциональности, который называется константой скорости реакции; [ А ] – молярная концентрация вещества А; [ В ] – молярная концентрация вещества В; m и n – стехиометрические коэффициенты в уравнении реакции. Из закона действия масс следует, что чем больше концентрация реагирующих веществ, тем выше вероятность их столкновения в объеме системы и тем больше скорость реакции в данный момент времени. Константа скорости реакции k зависит от природы реагирующих веществ, температуры и катализатора, а в случае жидкого раствора – также и от давления; последняя зависимость существенна лишь при высоких давлениях, но не зависит от значения концентраций реагентов. Физический смысл константы скорости заключается в том, что она равна скорости реакции при единичных концентрациях реагирующих веществ.
Для гетерогенных реакций концентрация твердой фазы в выражение скорости реакции не входит. Так, например, выражение закона действующих масс для следующих реакций: 1) N2(г) + 3H2(г) = 2NH3(г); 1) 2C(к) + O2(г) = 2CO(г). 1) Поскольку в данной реакции все вещества находятся в газообразном состоянии, то данная система будет являться гомогенной и в формулу закона для прямой реакции будут входить концентрации всех компонентов: u=[N2]·[H2]3; для обратной реакции: u=[NH3]2. 2) Поскольку в данной реакции вещества находятся в газообразном и кристаллическом состоянии, то данная система будет являться гетерогенной и в формулу закона для прямой реакции будут входить концентрации только газообразных веществ ([C] не учитывается, т. к. углерод находится в кристаллическом состоянии, а концентрации кристаллических веществ равны единице.): u=[О2]; для обратной реакции: u=[CO]2. Температура. Многочисленные опыты показывают, что при повышении температуры скорость большинства химических реакций существенно увеличивается, причем для реакций в гомогенных системах при нагревании на каждые десять градусов скорость реакции возрастает в 2–4 раза (правило Вант-Гоффа). Это правило связано с понятием температурного коэффициента скорости реакции γ и определяется соотношением:
При увеличении температуры от t1 (Т1) до t2 (Т2) изменение скорости реакции можно рассчитать по формуле:
где С одной стороны, увеличение температуры приводит к увеличению скорости движения молекул и, как следствие, к более частым столкновениям. Но этот фактор не вызывает увеличение скорости даже в 2а раза, т. к. не все столкновения оказываются эффективными. Реакция начнется только в том случае, если энергия молекул превысит некоторую величину, достаточную для преодоления барьера отталкивания. В этом случае происходит сближение взаимодействующих частиц, при котором становиться возможным образование химической связи. При этом возникает активированный комплекс – единое образование из столкнувшихся молекул, находящихся в состоянии перераспределения электронной плотности. Такие молекулы называются активными, а энергия, которой должны обладать эти сталкивающиеся молекулы, чтобы их столкновение привело к химическому превращению, называют энергией активации. Отсюда следует, что при увеличении температуры увеличивается доля активных, т. е. способных к взаимодействию молекул, и скорость реакции увеличивается.
Правило Вант-Гоффа применимо только в узком интервале температур. Более точным является уравнение Аррениуса. Поверхность соприкосновения реагирующих веществ. Для гетерогенных систем, в которых вещества находятся в разных агрегатных состояниях, справедливо правило: чем больше поверхность соприкосновения, тем быстрее протекает реакция. Поверхность твердых веществ может быть увеличена путем их измельчения, а для растворимых веществ – путем их растворения. Катализ. Катализ – процесс, заключающийся в изменении скорости химических реакций в присутствии веществ, называемых катализаторами. Катализаторы – вещества, изменяющие скорость химической реакции, которые могут входить в состав промежуточных продуктов, но не входят в состав конечных продуктов реакции и после окончания реакции остаются неизменными. Каталитические реакции – реакции, протекающие в присутствии катализаторов. Положительным называют катализ, при котором скорость реакции возрастает, отрицательным (ингибированием) – при котором она убывает. Примером положительного катализа может служить процесс окисления аммиака на платине при получении азотной кислоты. Примером отрицательного – снижение скорости коррозии при введении в жидкость, в которой эксплуатируется металл, нитрита натрия, хромата и дихромата калия. Катализаторы, замедляющие химическую реакцию, называются ингибиторами. В зависимости от того, находится катализатор в той же фазе, что и реагирующие вещества, или образует самостоятельную фазу, говорят о гомогенном или гетерогенном катализе. При гомогенном катализе действие катализатора связано с тем, что он вступает во взаимодействие с реагирующими веществами с образованием промежуточных соединений, это приводит к снижению энергии активации. При гетерогенном катализе ускорение процесса обычно происходит на поверхности твердого тела – катализатора, поэтому активность катализатора зависит от величины и свойств его поверхности. На практике катализатор обычно наносят на твердый пористый носитель. Механизм гетерогенного катализа сложнее, чем у гомогенного.
|
||||||
|
Последнее изменение этой страницы: 2021-05-11; просмотров: 53; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.240.178 (0.006 с.) |
 ,
,
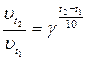 ,
,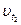 и
и  – скорости реакции при температурах t 2 и t 1 соответственно; γ – температурный коэффициент скорости данной реакции, показывающий, во сколько раз изменяется скорость реакции при изменении температуры на каждые 100 С.
– скорости реакции при температурах t 2 и t 1 соответственно; γ – температурный коэффициент скорости данной реакции, показывающий, во сколько раз изменяется скорость реакции при изменении температуры на каждые 100 С.


