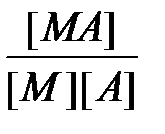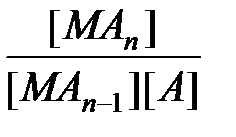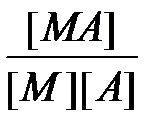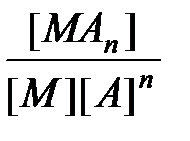Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Опыт 6. Возможность протекания ОВР ⇐ ПредыдущаяСтр 4 из 4
Используя стандартные окислительно-восстановительные потенциалы определить возможность протекания ОВР между дихроматом калия и соляной кислотой. В пробирку поместить несколько кристаллов дихромата калия, прилить 1-2 мл концентрированной соляной кислоты и нагреть в пламени спиртовки (ТЯГА!). Что наблюдается? Объясните причину протекания реакции. Написать уравнение реакции пользуясь электронно-ионным методом.
Контрольные вопросы 1. Какие из указанных ниже веществ: Cl2, PbO2, K2Cr2O7, KMnO4, Na2S, KJ, KBr, FeSO4, Na2SO3, NaNO2 - могут проявлять окислительные свойства, какие - востановительные свойства? 2. Рассчитайте DHo, DSo и DGo реакции 2(NH4)2CrO4(тв.) = Cr2O3 (тв.) + 2NH3 (г.)+ N2 (г.)+ 5H2O (г.) Какова роль энтальпийного и энтропийного факторов протекания этого процесса? Является ли процесс обратимым? Какие элементы изменяют степень окисления и к какому типу ОВР относится данный процесс? 3. Вычислите потенциал системы: а) Fe3+/Fe2+, если активности ионов Fe3+ = 0.1 моль/л, Fe2+ = 5·10-3 моль/л; б) MnO4-/Mn2+ при 1) [H+] = 1 моль/л и 2) [H+] = 1·10-2 моль/л, если [MnO4-]/[Mn2+] = 1.Объясните зависимость потенциала системы MnO4-/Mn2+ от рН среды. 4. Вычислите электродвижущую силу, необходимую для разложения хлорида натрия при 1100 К, если DGо при 1100 К равно 311 кДж/моль. 5. Составьте уравнения реакций, происходящих при электролизе раствора иодида калия на угольных электродах. 6. Пользуясь методом электронно-ионного баланса, закончите составление следующих уравнений окислительно-восстановительных реакций и укажите их тип: 1) KМnO4 + NaNO2 +H2SO4(разб.) ®... 2) NaClO + KJ + H2SO4(разб.) ® NaCl + J2 +... 3) Cl2 +KOH ® KСlO3 +... 4) J2 + Cl2 + H2O ®HJO3 +... 5) NO2 + NaOH ® NaNO2 +... 6) K2Cr2O7 + H2SO4(разб.) + FeSO4 ® Cr2(SO4)3 +... 7) H2S + H2SO3 ® S +... 8) KСlO3 ® O2 +... 9) KСlO3 ® KСlO4 +... 10) HNO2 ® NO +... 11) KМnO4 ® K2MnO4 + MnO2 + O2 12) As2S3 + HNO3 ® H3AsO4 + H2SO4 + NO +... 13) MnO2 + HCl(конц.) ®... 14) Mg + HNO3 ® NH4NO3 +... 15) Cu + HNO3 ® NO +... 16) KJ + H2SO4(конц.) ® J2 + H2S +... 7. Закончите уравнения реакции между следующими ионами, пользуясь методом электронно-ионного баланса: 1) MnO4- + NO2- + H+ ® Mn2+ + NO3- +... 2) Fe3+ + S2- ® S + Fe2+ 3) MnO4- + J- + H+ ® Mn2+ + J2 4) ClO- + J- + OH- ® JO3- + Cl- +... 5) MnO4- + SO32- + H+ ® Mn2+ + SO42- +... 6) MnO4- + NO2- + OH- ® Mn2+ + NO3- +... 8. Железная пластинка погружена в раствор CuSO4. После окончания реакции масса пластинки увеличилась на 2 грамма. Найти массу выделившейся из раствора меди. 9. Какую массу сероводорода можно окислить до свободной серы одним граммом йода?
Лабораторная работа № 6 КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
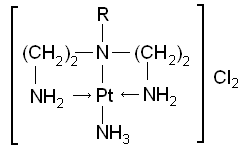
Основные положения Комплексными соединениями называются определенные химические соединения, образованные сочетанием отдельных компонентов и представляющие собой сложные ионы или молекулы, способные к существованию как в кристаллическом, так и в растворенном состоянии. Комплексные соединения содержат катионный, анионный или нейтральный комплекс, состоящий из центрального атома или иона и связанных с ним молекул или ионов - лигандов. Центральный атом (комплексообразователь) - обычно акцептор, а лиганды - доноры электронов и при образовании комплекса между ними возникает донорно-акцепторная, или координационная связь. Комплекс может быть электронейтральным (неэлектролит), иметь положительный заряд (комплексный катион) или отрицательный (комплексный анион). В случае образования комплексного соединения с одноименными лигандами все связи в комплексе равноценны, если он находится в растворе или в газовой фазе, а в случае разнородных лигандов характер связи зависит от их свойств. Число атомов лигандов, координированных центральным атомом, - координационное число (к.ч.) - обычно превышает его степень окисления. Лиганды, связанные с центральным атомом, образуют внутреннюю координационную сферу комплексного соединения. Анионы или катионы (противоионы), входящие вместе с комплексом в состав комплексного соединения, образуют вторую (внешнюю) сферу. В зависимости от числа донорных атомов лиганда, способных к координации, различают моно-, би- и полидентатные лиганды. Лиганды, координирующиеся через два и более донорных атомов к одному центральному атому, называются хелатными, а координирующиеся к разным центральным ионам - мостиковыми. Комплексы, в которых лиганды связывают два или более центральных ионов, называются би- или полиядерными. Полиядерные комплексы, имеющие химические связи между центральными атомами, называются кластерами. Комплексные соединения, содержащие циклические комплексы металлов с полидентатными лигандами, в которых центральный атом входит в один или несколько циклов, называются хелатами. Например:
Природа химической связи в комплексных соединениях. В комплексных соединениях - хотя бы одна из связей - донорно- акцепторная, образуется в результате перекрывания заселенных электронами орбиталей лигандов с вакантными орбиталями центрального атома. Если лиганд, как, например, OH-, OR-, NR2-, SR-, O2-, NR2-, имеет дополнительные неподеленные пары электронов, а центральный атом - подходящие вакантные орбитали, то образуются простые дативные связи. Лиганды, у которых есть вакантные орбитали с центральными атомами, имеющими d -электроны (как, например, у PR3, SR2, AsR3), могут образовывать обратные дативные связи p -типа. Оба эффекта приводят к упрочению координационной связи, увеличивая ее кратность. Природу химической связи в комплексных соединениях объясняют с помощью метода валентных связей, методов молекулярных орбиталей, электростатической теории и ее модификации - теории кристаллического поля. Комплексные соединения в водных растворах При растворении кристаллического комплексного соединения в воде его кристаллическая решетка разрушается, а координационная сфера и внешнесферные ионы гидратируются водой. Этот процесс протекает по механизму диссоциации сильных электролитов. Образование и диссоциация координационной сферы комплексных соединений происходит ступенчато: M + A Û MA K1 = MA + A Û MA2 K2 = ...... MAn-1 + A Û MAn K n = Константы К1, К2,..., К n называются ступенчатыми константами образования (устойчивости). Для обозначения полных констант образования используют символ b: M + A Û MA b 1 = M + 2A Û MA2 b 2 = ...... M + nA Û MAn b n = При этом b n является произведением ступенчатых констант b n =K1 × K2 × ¼ × K n. Константы K n и b n - термодинамические характеристики устойчивости комплекса в растворе. Величины, обратные K n или b n, называются константами диссоциации или нестойкости. Устойчивость комплексных соединений определяется природой центрального атома и лиганда и стерическими факторами. В соответствии с теорией «жестких» и «мягких» кислот и оснований все центральные атомы могут быть условно разделены на два класса: жесткие кислоты Льюиса и мягкие кислоты Льюиса. Первые имеют малый атомный или ионный радиус и высшую положительную степень окисления, предпочтительно взаимодействующие с неполяризующимися жесткими основаниями, такими как F-, OH-, NR2-. Кислоты второго класса имеют большой атомный или ионный радиус и низкую степень окисления, более эффективно взаимодействуют с легко поляризующимися мягкими лигандами. К жестким кислотам Льюиса относятся центральные ионы элементов в высших степенях окисления, с электронной конфигурацией d0 или d10. Мягкие кислоты Льюиса имеют электроны на d -орбиталях, способные к образованию p -связей в результате перекрывания с вакантными d -орбиталями мягких лигандов. С увеличением основных свойств лигандов устойчивость комплексов повышается. Комплексы хелатообразующих реагентов по сравнению с комплексами их монодентантных аналогов обладают повышенной устойчивостью (так называемый хелатный эффект).
Присоединение объемного заместителя к донорному атому или вблизи него, например, замена атома водорода на алкильную группу, приводит под влиянием стерических факторов к уменьшению стабильности комплекса, напротив, введение алкильных групп в другие положения, вследствие увеличения основности лигандов, повышает стабильность комплексов. На стабильность комплексов оказывает влияние и природа донорного атома лигандов. В случае «жестких» центральных атомов уменьшение размера донорных атомов лиганда и повышение его электронной плотности приводит к увеличению стабильности комплексов. Например, стабильность комплексов падает в рядах F > Cl > Br > J или O > S > Se > Te. В случае «мягких» центральных ионов наблюдается обратная тенденция: F < Cl < Br < J.
Экспериментальная часть Опыт 1. Образование и разрушение комплексных соединений а) В пробирку налить небольшое количество нитрата серебра и добавить двукратный объем хлорида натрия. Полученный осадок отцентрифугировать, фильтрат слить и к осадку добавить концентрированный раствор аммиака до полного его растворения. Напишите уравнения протекающих реакций в молекулярной и ионно-молекулярной формах. Запишите выражение для константы нестойкости образующегося комплексного иона и ее значение (справочник). Затем в пробирку с растворенным осадком добавить по каплям концентрированную азотную кислоту. Объяснить образование осадка и написать уравнение реакции. б) В пробирку внести несколько кристаллов соли CoCl2·6H2O и осторожно нагреть. Каким процессом обусловлено изменение цвета? Напишите уравнение реакции в молекулярной и ионно-молекулярной формах. Охладить пробирку и добавить несколько капель воды. Что образуется? в) К раствору соли Ni2+ добавляют в избытке водный раствор аммиака. Какой комплекс образуется? Добавить к полученному раствору раствор Na2S. Что происходит? Напишите уравнения протекающих реакций в молекулярной и ионно-молекулярной формах.
Опыт 2. Образование соединений с комплексным анионом К растворам солей Al3+, Cr3+, Sn2+, Zn2+, Pb2+, Co2+ приливают раствор NaOH до растворения вначале выпавшего осадка. Для растворения Pb(OH)2 и Co(OH)2 требуется концентрированный раствор щелочи. Напишите уравнения реакций в молекулярной и ионно-молекулярной формах и выражения для констант нестойкости образующихся комплексных ионов и их значения (справочник). Назовите полученные комплексные соединения.
Опыт 3. Образование соединений с комплексным катионом К растворам солей Cu2+, Zn2+ и Ni2+ приливают водный раствор аммиака. Осаждающиеся гидроксиды растворяют в избытке раствора аммиака. Напишите уравнения реакций в молекулярной и ионно-молекулярной формах и выражения для констант нестойкости образующихся комплексных ионов и их значения (справочник). Назовите полученные комплексные соединения.
|
||||||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 145; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.137.171.121 (0.016 с.) |