
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Институт математики, физики и информационных технологийСтр 1 из 3Следующая ⇒
Институт математики, физики и информационных технологий Кафедра «Общая и теоретическая физика»
Потемкина С.Н.
КУРС ЛЕКЦИЙ ПО ФИЗИКЕ 3й семестр Модуль 6
Лекция 10 Уравнение Шредингера. Движение частицы в потенциальной яме
2021 Вопросы Волновая функция. Уравнение Шрёдингера Прохождение частиц через потенциальный барьер Квантование энергии. Движение частицы в одномерной потенциальной яме. Квантовые числа. Квантовый гармонический осциллятор 7. Волновая функция
С 1900 по 1920 г - создание квантовой механики. Её создание связано с: 1) формулировкой М. Планком квантовой гипотезы в 1900 г; 2) работами австрийского физика Э. Шредингера, немецкого физика В. Гейзенберга и английского физика П. Дирака. На этом этапе возникли новые принципиальные проблемы, например, проблема физической природы волн де Бройля. Для выяснения этой проблемы сравним дифракцию световых волн и микрочастиц. Согласно волновым представлениям о природе света, интенсивность дифракционной картины пропорциональна квадрату амплитуды световой волны. А согласно фотонной теории, интенсивность определяется числом фотонов, попадающих в данную точку дифракционной картины. Т.е. число фотонов в данной точке дифракционной картины задается квадратом амплитуды световой волны, в то время как для одного фотона квадрат амплитуды определяет вероятность попадания фотона в ту или иную точку. Дифракционная картина для микрочастиц также характеризуется неодинаковым распределением потока микрочастиц по разным направлениям. Наличие max в дифракционной картине с точки зрения волновой теории означает, что эти направления соответствуют наибольшей интенсивности волн де Бройля. А интенсивность волн де Бройля оказывается больше там, где имеется большее число частиц. Т.е. дифракционная картина для микрочастиц является проявлением статической (вероятностной) закономерности. Но волны де Бройля нельзя истолковывать как волны вероятности, т.к. тогда вероятность обнаружения частиц в некоторых точках пространства может быть отрицательна, что не имеет смысла. Де Бройль связал со свободно движущейся частицей плоскую волну.
Реальная плоская волна, распространяющаяся в положительном направлении оси X, описывается уравнением:
Но
или в комплексной форме:
(48.3) -уравнение волны де Бройля для свободной частицы, где ψ – волновая или пси-функция. Уравнение Шрёдингера
В 1926 г. развивая идеи де Бройля о волновых свойствах вещества, Шрёдингер получил свое уравнение. Оно позволяет найти волновые функции частиц, движущихся в различных силовых полях.
где m - масса частицы, i - мнимая единица, U - потенциальная энергия, Δ - оператор Лапласа. Результат действия оператора Лапласа на некоторую функцию представляет собой сумму вторых частных производных по соответствующим координатам:
Из (49.1) следует, что вид волновой функции Ψ(x, y, z, t) определяется функцией U, т.е. характером сил, действующих на частицу. Уравнение Шредингера является основным уравнением релятивистской механики. Оно не может быть выведено из других соотношений. Шредингер установил свое соотношение, исходя из оптико-механической аналогии. Для одномерного случая уравнение Шредингера имеет вид:
Это уравнение (49.3) совпадает c уравнением (48.1), если U =0. Если же частица движется в силовом поле, характеризуемом потенциальной энергией U, то энергия и импульс связаны соотношением:
Уравнение Шрёдингера в этом случае имеет вид:
Для стационарного силового поля (постоянного во времени)
где E – полная энергия частицы. Тогда дифференциальное уравнение принимает вид:
Сократив на общий множитель exp[-i(E/ħ)t], придем к дифференциальному уравнению, определяющему функцию φ:
Уравнение (49.8) называется – уравнением Шредингера для стационарных состояний. Это уравнение часто записывают в виде (49.9):
В случае стационарного силового поля волновая функция имеет вид (49.6), и тогда:
плотность вероятности равна Квантование энергии
1. Уравнение Шредингера позволяет найти волновую функцию данного состояния и определить вероятность нахождения частицы в различных точках данного пространства. Квантовые числа В квантовой механике доказывается, что уравнению Шрёдингера:
где U - потенциальная энергия, удовлетворяют три квантовых числа. 1) Главное квантовое число n определяет номер энергетического уровни электрона в атоме и может принимать значения: n = 1, 2, 3,... 2) Из уравнения Шредингера следует - момент импульса электрона квантуется:
где l - орбитальное квантовое число, принимающее при заданном n значения: l = 0,1,2,..., (n -1), т.е. всего n значений. Вопросы для повторения
Институт математики, физики и информационных технологий
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 70; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.224.73.125 (0.011 с.) |
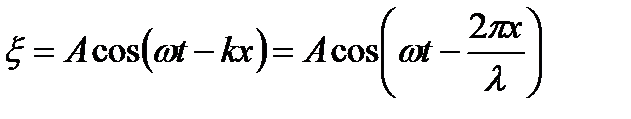 .
.
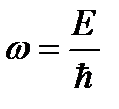 , а
, а  ,
,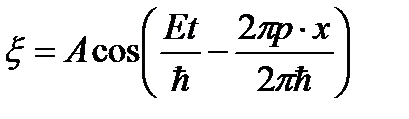 ,
,
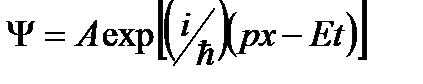 ,
,
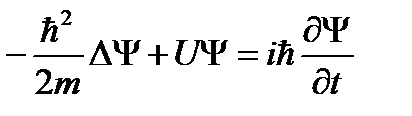 ,
,
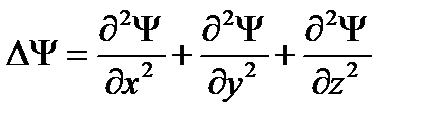 .
.
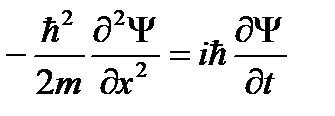 .
.

 .
.
 не зависит от t, тогда:
не зависит от t, тогда: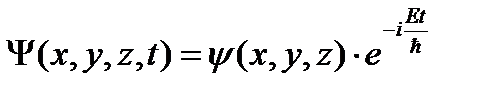 ,
,
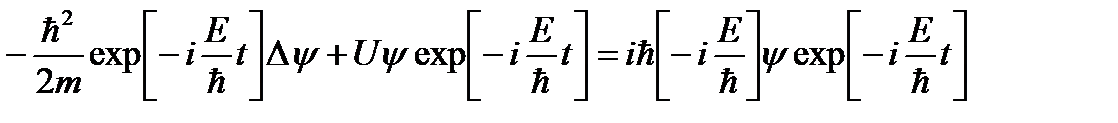 .
.
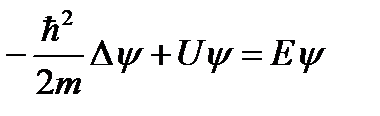 .
.
 .
.
 ,
,
 и, следовательно, от времени не зависит.
и, следовательно, от времени не зависит.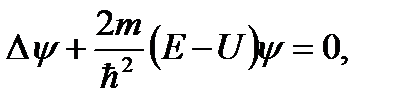
 ,
,



