Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Модели атома Томсона и РезерфордаСодержание книги Поиск на нашем сайте
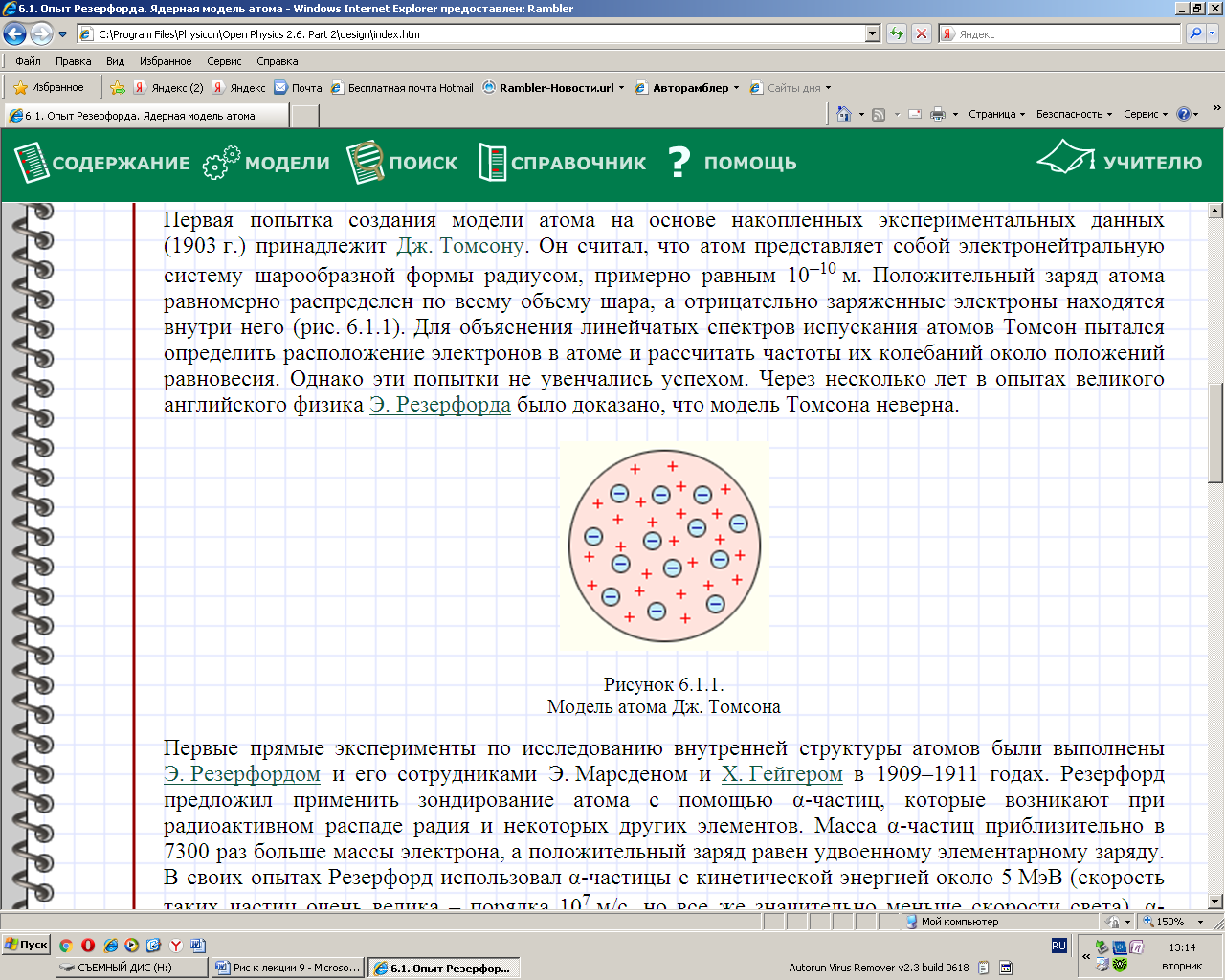
Учение об атомах возникло еще в античные времена. Атомос - в переводе с греческого - неразложимый. Древнегреческий философ Демокрит считал атомы мельчайшими неделимыми частицами вещества. Опытами М.В. Ломоносова и А. Лавуазье была доказана реальность существования атомов. В 1869 г. Д.И. Менделеев при разработке периодической системы элементов, поставил вопрос о единой природе атомов. Затем, во второй половине 19 века было экспериментально доказано, что электрон является составной частью любого атома. В 1903 г. Дж. Дж. Томсон предпринял попытку создать первую модель атома. По модели Томсона атом - это непрерывный, положительно заряженный шар радиусом ~ r = 10-10м, внутри которого около своих положений равновесия колеблются электроны. Суммарный положительный заряд шара равен суммарному отрицательному заряду электронов, и атом в целом электрически нейтрален.
Рис. 43.1. Модель атома Дж. Томсона Однако эта модель оказалась несостоятельной. В 1911 г. Резерфорд предложил ядерную(планетарную) модель атома, после объяснения экспериментальных результатов опыта Резерфорда и его сотрудников по рассеянию α -частиц в веществе. Альфа-частицы возникают при радиоактивных превращениях; они являются положительно заряженными частицами (ядрами атома гелия).
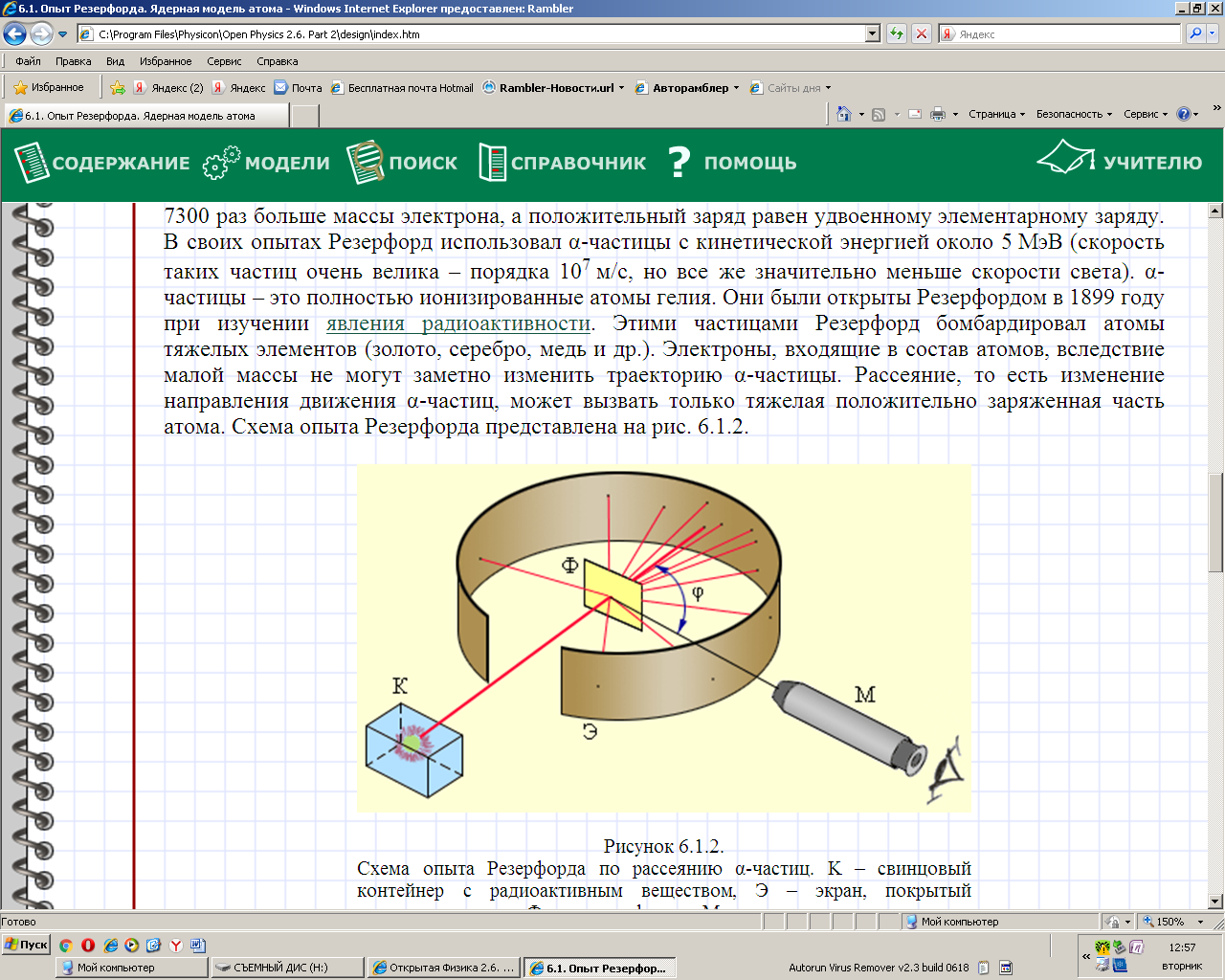
Рис. 43.2 Схема опыта Резерфорда
Опыт Резерфорда осуществляется так (рис. 43.2): узкий пучок α -частиц от радиоактивного препарата - К, падал на тонкую золотую фольгу Ф. После фольги Ф α -частицы отклонялись от первоначального направления на угол φ. Рассеянные частицы ударялись об экран-Э, покрытый сернистым цинком и вызываемые ими вспышки наблюдались в микроскоп - М, который можно было вращать вокруг оси, проходящей через центр фольги, и устанавливать под любым углом. Весь прибор помещался в откачанный кожух, чтобы устранить рассеяние α-частиц за счет столкновения с молекулами воздуха. Оказалось, что некоторое количество α -частиц (примерно 1 из 20000) рассеивается на очень большие углы (α ≈ 180º). Из анализа результатов опыта Резерфорд пришел к выводам:
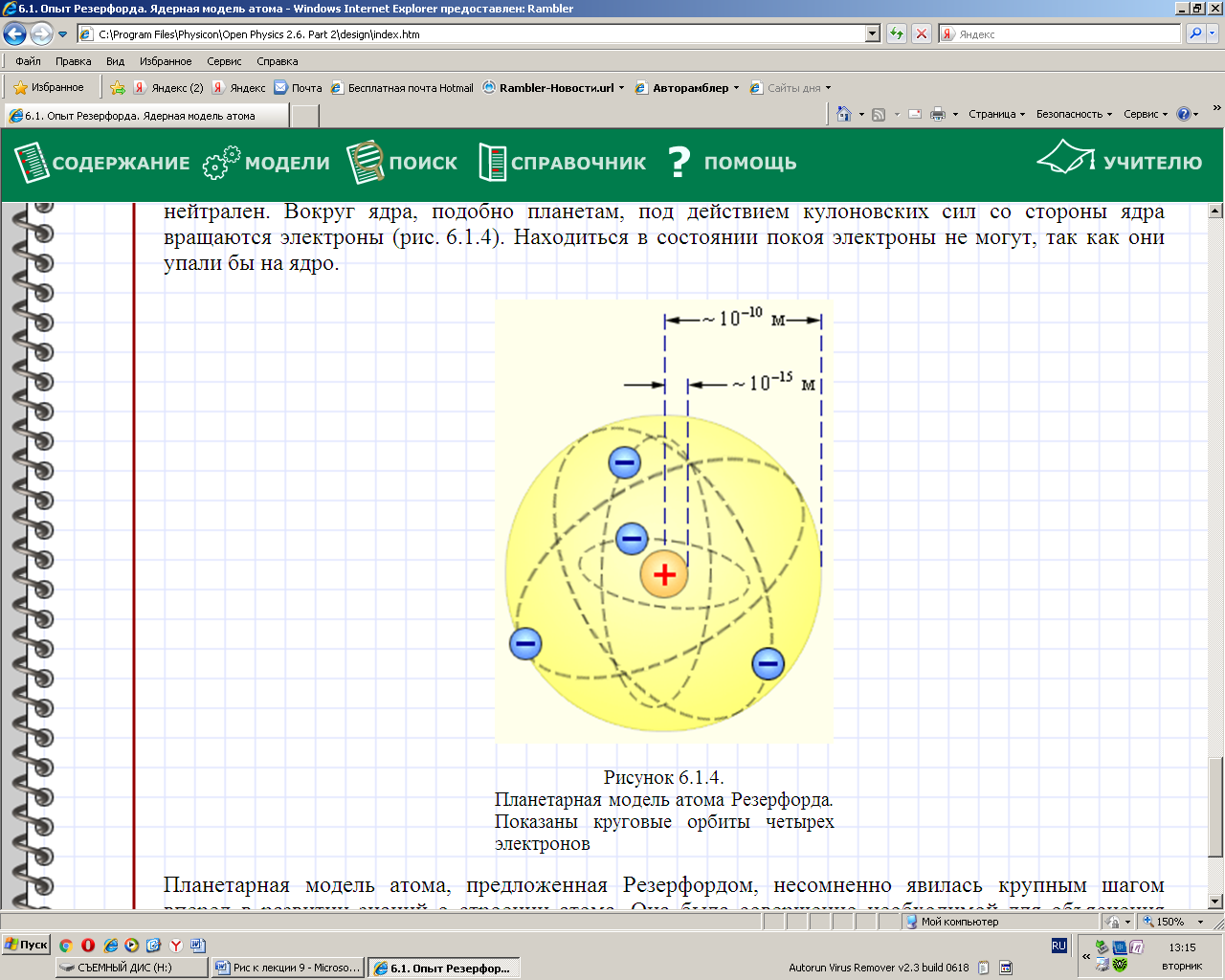
Ядерная (планетарная) модель атома по Резерфорду (рис. 43.3): атом представляет систему зарядов, в центре которой расположено тяжелое положительно заряженное ядро с зарядом Ze, размером 10–14м, а вокруг ядра расположены Z электронов. Почти вся масса атома сосредоточена в ядре.
Рис. 43.3. Планетарная (ядерная) модель атома Резерфорда. Показаны орбиты четырех электронов
Но эта модель оказалась в противоречии с законами классической механики и электродинамики. Согласно этим законам:
Выход из такого тупика был найден в 1913г. Нильсом Бором. Н. Бор ввел допущения, противоречащие классическим представлениям, эти допущения носят название постулаты Бора. I ый постулат Бора: из бесконечного множества электронных орбит, возможных с точки зрения классической механики, в действительности осуществляются только некоторые дискретные орбиты, удовлетворяющие определенным квантовым условиям.
|
||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 178; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.33 (0.008 с.) |