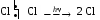Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Формулы в органической химии.Содержание книги
Поиск на нашем сайте
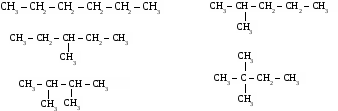
2. Теория химического строения органических соединений А.М. Бутлерова. Химическое строение - определенная последовательность соединения атомов в молекулах веществ. Основные положения теории химического строения. 1. Атомы в молекулах соединены друг с другом согласно их валентности, причем углерод в органических веществах всегда четырехвалентен, а его атомы способны соединяться в цепи линейного, разветвленного и замкнутого строения. Свойства органических веществ определяются не только их качественным и количественные составом, но и порядком связи в молекуле, то есть химическим строением. Атомы в молекулах органических веществ оказывают друг на друга взаимное влияние, от которого зависят свойства вещества в целом. 3. Изомерия органических соединений. Изомеры – вещества, имеющие одинаковый состав молекул, но различное химическое строение и, обладающие поэтому разными свойствами. 1. Изомерия углеродного скелета. Упражнение: составить формулы пяти изомеров вещества, имеющего состав С6Н14.
Лекция.ТЕМА 2.2: ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ. (Парафины. Алканы). Предельными или насыщенными углеводородами называют углеводороды с незамкнутыми углеродными цепями, в молекулах которых все атомы связаны одинарными связями. МЕТАН. 1. Электронное и пространственное строение молекулы метана. Атом углерода имеет электронную формулу 1s2 2s2 2р2, на внешнем энергетическом уровне находится четыре электрона. В невозбужденном состоянии у атома углерода два неспаренных электрона. При переходе в возбужденное состояние один s-электрон переходит на вакантную р-орбиталь, атом углерода становится четырехвалентным. При образований молекулы метана и молекул других предельных углеводородов происходит гибридизация электронных орбиталей. Одна s- и три р-орбитали взаимодействуют между собой, образуя четыре новые, совершенно равноценные орбитали. Такой процесс называется sp3 - гибридизацией. Гибридизация - процесс выравнивания электронных орбиталей по форме и энергии. В результате взаимного отталкивания гибридные орбитали занимают в пространстве самое выгодное положение, поэтому угол между их осями равен 109°28¢ и они направлены по вершинам правильного тетраэдра. Таким образом молекула метана в пространстве представляет собой тетраэдр. 2 Физические свойства метана. Метан в природе. Метан - газ без цвета, вкуса и запаха, легче воздуха, нерастворим в воде. Входит в состав природного газа (до 95%), встречается в каменноугольных шахтах, где представляет большую опасность. 3. Химические свойства метана. 3.1 горение СН4 + 2О2 → СО2 + 2Н2О 3.2 разложение при нагревании
3.3 реакция замещения
Механизм реакции замещения.
Реакция замещения идет по свободно-радикальному механизму. Частицы, имеющие неспаренные электроны, и обладающие поэтому неиспользованными валентностями, называются свободными радикалами. 5. Получение метана в лаборатории.
6. Применение метана. Метан используется как топливо и сырье в химической промышленности.
|
||||||
|
Последнее изменение этой страницы: 2021-02-07; просмотров: 151; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.220.134.161 (0.006 с.) |