
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кафедра пропедевтики внутренних болезнейСтр 1 из 7Следующая ⇒
Министерство здравоохранения Российской Федерации Волгоградский государственный медицинский университет Кафедра пропедевтики внутренних болезней ИНСТРУМЕНТАЛЬНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ В ПУЛЬМОНОЛОГИИ
Методические рекомендации для студентов 3 курса лечебного факультета
Волгоград 2013
Составители: д.м.н., доцент Скворцов В.В., к.м.н., ассистент Родионова И.В.
Рецензенты: профессор кафедры терапии ФПК ППС болезней Саратовского государственного медицинского университета, д.м.н. В.Р.Гриценгер, д.м.н., профессор, зав.кафедрой внутренних болезней Кировской государственной медицинской академии Е.Н.Чичерина.
Аннотация: методические рекомендации предназначены для самоподготовки студентов 3 курса лечебного факультета. В рекомендациях освещены анатомо-физиологические особенности органов дыхания, методы рентгено- и флюорографии, исследования функции внешнего дыхания, бронхоскопии, сцинтипульмонографии, эхокардиографии, КТ и МРТ в практике терапевта, пульмонолога.
Методические рекомендации рекомендованы к изданию цикловой методической комиссией терапевтических дисциплин Волгоградского государственного медицинского университета (протокол N от __________ 20___ года).
Волгоградский государственный медицинский университет 400066, г. Волгоград, пл. Павших борцов, 1.
Волгоград-2013
Оглавление 1. Анатомия и физиология органов дыхания………………………………….....4 2. Рентгенография и флюорография………………………………………………7 3. Исследование функции внешнего дыхания.…………………….......................9 4. Бронхоскопия……………………………………………………………………..23 5. Сцинтиграфия……………………………………………………………………24 6. Возможности ЭхоКГ в пульмонологии………………………………….…….25 7. МРТ и КТ………………………………………………………………………….28 8. Литература…………………………………………………………………………31
Лёгкие и грудная клетка. Грудная или торакальная полость состоит из костного каркаса, рёбер и позвоночного столба. Рёбра подвижно соединены с позвоночным столбом. Внизу грудная полость заканчивается куполообразной мышечной перегородкой - диафрагмой.
Как мы дышим? Вдох и выдох воздуха происходят благодаря ритмичным движениям органов дыхания. Это лёгкие, грудная клетка с относящейся к ней мускулатурой, диафрагма и брюшная стенка. Грудная полость при вдохе Эластичная ткань лёгких обладает свойством сокращаться, в то время как грудная клетка скорее тяготеет к тому, чтобы оставаться в положении вдоха. Вдох происходит благодаря тому, что дыхательная мускулатура поднимает и расширяет грудную клетку, диафрагма опускается; при этом должно быть преодолено эластичное сопротивление грудной клетки и лёгких. При потоке воздуха во время вдоха и выдоха через систему труб дыхательных путей различного диаметра возникает сопротивление, так называемое противодействие току воздуха. Итак, вдох - это активный процесс. При вдохе в дыхательных путях возникает более низкое давление по сравнению с атмосферным давлением. Благодаря этому воздух может пройти в дыхательные пути. Выдох происходит потому, что лёгкое, расширенное во время вдоха, сжимается. Следовательно, при дыхании в покое вдох активный, выдох - пассивный процесс. Во время выдоха в результате сжатия лёгких поднимается давление в бронхах и альвеолах по сравнению с атмосферным давлением и воздух устремляется наружу. Самая главная дыхательная мышца - диафрагма. Она движется вниз в направлении живота, как поршень с возвратно-поступательным движением в автомашине, и расширяет при этом лёгкие. Движение диафрагмы изображено на рисунке, данном выше. При выдохе диафрагма движется вверх. При напряжённом дыхании или сильном выдохе (например, FET) выдох поддерживается мышцами живота.
При дыхании в покое у взрослых 2/3 воздуха перекачивается в лёгкие диафрагмой и только 1/3 - грудной клеткой. Флюорография Флюорография - метод рентгенологического исследования, заключающийся в фотографировании рентгеновского изображения исследуемого объекта со светящегося экрана на фотографическую (флюорографическую) пленку. Различают малоформатную, средне-форматную и крупноформатную флюорографию. В первом случае съемку производят на перфорированную пленку с размером кадра 24x24 мм или неперфорированную с размером кадра 32x32 мм, во втором - на пленку с форматом кадра 70x70 мм, в третьем - 100x100 или 110x110 мм. Флюорограф представляет собой специальный рентгеновский аппарат, снабженный флюоресцентным экраном, фотокамерой и механизмом автоматического перемещения пленки. Современные рентгенодиагностические системы с электронно-оптическими усилителями рентгеновского изображения также снабжены специальными камерами для Ф. Они обеспечивают возможность флюорографии легких, желудка и других органов с частотой до 6 кадров в 1 с. Основная задача флюорографии - проведение массовых обследований населения для выявления скрыто протекающих заболеваний - выполняется как в флюорографических кабинетах поликлиник, медсанчастей, противотуберкулезных диспансеров, больниц, так и с помощью передвижных флюорографических установок, смонтированных на специальных транспортных средствах. Достоинства метода: высокая пропускная способность флюорографических кабинетов, относительно небольшая лучевая нагрузка при исследовании легких, возможность хранения флюорограмм, что позволяет сравнивать рентгеновскую картину у одних и тех же лиц в динамике. Флюорографическое исследование проводится дифференцированно, но не реже чем 1 раз в 3 года; при высоком уровне заболеваемости туберкулезом в области (крае, республике) ежегодно. Лица, у которых обнаружены изменения в легких и сердце, подлежат вызову и первичному рентгенологическому дообследованнию. Архив флюорограмм и картотека позволяют выделить отдельные группы диспансерного наблюдения. Диагностические флюорографические исследования органов грудной полости выполняют при клинико-рентгенол. признаках болезней легких, плевры, диафрагмы и средостения, а также с целью рентгенологического наблюдения за уже распознанными изменениями этих органов. Крупнокадровая флюорография желудка, осуществляемая на специальных гастрофлюорографах с дистанционным управлением и рентгенотелевизионным контролем по специальной программе, позволяет исследовать все категории пациентов как с профилактической, так и с диагностической целью. Пикфлоуметрия Пикфлоуметр − индивидуальный прибор для самоконтроля при бронхиальной астме, фиксирующий пиковую скорость выдоха (ПСВ), то есть максимальную скорость воздушного потока при форсированном выдохе. Пикфлоуметрия является одним из методов диагностики и контроля над течением бронхиальной астмы. Применяют данный метод при любых обструктивных заболеваниях легких, но особенно он важен при бронхиальной астме.
Значение пикфлоуметрии можно сравнить с контролем артериального давления при гипертонической болезни или «сахара» (глюкозы) крови при сахарном диабете. Метод используется для: − установления диагноза и проведения дифференциальной диагностики заболеваний, сопровождающихся обструкцией дыхательных путей; − диагностики профессиональной астмы и установления других провоцирующих факторов; − определения степени тяжести заболевания; − определения степени контроля бронхиальной астмы; − определения эффективности лечения и первых признаков надвигающегося обострения заболевания. Преимущества для пациента при использовании пикфлоуметра: − позволяет контролировать правильность подобранной терапии; − снижает потребность в частых консультациях врача (при правильном истолковании значений); − предупреждает пациента об ухудшении состояния еще до возникновения заметных внешних проявлений заболевания, что позволяет провести своевременную коррекцию терапии. Правила проведения пикфлоуметрии. Итак, каждому больному бронхиальной астмой рекомендована ежедневная пикфлоуметрия. Пикфлоуметрия наиболее информативна при длительным (не менее 3-х недель) и ежедневном применении. На основании эпизодических замеров объективную оценку параметров произвести невозможно. Измерять значение пиковой скорости выдоха (ПСВ) необходимо 2 раза в день. Желательно проводить измерение в одни и те же часы. В случае если пациент не применяет бронходилататоры, измерение проводится утром сразу после сна и вечером перед тем, как лечь спать. Если пациентом уже используются бронхолитики, то утреннее измерение проводится до использования лекарственного препарата, а вечером через 3-4 часа после его применения. Техника использования пикфлоуметра. Пикфлоуметр − средство индивидуального пользования и должен быть всегда чистым перед использованием. − Пикфлоуметрию проводят в положении стоя; пикфлоуметр держат горизонтально; − Присоедините мундштук к пикфлоуметру; − Перед каждым измерением ставьте указатель на отметку ноль; − Не касайтесь пальцами шкалы и не закрывайте отверстия в торце; − Сделайте глубокий вдох; − Обхватите мундштук прибора губами. Сделайте максимально быстрый и сильный выдох через рот (детям объясните, что выдыхать нужно так, как будто гасишь свечи на праздничном торте праздника).
Выдыхаемый воздух оказывает давление на клапан прибора, который перемещает вдоль шкалы стрелку-указатель. Стрелка покажет пиковую скорость выдоха (ПСВ) − Повторите процедуру 3 раза; − Из трех полученных результатов выберите наибольший (наилучший) и отметьте его в дневнике самонаблюдения (рис.).
Рис. Таблица для записи результатов пикфлоуметрии. Примечание: ☼ − утреннее измерение;) − вечернее измерение.
Оценка результатов пикфлоуметрии. Пиковая скорость выдоха (ПСВ) у каждого человека индивидуальна и зависит не только от возраста, пола, веса и роста. Очевидно, что функция легких человека, длительно занимавшегося спортом (плаванием, велоспортом), и функция легких длительно больного бронхиальной астмой будут сильно отличаться друг от друга, даже при условии, что рост, вес, пол и возраст совпадают. В этом случае нужно ориентироваться не на должные (вычисляемые по таблицам среднестатистической нормы) показатели, а на свои лучшие, которые были зафиксированы в процессе лечения. Если у вас бронхиальная астма находится в фазе ремиссии, то есть проявления болезни отсутствуют, то лучший показатель ПСВ определяется в течение 2-3 недель проведения ежедневной пикфлоуметрии в этот период. Для того чтобы помочь пациенту контролировать течение бронхиальной астмы были разработаны специальные зоны (зеленая, желтая, красная). Их можно рассчитать согласно должным значениям ПСВ (на основании специальных таблиц − можете спросить у лечащего врача) или рассчитать самостоятельно, зная свой лучший результат, зафиксированный вне периода обострения (см.выше). В соответствии с этими зонами (зеленая, желтая, красная) врач устанавливает нижние границы значения ПСВ, равные 80% и 60% от должного значения ПСВ (рассчитывается по таблицам) или от лучшего результата (измеряется самостоятельно вне периода обострения).
Расчет границ зон по наилучшему показателю ПСВ (рис). При достижении самых лучших показателей скорости выдоха, приближающихся к нормальным и при отсутствие симптомов астмы, рассчитывают три цветные зоны. Ваш самый лучший показатель пикфлоуметрии умножьте на 0,8. Например, если у Вас лучшее значение пикфлоуметрии равно 600 л/мин, то 600 умножьте на 0,8. Полученный результат − 480 л/мин. Любое значение выше 480 л/мин будет относиться к так называемой зеленой зоне, что означает − нормальный уровень проходимости бронхов. Для определения границ желтой зоны умножьте Ваш лучший показатель на 0,6. Допустим, 600 * 0,6 = 360 л/мин, что будет нижней границей желтой зоны. А верхнюю границу желтой зоны вы уже знаете (ранее подсчитанное значение). Т.е. желтая зона в нашем примере будет находиться между 360 и 480 л/мин. Красная зона находится ниже уровня нижней границы желтой зоны.
То есть, в нашем случае ниже 360 л/мин. Рис.2. "Зеленая зона" − показатель нормы − астма под контролем.
Физическая активность и сон не нарушены, симптомы болезни минимальны или отсутствуют. ПСВ ≥ 80% должных или лучших индивидуальных показателей. Суточный разброс показателей не превышает 20%. Терапия определяется тяжестью течения астмы. "Желтая зона" − сигнал "Внимание". Появляются клинические симптомы астмы в виде кашля, свистящих хрипов, одышки (особенно ночью), тяжести в груди. Снижается активность, нарушается сон. ПСВ составляет 60-80% от должных или лучших индивидуальных значений с суточным разбросом 20-30%. Переход в "желтую зону" указывает на начинающееся или развившееся обострение. Необходим прием препаратов в соответствии с назначениями врача при этой клинической ситуации, при необходимости − усиление терапии. "Красная зона" − зона тревоги. Симптомы астмы присутствуют в покое и при нагрузке. Отмечаются кашель, одышка с участием в дыхании вспомогательной мускулатуры. Значение ПСВ менее 60% от должных или лучших индивидуальных значений с суточным разбросом более 30%. Необходим прием препаратов для экстренной помощи (согласно рекомендованному врачом плану), незамедлительное обращение за медицинской помощью. Переход в "красную зону" свидетельствует о необходимости пересмотра плана медикаментозной терапии в "зеленой зоне". Любое значение пикфлоуметрии в красной зоне должно сопровождаться незамедлительным выполнением действий, согласно инструкции на этот счет вашего лечащего врача (дополнительная ингаляция бронхолитика и прочее), которые вы должны оговорить заранее.
Расчет суточного разброса показателей ПСВ: (ПСВ (веч)− ПСВ(утр))/ 1/2 (ПСВ(веч) + ПСВ(утр)) x 100 Например: ПСВ (веч) = 600 л/мин, ПСВ(утр)=400 л/мин. Расчет: (600-400) / ½ (600+400) x 100% = 40% суточный разброс. Помните, постоянный контроль пиковой скорости выдоха позволяет контролировать течение бронхиальной астмы и своевременно проводить коррекцию терапии.
Бронхоскопия Бронхоскопия - метол исследования трахеи и крупных бронхов, во время которого бронхоскоп помещают в рот, затем проталкивают глубже и с его помощью осматривают трахею. После этого трубку просовывают в один из главных бронхов (левый либо правый). Бронхоскоп - это прямая металлическая трубка с оптической и осветительной системами, позволяющими произвести осмотр нижних дыхательных путей. Сегодня чаще используется не обычный, «жесткий», бронхоскоп, а «гибкий», состоящий из специальных волокон (фибробронхоскоп). Устройство современных приборов таково, что они позволяют проводить ряд дополнительных, кроме осмотра, манипуляций - отсасывание секрета бронхов, биопсию слизистой бронхов и др. Когда необходима бронхоскопия? Существует много причин, по которым пациенту делают бронхоскопию, например, затрудненное дыхание из-за попадания в дыхательные пути инородных тел. Кроме того, если в течение нескольких недель у человека не проходит кашель, то причину этого чаще всего удается установить с помощью бронхоскопии. Бронхоскопию применяют также при наличии в мокроте крови, перед операцией на легких или, в том случае, если в нижние дыхательные пути нужно ввести точную дозу лекарств. Бронхоскопию выполняют и с целью уточнения диагноза, например, бронхогенного рака легких. Для этого во время исследования производится биопсия.
Перед этой диагностической процедурой пациенту запрещается принимать пищу и курить. Если во время бронхоскопии используется твердый металлический бронхоскоп, то процедуру проводят в условиях общей анестезии, если фибробронхоскоп - в условиях местной анестезии. Затем через бронхоскоп врач осматривает нижние дыхательные пути. В зависимости от цели исследования он производит взятие проб для дальнейшего бактериологического, клеточного или тканевого анализа. Он также может осуществить отсос содержимого бронхов или удалить инородные тела небольших размеров. Питье пациенту дают не ранее чем через 2 часа, а пищу по истечении 4 часов после исследования, т. к. следствием наркоза является некоторое нарушение глотания. Преимущества и недостатки бронхоскопии. Бронхоскопия - это сравнительно не опасная диагностическая процедура. Оценка ее результатов позволяет получить сведения о причинах тех болезней, которые не удается диагностировать с помощью других методов исследования. Кроме того, фибробронхоскоп позволяет провести более тщательный осмотр нижних дыхательных путей, т. к. в силу своей эластичности он может намного глубже проникнуть в бронхи. Главным недостатком бронхоскопии является то, что эта процедура малоприятна для пациента. Во время ее проведения возможны повреждение стенки бронха и кровотечение из слизистой оболочки бронхов. Слабая боль или кровотечение после бронхоскопии наблюдаются довольно часто, не следует обращать на эти симптомы много внимания. Однако если эти симптомы усиливаются, то необходимо обратиться к врачу. Сцинтиграфия Что такое сцинтиграфия легких? На сцинтиграмме легких виден моментный снимок легких. Различают два метода сцинтиграфии легких: перфузионный и вентиляционный. Перфузионная сцинтиграфия основана на визуализации кровотока из правого желудочка в легочные артерии и распределении крови в легких. Вентиляционная сцинтиграфия позволяет увидеть, как воздух поступает в отдельные доли легких. Сцинтиграфию легких выполняют после введения в кровеносные сосуды или бронхи радиоактивных веществ. Затем с помощью специальных приборов определяют локализацию поражений. В каких случаях проводят сцинтиграфию легких? Сцинтиграфия легких очень информативна при подозрении на бронхогенный рак легких. Примерно в 70% случаев рака бронхов патологический процесс локализуется в корне легкого. При центральном раке бронхов нарушается кровообращение в легких. На сцинтиграмме можно увидеть то, что нельзя визуализировать на рентгеновском снимке. Сцинтиграфию легких выполняют и при подозрении на тромбоэмболию легочной артерии. Исследование позволяет определить местонахождение эмбола. Как проводят сцинтиграфию легких? Во время перфузионной сцинтиграфии пациенту внутривенно вводят частицы белка, меченные радиоактивными изотопами. Размеры частиц таковы, что они не могут пройти через мельчайшие легочные артериолы и капилляры. Они на некоторое время застревают и начинают испускать гамма-лучи. С помощью специальных камер они превращаются в изображение. Таким образом исследуется перфузия легочных капилляров. По количеству частиц белка, меченных изотопами, которые застряли в местах поражения, можно выявить ослабление или отсутствие кровообращения в легком. При проведении вентиляционной сцинтиграфии пациент вдыхает радиоактивный газ до тех пор, пока в легких не устанавливается равновесие газов. Если при выявлении дефекта перфузии отсутствуют нарушения вентиляции в этой зоне, то диагноз тромбоэмболия легочной артерии высоковероятен. Частицы, отмеченные технецием или другими изотопами, излучают гамма-лучи. Таким образом можно эффективно выявить дефект перфузии легких. Гамма-камера используется для фиксации изображений, полученных с помощью излучения, испускаемого изотопами. Картина распределения и накопления радионуклида дает врачу четкое представление о топографии, форме и размерах легких, а также о наличии в них различных патологических очагов или изменении их функции. В тот момент, когда пациент выдыхает газ, используемый для исследования, выполняется еще несколько снимков легких. Опасна ли сцинтиграфия легких? Болевые ощущения возникают у пациента только при введении иглы в вену. Во время исследования самочувствие пациента стабильно, тошнота и головная боль не наблюдаются. Разовая лучевая нагрузка очень незначительна. Исследование позволяет получить ценную информацию об анатомических изменениях и функциональных нарушениях легких. Правда, действие, которое оказывают радиоактивные вещества на организм, до конца не изучено, поэтому пока нельзя утверждать, что исследование является абсолютно безопасным для здоровья человека. Для фиксирования лучей, испускаемых радиоактивными частицами, нужно специальное оборудование. Сцинтиграфия регистрирует распределение интенсивности излучения радиоактивного препарата после введения его в организм. Гамма-камера позволяет увидеть легкие. Курильщики, страдающие хроническим кашлем, должны обратиться к врачу. Правда, кашель еще не означает наличия рака, однако он является одним из характерных симптомов этой болезни. Сцинтиграфия легких позволяет быстрее обнаружить раковую опухоль. Иногда полученные результаты могут быть интерпретированы двояко. В таких случаях для уточнения диагноза проводится ангиография. Во время этого исследования в кровеносный сосуд малого круга кровообращения вводят контрастное вещество, затем делают рентгеновский снимок. Для уточнения диагноза необходим один, а иногда несколько снимков. Легочное сердце Согласно определению Всемирной организации здравоохранения под легочным сердцем(ЛС) понимают изменения ПЖ – только его гипертрофию либо сочетание гипертрофии с дилатацией или недостаточностью, которые возникают вследствие функциональных и/или структурных изменений в легких и не связаны с первичной недостаточностью левых отделов или врожденными пороками сердца. По мнению многих специалистов, занимающихся проблемой ЛС, это определение требует коррекции. Во первых, в нем не упомянута легочная гипертензия, хотя она существенно влияет на последующие изменения ПЖ. Во вторых, к настоящему времени накоплены данные о ранних изменениях ЛЖ при хроническом легочном сердце(ХЛС). В_третьих, появились сведения о новых важных механизмах формирования легочной гипертензии и правожелудочковой недостаточности. А.Г. Чучалин и соавт. определяют ЛС как синдром, характеризующийся перегрузкой и гипертрофией правых отделов сердца, которые в значительной мере связаны с повышением сопротивления сосудов малого круга кровообращения при ряде хронических заболеваний легких, тромбоэмболии легочной артерии, первичной легочной гипертензии и т.д. Этот термин не используется для описания изменений ПЖ при патологии левых отделов сердца, врожденных и приобретенных пороках сердца. Любой патологический процесс в легких, вызывающий легочную гипертензию, может привести к ЛС. Чаще всего причиной ЛС служит хроническая обструктивная болезнь легких, но ЛС может развиваться и при тромбоэмболии легочной артерии, муковисцидозе, коллагенозах, саркоидозе, ожирении и др. Различают острое и хроническое легочное сердце. Главная причина острого ЛС – тромбоэмболия легочной артерии, хронического ЛС – хронические заболевания легких. Следует заметить, что к формированию ХЛС иногда приводят повторные тромбоэмболии ЛА. В целом все патологические процессы, осложняющиеся развитием ХЛС, могут быть условно объединены в три большие группы. 1. Заболевания бронхолегочного аппарата – хроническая обструктивная болезнь легких, фиброз легких, врожденная патология легких (муковисцидоз, гипоплазия и т.д.), гранулематозы. 2. Заболевания с первичным поражением легочных сосудов – системные васкулиты, повторные тромбоэмболии мелких ветвей ЛА, первичная легочная гипертензия. 3. Торакодиафрагмальные поражения – деформации грудной клетки, ожирение, миастения. По мнению многих авторов, первопричиной изменений легочной гемодинамики при формировании ХЛС следует считать альвеолярную гипоксию при нарастающей неравномерности альвеолярной вентиляции, что приводит к артериальной гипоксемии и затем – к повышению тонуса мелких артерий и артериол легких с развитием легочной артериальной гипертензии. Повышение тонуса в артериальной системе малого круга кровообращения может быть исключительно нейрогенным, т.е. возникать в результате усиления симпатической стимуляции сосудов малого круга. Важная роль в формировании указанных реакций принадлежит изменению функции эндотелия легочных сосудов. Длительное повышение давления в ЛА приводит к гипертрофии, а с течением времени – к дилатации и недостаточности ПЖ. Как острое, так и хроническое ЛС имеет свои признаки на ЭхоКГ: повышение давления в ЛА, расширение ПЖ и правого предсердия (ПП), дрожание и парадоксальное движение межжелудочковой перегородки. В тяжелых случаях резкое увеличение размеров ПЖ приводит к сдавлению ЛЖ и нарушает его наполнение, что проявляется диастолической дисфункцией ЛЖ. Кроме того, при ХЛС выявляется гипертрофия ПЖ. Измерение давления в ЛА Измерение давления в ЛА является одним из ключевых моментов ЭхоКГ исследования. Расчет давления в ЛА можно провести следующими способами: • по отношению времени ускорения потока в выносящем тракте ПЖ к времени выброса (среднее давление в ЛА); • по скорости струи трикуспидальной регургитации (максимальное систолическое давление в ЛА); • по скорости потока легочной регургитации (конечно диастолическое давление в ЛА). Для расчета среднего давления в ЛА по отношению времени ускорения потока в выносящем тракте ПЖ к времени выброса (АТ/ЕТ) измерения проводят в режиме импульсного допплеровского исследования. В норме отношение АТ/ЕТ составляет 0,4–0,45 (рис. 1), а среднее давление в ЛА не превышает 20 мм рт. ст. Уменьшение показателя АТ/ЕТ указывает на повышение среднего давления в ЛА, которое определяют по следующей номограмме: Расчет максимального систолического давления в ЛА по скорости струи трикуспидальной регургитации проводится следующим образом. Учитывая, что разница систолического давления в ПЖ и ЛА незначительна (при отсутствии стеноза клапана ЛА), ей можно пренебречь и принять эти показатели равными. Тогда систолическое давление в ЛА равно сумме давления в ПП и максимального градиента давления между ПЖ и ПП. Для расчета систолического давления в ЛА измеряют максимальную скорость потока трикуспидальной регургитации в непрерывноволновом допплеровском режиме и с помощью упрощенного уравнения Бернулли рассчитывают градиент давления между ПЖ и ПП (эта формула заложена в современных приборах). Давление в ПП принимают равным 5 мм рт. ст., если правые отделы сердца и нижняя полая вена (НПВ) не расширены и НПВ спадается на вдохе не менее чем на 50%. Если правые отделы сердца расширены, но нет расширения НПВ и ее реакция на вдох сохранена, то давление в ПП принимают равным 10 мм рт. ст. Если имеется дилатация правых отделов сердца и НПВ, причем НПВ спадается на вдохе <50%, то давление в ПП составляет 15 мм рт. ст. При значительной дилатации ПЖ, ПП, НПВ и печеночных вен, а также при отсутствии реакции НПВ на вдох давление в ПП составляет около 20 мм рт. ст. В норме систолическое давление в ЛА не превышает 30 мм рт. ст., а по степени его повышения можно оценить выраженность легочной гипертензии: 30–50 мм рт. ст. – умеренная легочная гипертензия; 50–80 мм рт. ст. – значительная; >80 мм рт. ст. – выраженная. Конечно-диастолическое давление (КДД) в ЛА рассчитывают по скорости потока легочной регургитации. В диастолу давление в ЛА в норме составляет около 14 мм рт. ст., в ПЖ – около 5 мм рт. ст. Разность этих величин измеряют в непрерывноволновом допплеровском режиме по скорости потока легочной регургитации в конце диастолы (рис. 3). С помощью уравнения Бернулли рассчитывают градиент давления между ПЖ и ЛА в конце диастолы. КДД в ЛА вычисляется как сумма давления в ПП и градиента конечно_диастолического давления между ПЖ и ЛА. Другие возможности ЭхоКГ. С помощью ЭхоКГ можно оценить состояние клапана ЛА (выявить стеноз ЛА или недостаточность клапана ЛА), а также измерить диаметр ствола ЛА, который в норме составляет 0,9–2,9 см. При увеличении диаметра ствола ЛА можно заподозрить наличие аневризмы ЛА. Патология клапана ЛА редко бывает приобретенной, чаще всего встречается врожденный порок – стеноз легочной артерии. Как и в случае с митральной и трикуспидальной регургитацией, незначительная легочная регургитация встречается у большей части здоровых людей. ЭхоКГ позволяет выявить наличие жидкости в полости перикарда. В норме полость перикарда, заключенная между его париетальным и висцеральным листками, содержит 10–50 мл серозной жидкости. При появлении выпота листки перикарда разделяются, создавая эхонег ативное пространство. ЭхоКГ достоверно выявляет наличие жидкости в полости перикарда, но не позволяет точно измерить ее объем, поскольку нет позиции, из которой был бы виден весь перикард. Однако иногда в клинической практике для приблизительной оценки количества жидкости используют формулу Тейхольца. За конечный диастолический размер принимают диаметр всего перикарда, за конечный систолический размер – диаметр всего сердца. Разность этих объемов (по формуле Тейхольца – ударный объем) будет приблизительно соответствовать количеству жидкости в перикарде. Объем жидкости до 150 мл расценивают как незначительный, 150–500 мл – умеренный, >500 мл – большой. Судить о происхождении выпота по данным ЭхоКГ затруднительно: транссудат, экссудат и кровь выглядят одинаково. С помощью ультразвукового исследования можно установить наличие плеврального выпота. Как и в случае с перикардиальным выпотом, между висцеральным и париетальным листками плевры выявляется эхонегативное пространство. Ультразвуковое исследование помогает определить локализацию максимального скопления ж идкости в плевральной полости, чтобы выбрать оптимальное место для возможной плевральной пункции. Кроме того, с помощью данного метода можно контролировать количество жидкости в полости перикарда и в плевральных полостях в процессе лечения, что позволяет оценить эффективность терапии и уменьшить количество рентгенологических обследований. Таким образом, вовремя назначенное эхокардиографическое исследование и грамотная интерпретация полученных результатов в ряде ситуаций помогают врачу-пульмонологу правильно выбрать тактику лечения или скорректировать ранее назначенную терапию. МРТ и КТ Магнитно-резонансная томография легких. Современный этап развития медицины характеризуется широким внедрением в клиническую практику сложных инструментальных методов исследования, которые зачастую меняют представления об особенностях течения того или иного заболевания. Несмотря на большое число методов исследования, продолжаются поиски новых путей изучения внутренних органов, причем особое внимание уделяется таким критериям, как неинвазивность, безопасность, высокая информативность. К настоящему времени сформировалось мнение о том, что МРТ является неэффективным методом в оценке состояния паренхимы легких. Существует три основных причины, на которые ссылаются сторонники этого утверждения: МРТ легких не является рутинным методом из-за сложности проведения исследования, возможности МРТ в этой области не изучены и поэтому считаются ограниченными, утвердившийся авторитет РКТ, как «золотого стандарта» в этой области исследований, нивелирует информационные возможности МРТ. Между тем, внедрение новых технологических приемов в течение последних 5-10 лет, позволило стать магнитно-резонансной томографии альтернативным методом в исследовании легких. МРТ позволяет дифференцировать ткани по времени релаксации (Т1, Т2), протонной плотности, применяя широкий спектр контрастных препаратов и различные технические возможности пульсовых последовательностей (жироподавление, миелография, динамическое сканирование и др.), а также различного рода ЭКГ и дыхательные синхронизаторы. В качестве контрастных препаратов предлагаются соединения гадолиния (для исследования тканевых образований и изучения перфузии легких), кислород и гиперполяризованные газы для изучения вентиляционных способностей легких. Хронические неспецифические заболевания легких. Потенциальные возможности магнитно-резонансной томографии в исследовании хронических инфильтративно-воспалительных процессов легочной паренхимы (ХНЗЛ) обоснованы в работах Мак-Фаддена с соавторами (1987). Авторы установили корреляцию между клиническими проявлениями ХНЗЛ и МР-признаками, установлены релаксационные характеристики паренхимы в норме и при ХНЗЛ. Сравнительные исследования, проведенные нами, указывают на превосходство РКТ в оценке фиброзных процессов, а МРТ при выявлении активного альвеолита. Последовательности на основе протонной плотности и Т1ВИ имеют высокую чувствительность к наличию паренхиматозных узлов, утолщенных интерлобулярных перегородок, снижение воздушности паренхимы. Снижение воздушности паренхимы легочной ткани, как следствие воспалительных изменений, включая альвеолит, пневмонию и гранулематозные воспалительные изменения, подтверждено в 90% случаях. Консолидированные участки фиброза дают изоинтенсивный сигнал с мышечной тканью на Т1ВИ в 70% случаев. После внутривенного введения контрастного препарата в 50% исследований прослеживается кольцеобразное усиление интенсивности сигнала по периферии очагов фиброза. На Т2ВИ очаги имеют гипоинтенсивный сигнал в сравнении со скелетной мышечной тканью зоной повышенной интенсивности в центре. Очаговые образования паренхимы легких. Визуализация легочных паренхиматозных очаговых образований при МРТ достигается подавляющим количеством применяемых последовательностей. Получаемый сигнал, при этом, по высокой контрастности между паренхимой и образованием, может быть сравним с сигнало
|
||||||||||||
|
Последнее изменение этой страницы: 2021-03-10; просмотров: 86; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.227.24.209 (0.107 с.) |
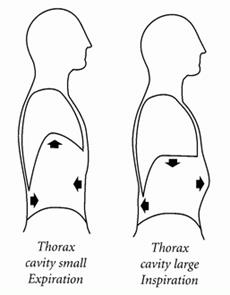 Рёбра связаны между собой мышцами и активно участвуют в процессе дыхания. Лёгкие покрыты висцеральной плеврой (Pleura pulmonalis или visceralis), и с внутренней стороны плотно прилегают к грудной полости. Грудная полость тоже покрыта тонкой слизистой плёнкой - (Pleura parietalis) -пристеночной или париетальной плеврой. Слой жидкости, находящийся в узкой щели между двумя слизистыми оболочками, препятствует образованию трения при движении лёгких, и способствует прочному сцеплению висцеральной плевры с рёберной плеврой. Таким образом лёгкие подвешены в грудной полости и следуют движениям грудной клетки, и наоборот, грудная клетка следует эластичной тяге лёгких при выдохе.
Рёбра связаны между собой мышцами и активно участвуют в процессе дыхания. Лёгкие покрыты висцеральной плеврой (Pleura pulmonalis или visceralis), и с внутренней стороны плотно прилегают к грудной полости. Грудная полость тоже покрыта тонкой слизистой плёнкой - (Pleura parietalis) -пристеночной или париетальной плеврой. Слой жидкости, находящийся в узкой щели между двумя слизистыми оболочками, препятствует образованию трения при движении лёгких, и способствует прочному сцеплению висцеральной плевры с рёберной плеврой. Таким образом лёгкие подвешены в грудной полости и следуют движениям грудной клетки, и наоборот, грудная клетка следует эластичной тяге лёгких при выдохе.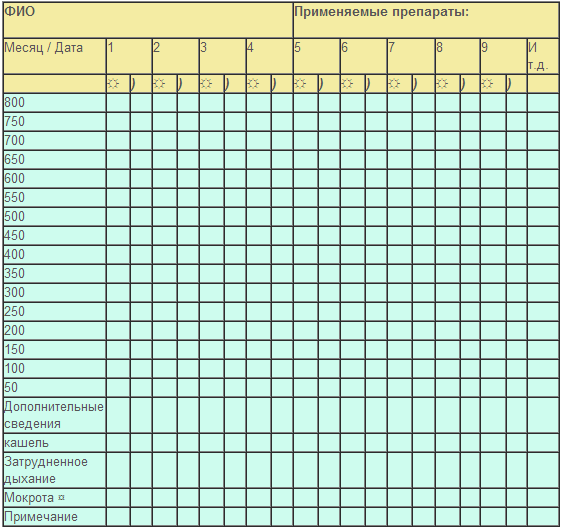

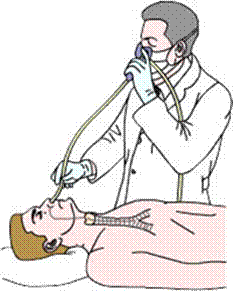 Как выполняют бронхоскопию?
Как выполняют бронхоскопию?


