Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Работа 8. Спектрофотометрический анализ двухкомпонентной смеси
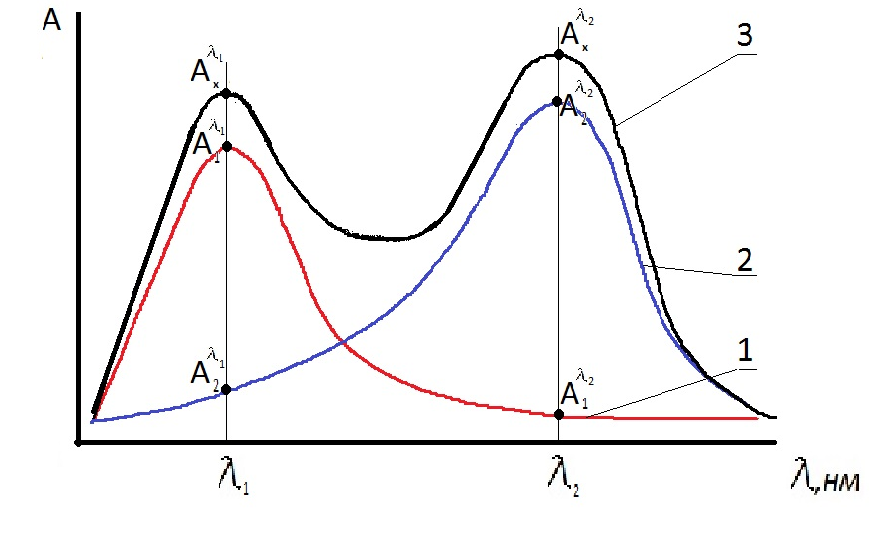
Метод спектрофотометрии позволяет определять несколько компонентов смеси без их предварительного разделения. Оптическая плотность любой смеси, содержащей несколько окрашенных компонентов, не взаимодействующих между собой, подчиняется закону аддитивности, т.е. равна сумме оптических плотностей компонентов смеси при одной и той же длине волны: А = А 1 + А 2 + ….. + А п. Согласно основному закону светопоглощения оптическая плотность каждого компонента равна А i = ε i l C i . (1) Если спектры двух красителей накладываются друг на друга, но имеют разные λ max, то для каждой длины волны λ max оптическая плотность смеси определяется уравнениями при λ 1: А х λ 1 = ε 1 λ 1 l C 1 + ε 2 λ 1 l C 2, (2) при λ 2: А х λ 2 = ε 1 λ 2 l C 1 + ε 2 λ 2 l C 2, (3) где С 1 и С 2 –концентрации 1 и 2-го красителя; ε 1 λ 1и ε 2 λ 1 – коэффициенты поглощения 1 и 2-го красителя при длине волны λ 1; ε 1 λ 2и ε 2 λ 2–коэффициенты поглощения 1 и 2-го красителя при длине волны λ 2; l – толщина поглощающего слоя раствора (кюветы). Для экспериментального нахождения значений ε 1 и ε 2 при λ 1 и λ 2 измеряют величины оптической плотности стандартных растворов каждого красителя при разных длинах волн и вычисляют коэффициенты поглощения по формуле (1). В результате решения системы линейных уравнений (2) и (3) формулы для расчета концентраций двух красителей, находящихся в смеси, имеют вид: На рисунке 2.3 показаны все оптические плотности: – стандартных растворов красителей (А 1 λ 1 и А 1 λ 2; А 2 λ 1 и А 2 λ 2) – их смеси (А x λ 1 и А x λ 2). C 1o и C 2o – концентрации стандартных растворов красителей. Цель работы: Определение содержания двух красителей при их совместном присутствии в растворе. Реагенты, посуда, приборы Водный раствор 1-го красителя, С 1= 0,23 г/л. Водный раствор 2 -го красителя, С 2 = 0,23 г/л. Мерные колбы вместимостью 50,00 мл.
Спектрофотометр. Кюветы 1 = 1 см. Выполнение работы 1. Приготовление стандартных растворов двух красителей с концентрацией C 1o и C 2o. В мерных колбах V к = 50,00 мл разбавляют раствор каждого красителя с концентрациями C 1 и C 2 в 20 раз. 2. Измеряют оптическую плотность приготовленных стандартных растворов и анализируемого раствора, т.е раствора смеси красителей, в диапазоне длин волн 400 - 680 нм с шагом ∆ λ = 10 нм. Результаты заносят в таблицу 2.7. На одном графике строят три спектра поглощения А = f (λ): стандартных растворов красителей и анализируемого раствора смеси красителей. 3. На спектрах для 1 и 2-го красителя находят λ max (длину волны, которой соответствует наибольшая величина оптической плотности). Измеряют оптические плотности стандартных растворов красителей и анализируемого раствора при λ 1 – А 1 λ 1, А 2 λ 1, А x λ 1 и при λ 2 – А 1 λ 2; А 2 λ 2 А x λ 2. Данные вносят в таблицу 2.8. 4. Рассчитывают концентрации каждого красителя в смеси по формулам (4) и (5).
Рисунок 2.3 – Спектры поглощения растворов красителей (1), (2) и их смеси (3)
Таблица 2.7 – Светопоглощение растворов красителей
Таблица 2.8 – Данные для определения состава смеси
2.1.4. Контрольные вопросы 1. На чем основан метод спектрофотометрии в видимой области спектра? 2. Каким энергетические переходы происходят при поглощении излучения видимой области молекулами определяемого соединения? 3. Перечислите основные параметры электромагнитного излучения. 4. Напишите уравнение Планка для характеристики электромагнитного излучения. 5. Что такое спектр поглощения? Как его изображают графически в видимой области? 6. С какой целью снимают спектр анализируемого соединения?
7. Нарисуйте блок-схему спектрофотометра, назовите основные узлы прибора и их назначение. 8. Какие характеристики используют для оценки степени поглощения раствором определяемого вещества видимого излучения? 9. Сформулируйте основной закон светопоглощения. Запишите его выражение. Как его используют в фотометрии? 10. Что представляет собой молярный коэффициент поглощения ε и что он характеризует? Как можно определить ε? 11. С какой целью снимают градуировочный график А = f (С)? 12.Приведите последовательность проведения анализа прямым фотометрическим методом. 13. Какие факторы влияют на выбор толщины кюветы? 14. Что такое раствор сравнения и для чего его применяют? 15. Назовите условия проведения анализа методом прямой фотометрии в видимой области спектра. 16. Толщина поглощающего слоя раствора увеличена в три раза. Как изменится оптическая плотность раствора? 17. Концентрация раствора увеличена в 2 раза. Как изменится оптическая плотность раствора? 18. Рассчитайте молярный коэффициент поглощения, если при измерениях использовали кювету толщиной 5 см, измеренная оптическая плотность раствора красителя равна 0,490, концентрация красителя – 2.10–4 М. 19. В каком случае разбавляют анализируемый раствор? Как подбирают и проводят разбавление? 20. Как оценить воспроизводимость и правильность результатов определения? Фотометрическое титрование Метод фотометрического титрования основан на последовательном измерении поглощения раствора в процессе титрования и установлении зависимости между оптической плотностью раствора А (или пропусканием Т) и объемом прибавленного титранта. Фотометрическое титрование проводят при определенной длине волны, которую выбирают по предварительно снятым спектрам поглощения исходного раствора и раствора с избытком титранта. Излучение, поглощаемое раствором, должно подчиняться закону Бугера-Ламберта-Бера. В этом случае наблюдается прямолинейная зависимость между оптической плотностью титруемого раствора и объемом титранта. Объем титранта в конечной точке титрования V ктт находят по кривой титрования как точку пересечения ее линейных участков. Концентрацию определяемого соединения, зная V ктт, рассчитывают на основании закона эквивалентности. Фотометрическое титрование обычно используют при поглощении веществом излучения в видимой области спектра. Необходимо, чтобы один из компонентов реакции – определяемое вещество, титрант или продукт реакции – имел характерную полосу поглощения, т.е. был окрашен (безинди каторное титрование). Если ни один из участников реакции не поглощает излучение, то можно проводить титрование с индикатором. В качестве индикатора в титруемую систему вводят новое вещество, которое образует окрашенное соединение с одним из компонентов реакции. Основным условием выполнения определения методом фотометрического титрования является резкое изменение оптической плотности титруемого соединения в точке эквивалентности. Метод фотометрического титрования имеет ряд преимуществ перед визуальным методом индикации КТТ. Он отличается большей чувствительностью, правильностью, избирательностью, дает возможность автоматизировать процесс титрования.
|
||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 384; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.46.36 (0.016 с.) |
|||||||||||||||||||||||||||||||||||||

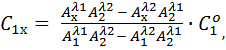 (4)
(4)  (5)
(5)