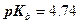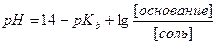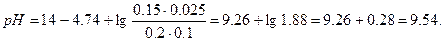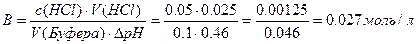Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Занятие № 6 Тема: «Кислотно-основное равновесие в организме. Водородный показатель биологических жидкостей. Буферные растворы». ⇐ ПредыдущаяСтр 9 из 9
1. Актуальность темы: Поддержание кислотно-основного и электролитного равновесия в тканях, биологических жидкостях крайне важно для нормального функционирования организма. Изменение электролитного состава приводит к изменению реакции среды биологических жидкостей. Во-первых, ионы Н+ оказывают каталитическое действие на многие биохимические превращения. Во-вторых, ферменты и гормоны проявляют биологическую активность только в строго определенном интервале значений рН (например, фермент пепсин, участвующий в расщеплении пищи в желудке, активен только при рН = 1,5). В-третьих, даже небольшие изменения концентрации ионов Н+ ощутимо влияют на величину осмотического давления в этих жидкостях. Поддержание постоянного рН в крови и тканевых жидкостях регулируется с помощью нескольких буферных систем. Одним из способов диагностики заболеваний является определение рН желудочного сока, крови, мочи. 2. Цель обучения: Знать основные положения теории электролитической диссоциации; понятие о сильных и слабых электролитах; понятие о буферных растворах; механизм действия буферных растворов; буферные системы организма. Уметь решать расчетные задачи по вычислению концентрации ионов водорода и рН растворов сильных и слабых электролитов; решать расчетные задачи на вычисление рН буферных растворов; буферной ёмкости. 3. Вопросы для обсуждения: 1. Диссоциация воды. Ионное произведение воды. 2. Водородный показатель. Шкала рН. рН биологических жидкостей. Ацидоз, алкалоз. 3. Теория кислот и оснований Аррениуса, Бренстеда-Лоури, Льюиса. 4. Типы протолитических реакций: нейтрализации, гидролиза, ионизации. 5. Гидролиз солей, типы гидролиза. Степень и константа гидролиза. Факторы, влияющие на степень гидролиза. 6. Роль гидролиза в биохимических процессах. 7. Буферные растворы. Классификация и химический состав. 8. Механизм буферного действия (гидрокарбонатного, фосфатного, ацетатного, аммиачного). 9. Расчёт pH буферных растворов. Уравнения Гендерсона–Хассельбаха для кислотного и основного буферных растворов. 10. Буферная ёмкость. Определение. Формулы для расчёта. Факторы, влияющие на буферную ёмкость. 11. Буферные системы крови. Понятие о кислотно-основном равновесии.
4. Ситуационные задачи:
1. Выполнить тестовые задания (письменно):
6. Задачи для самостоятельного решения (выполнить письменно):
7. Вспомогательные материалы по самоподготовке: Приложение 1
Таблица трехзначных десятичных логарифмов | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 | 000 | 041 | 079 | 114 | 146 | 176 | 204 | 230 | 225 | 279 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 | 301 | 322 | 342 | 362 | 380 | 398 | 415 | 431 | 447 | 464 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 | 477 | 491 | 505 | 519 | 532 | 544 | 556 | 568 | 580 | 591 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4 | 602 | 613 | 623 | 634 | 644 | 653 | 669 | 672 | 681 | 690 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5 | 699 | 708 | 716 | 724 | 732 | 740 | 748 | 756 | 763 | 771 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 6 | 778 | 785 | 792 | 799 | 806 | 813 | 820 | 826 | 833 | 839 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 7 | 845 | 851 | 857 | 863 | 869 | 875 | 881 | 887 | 892 | 898 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 8 | 903 | 909 | 914 | 919 | 924 | 929 | 965 | 940 | 945 | 949 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 9 | 954 | 959 | 964 | 969 | 973 | 978 | 982 | 987 | 991 | 996 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Пример расчета pH по [H+]: [H+]=5.3∙10-1 моль/литр
pH=-lg[H+]=-lg5,310-1=-(0.724-1)=-(-0.276)=0.28
Приложение 2
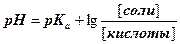
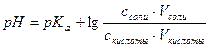 ;
; 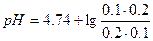 =4.74
б) При добавлении раствора NaOH:
=4.74
б) При добавлении раствора NaOH: 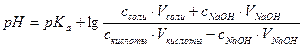
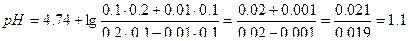
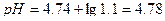 Изменение pH составляет 4.78-4.74=0.04
В) При разбавлении в 15 раз:
Изменение pH составляет 4.78-4.74=0.04
В) При разбавлении в 15 раз: 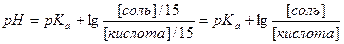 При разбавлении буферного раствора pH не изменется.
При разбавлении буферного раствора pH не изменется.