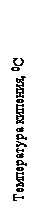Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Режимы проведения ректификационных процессов в лаборатории.Содержание книги
Поиск на нашем сайте Введение
Одним из основных процессов разделения жидких многокомпонентных смесей в промышленности основного органического и нефтехимического синтеза является ректификация. Данный процесс отвечает специфике указанных отраслей, прежде всего крупнотоннажности производств и требованию достаточно высокой степени чистоты получаемых продуктов. Последнее является показателем эффективности работы ректификационных установок, который зависит как от конструктивных особенностей колонны и физико-химических свойств разделяемой смеси, так и от выбора оптимального технологического режима. На стадии исследования физико-химических свойств разделяемой смеси и оценки возможности ее разделения ключевая роль отводится лабораторным методам исследования – периодической и непрерывной ректификации. Непрерывная ректификация позволяет определить статические параметры работы колонны при разделении жидкой многокомпонентной смеси известного состава. Основное значение периодической ректификации заключается в определении структуры диаграммы парожидкостного равновесия с целью качественной и количественной идентификации компонентов смеси.
Ректификация. Ректификация — процесс переноса компонента (компонентов) между жидкой и насыщенной конденсирующейся паровой фазами при противотоке этих фаз. Организация потоков пара и жидкости, а также их взаимодействие реализуются в специальных массообменных аппаратах — ректификационных колоннах. Поток пара создается за счет подвода теплоты (энергии) в выносной кипятильник ректификационной установки и испарения в нем части нижнего продукта. Поток жидкости (флегмы или орошения) организуется за счет возврата в колонну конденсата уходящего с верха колонны пара. Процесс тепломассообмена заключается в непрерывном обмене компонентами между жидкой и паровой фазами. Стекающая вниз жидкая фаза обогащается тяжелокипящим компонентом, а поднимающийся пар – легкокипящим. Взаимодействие потоков осуществляется на специальных контактных устройствах, размещенных по высоте ректификационной колонны. Можно выделить три основных типа массообменных устройств: тарельчатые, насадочные и пленочные. При расчете процесса ректификации оперируют понятием «теоретической тарелки», т.е. тарелки, на которой достигается равновесие между покидающими ее жидкостью и паром. Методы определения числа теоретических тарелок подробно описаны в работе [1]. В реальных условиях между данными потоками равновесие не достигается. Поэтому для проведения процесса ректификации потребуется большее число ступеней контакта, чем теоретическое. Мерой совершенства контактного устройства (тарелки, насадки) является степень отличия реального состава пара и жидкости после их взаимодействия в контактном устройстве от предельно возможного (теоретически достижимого) равновесного состояния. Эта степень отличия характеризуется коэффициентом полезного действия контактного устройства и в значительной степени определяет совершенство самой ректификационной колонны. Основными рабочими параметрами процесса ректификации являются давление, флегмовое число, число теоретических тарелок, уровень подачи питания. Под флегмовым числом понимается отношение количества возвращаемой в аппарат флегмы (части верхнего продукта) к количеству отбираемого дистиллята. От величины этого параметра зависит как качество получаемого продукта, так и энергетические затраты на его достижение. Чем больше флегмовое число, т.е. чем больше возвращается в аппарат флегмы на единицу отбираемого дистиллята, тем чище будет получаться товарный продукт, но энергетические затраты при этом будут также возрастать.
Лабораторный практикум 2.1 Использование лабораторной установки периодической ректификации для анализа трехкомпонентной смеси с целью определения структуры диаграммы парожидкостного равновесия Цель лабораторной работы: исследование диаграммы парожидкостного равновесия тройной смеси с использованием лабораторной установки периодической ректификации Основные задачи: · знакомство с устройством ректификационной установки периодического действия и принципами ее работы; · приготовление смеси заданного состава и ее ректификация; · получение кривой разгонки и анализ структуры диаграммы парожидкостного равновесия.
Подготовка к эксперименту Подготовка к эксперименту включает ряд этапов: · сбор информации о физико-химических свойствах заданной трехкомпонентной системы (чистых компонентах и азеотропах); · определение структуры диаграммы парожидкостного равновесия трехкомпонентной системы и для заданного исходного состава оценка порядка отбора проб; · приготовление смеси заданного состава; · выполнение эксперимента.
Проведение эксперимента Приготовленная смесь с помощью воронки заливается в куб колонны. Открывается подача холодной воды в холодильники и включается обогрев куба. По мере нагрева жидкости в кубе и изменении температурного профиля колонны включается компенсационный обогрев царг. После стабилизации температурного профиля включается отбор дистиллята. С помощью автоматического переключателя приемников производится отбор дистиллята за определенный равный промежуток времени. По мере отбора датчик уровня фиксирует необходимые данные и выводит на монитор компьютера информацию о температуре, наблюдаемой при отборе каждой пробы, и объеме жидкости, оставшейся в кубе. По полученным данным необходимо построить зависимости изменения температуры от количества отбираемых проб – кривые разгонки.
Пример выполнения лабораторной работы Исследуемая система этиловый спирт – вода – изобутиловый спирт. Ниже в таблицах 1-2 приведены свойства чистых веществ и азеотропов: Таблица 1. Свойства чистых веществ системы этанол – вода – изобутанол.
Таблица 2. Азеотропные данные системы этанол – вода – изобутанол
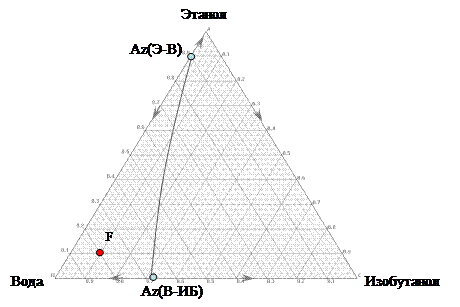
Согласно имеющимся справочным данным исследуемая система содержит два бинарных азеотропа: этанол – вода и вода – изобутиловый спирт. Диаграмма фазового равновесия представлена на рисунке 6. Система относится к классу 3.2.0-2б и характеризуется наличием двух областей дистилляции и ректификации.
Рисунок 6. Диаграмма фазового равновесия трехкомпонентной системы этанол – вода - изобутанол В качестве исходного выбран следующий состав: этанол – 10, вода – 80, изобутанол – 10 % мольн. Необходимо рассчитать данные для приготовления исходного раствора объемом 500 мл и представить их в таблице 3. Таблица 3. Данные для приготовления раствора.
Точка исходного состава принадлежит области ректификации, прилегающей к воде, следовательно, при загрузке данной смеси в колонну периодического действия первой будет отгоняться фракция, соответствующая азеотропу этанол – вода при температуре 78,0 град С, второй фракцией будет азеотроп вода – изобутанол (температура 89,82 град С), а третьей – вода (температура 100 град С). Пробы объемом 15 мл отбирались через равный промежуток времени. Общее количество отобранных проб составило 26. Давление в колонне – атмосферное. В результате эксперимента получена кривая разгонки исследуемой смеси заданного состава, которая представлена на рисунке 7. Как и ожидалось, в результате разгонки первой отгоняется фракция, соответствующая азеотропу этанол – вода при температуре 78,9 град С, второй – азеотропу вода – изобутанол (температура 91,2 град С) и третьей – воде (101 град С).
Рисунок 7. Кривая разгонки смеси этанол – вода – изобутанол состава (0,1; 0,8; 0,1)
Подготовка к эксперименту Подготовка к эксперименту включает ряд этапов: · сбор информации о физико-химических свойствах заданной трехкомпонентной системы (чистых компонентах и азеотропах); · определение структуры диаграммы парожидкостного равновесия трехкомпонентной смеси и для заданного исходного состава построение линии материального баланса колонны; · приготовление смесей, отвечающих составу исходной смеси и составу куба, полученному в результате расчета материального баланса ректификационной колонны; · выполнение эксперимента.
Проведение эксперимента Открывается подача холодной воды в холодильники. Приготовленная смесь, состав которой отвечает кубовому продукту, заливается через верх колонны до полного заполнения куба, после чего включается его обогрев. По мере того, как пары будут подниматься по ректификационной колонне, включается компенсационный обогрев на царгах. Как только пары достигнут уровня ввода исходной смеси необходимо включить насос для подачи исходной смеси в ректификационную колонну. Скорость подачи питания регулируется с помощью насоса. Колонна работает в режиме полного орошения до наступления стационарного режима (установления постоянства температуры). Далее колонну переводят на работу при конечном флегмовом числе. Анализ продуктовых потоков проводится с использованием хроматографа.
Пример выполнения лабораторной работы Разделению подвергается система этанол – вода – изобутиловый спирт. Свойства чистых веществ, а также азеотропные характеристики приведены в разделе 2.1.4. В качестве исходного выбран состав: этанол – 50, вода – 30, изобутанол – 20 % мол. Необходимо рассчитать данные для приготовления исходного раствора объемом 500 мл и представить их в таблице 4. Таблица 4. Данные для приготовления раствора.
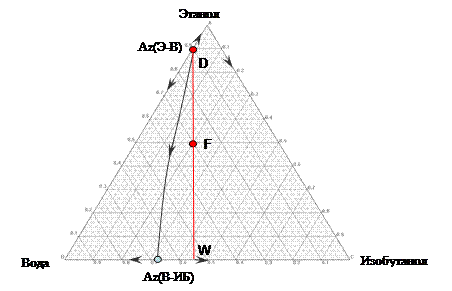
Основной задачей является получение в дистилляте азеотропа этанол-вода (I заданное разделение). Линия материального баланса процесса ректификаци в колонне проходит через точку исходного состава и азеотроп этанол-вода (рисунок 9).
Рисунок 9. Диаграмма фазового равновесия тройной системы этанол – вода – изобутанол и линия материального баланса процесса Зная состав исходной смеси и дистиллята, из материального баланса колонны можно определить состав кубового продукта, который согласно расчетам будет составлять: этанол – 0; вода – 55,5; изобутанол – 45,5 % мол. Следует отметить, что на практике получить данные составы дистиллятного и кубового продукта невозможно, поскольку разделение проводится на ректификационной колонне конечной эффективности и при конечном флегмовом числе. Для разделения смеси была использована ректификационная колонна непрерывного действия, описанная в пункте 2.2.1. Подача смеси осуществлялась в середину колонны, т.е. на 15 теоретическую тарелку. В результате опыта с постоянным набором регулирующих параметров (флегмовое число 8, поток питания – 82 г/час, поток дистиллята – 21 г/час) были получены следующие составы дистиллята и куба: дистиллят – (89,0; 11,0; 0,0 мол. %), куб – (8,3; 51,2; 40,5 % мол.). Регулирующие параметры получены путем предварительного вычислительного эксперимента. Таким образом, в результате эксперимента показана возможность выделения в дистилляте состава, близкого к составу азеотропа этанол – вода.
Подготовка к эксперименту Подготовка к эксперименту включает ряд этапов: · сбор информации о физико-химических свойствах заданной трехкомпонентной системы (чистых компонентах и азеотропах); · определение структуры диаграммы парожидкостного равновесия трехкомпонентной смеси и для заданного исходного состава построение линии материального баланса колонны; · приготовление исходной смеси; · выполнение эксперимента.
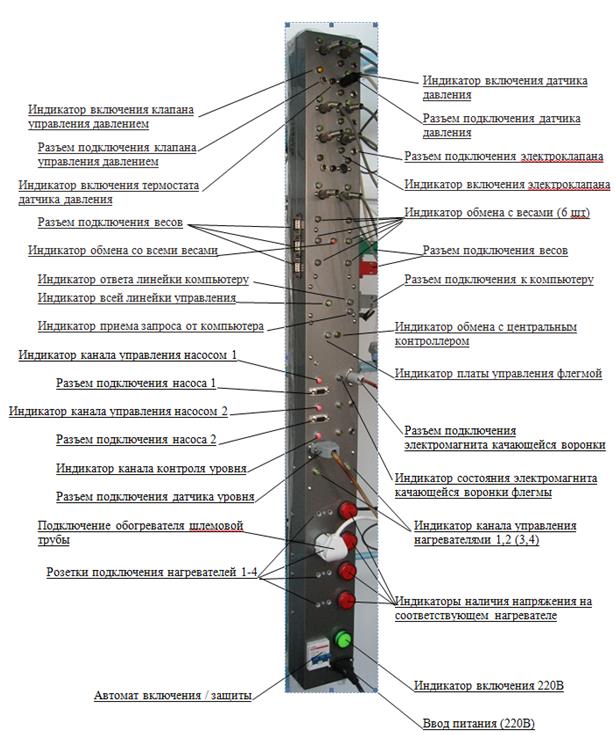
Рисунок 10. Устройство коммутационной линейки и ее составных частей
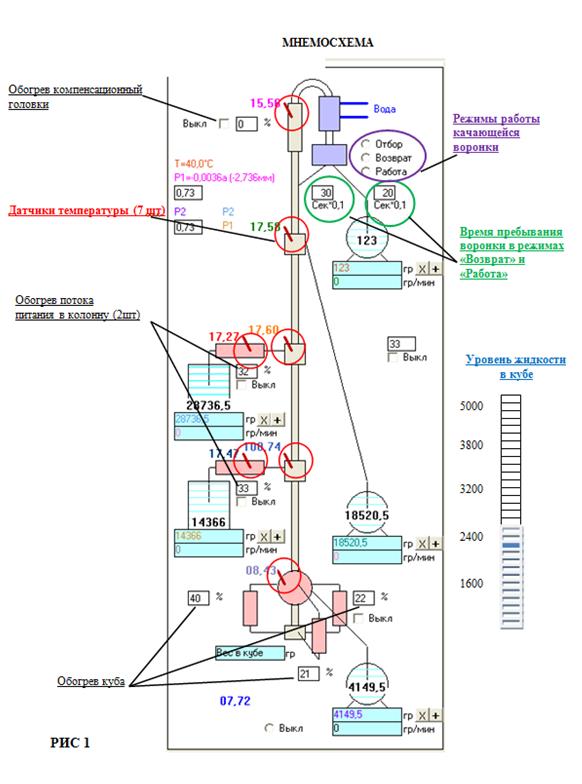
Рисунок 11. Мнемосхема ректификационной колонны
Пуск Включаем компьютер, входим в систему как «гость». Запускаем программу «Колонна». В открывшемся окне программы управления колонны отображается мнемоническая схема колонны (рисунок 11). Включаем водяное охлаждение шаровым краном, затем электропитание колонны и коммутационную линейку. Убеждаемся в наличии связи и обмена данными с компьютером. При этом в верхней части окна вывода графической информации надпись «ОБМЕНА НЕТ» должна смениться надписью «ИДЕТ ОБМЕН». Все краны на колонне по ее высоте должны быть перекрыты. Заполняем куб до уровня верхнего слива куба (через горловину куба или насосом питания) примерно на 3 – 4.5 литра. Закрываем горловину куба заглушкой. Проверяем уровень заливки куба по индикатору уровня на мнемосхеме колонны, расположенном в правом нижнем углу экрана монитора (рисунок 11). Устанавливаем приемники кубовой жидкости и дистиллята. Соединяем приемники с колонной. Включаем весы подачи питания и отбора продуктов. Проверяем показания весов визуально и на мнемосхеме колонны. Сверяем наличие обмена между линейкой и весами. Красный центральный индикатор сигнализирует не о неисправности, а об отсутствии связи с частью весов, общее количество которых может достигать 6 шт. На мнемосхеме устанавливаем качающуюся воронку в положение «ВОЗВРАТ». Включаем обогрев куба на мощность 10 – 30 %, не более. Контроль температуры куба осуществляется по показаниям на мнемосхеме. После закипания жидкости при необходимости снизить нагрузку на куб (контролируя уровень жидкости в кубе на мнемосхеме) После установления постоянства профиля температуры по высоте аппарата, переключаем регулятор флегмы в режим «РАБОТА». Проводим отбор дистиллята. Определив предварительно значение R (флегмового числа), задаем соотношение между отбираемым и возвращаемым в колонну количеством жидкости. Соотношение определяется количеством секунд работы в режимах «ВОЗВРАТ» и «РАБОТА» (пример 100 сек / 100 сек). Состав дистиллята определяем при помощи хроматографа. Контроль текущих параметров процесса В процессе работы колонны необходимо следить за поддержанием обогрева куба (сохранение заданной мощности), подачей холодной воды для охлаждения паров дистиллята, уровнем жидкости в кубе (критический уровень жидкости в кубе – 2л), а также изменением температуры по высоте колонны. Остановка колонны Выключаем обогрев куба (электропитание колонны).Переключаем регулятор флегмы в режим «ВОЗВРАТ». После охлаждения стенок куба до комнатной температуры остатки кубовой жидкости сливаем в приемник кубовой жидкости. Перекрываем кран подачи холодной воды на конденсатор паров. Закрываем трубку дистиллята заглушкой. Выключаем питание «линейки управления». Выключаем программу «Колонна» и компьютер. Отключаем электропитание компьютера. Пример выполнения лабораторной работы Исследуемая система этиловый спирт – вода. Свойства чистых веществ и азеотропов приведены выше в таблицах 1 и 2. Согласно имеющимся справочным данным исследуемая система содержит положительный азеотроп. Следовательно, при разделении предполагается в дистилляте получить состав, близкий к составу азеотропа. Готовится исходная смесь объемом 4 литра (2 литра этанола и 2 литра воды). Состав полученной смеси определяем с помощью хроматографа: этанол – 22,6 % мол., воды – 77,4 % мол. Подача смеси осуществлялась в середину колонны. Отбор дистиллята проводится при температуре 78 град С. В результате проведенного опыта в дистилляте получена смесь следующего состава: этанол – 88,9 % мол., воды – 11,1 % мол.
Список рекомендуемой литературы
1. Перегонка. Под редакцией А. Вайсбергера. Изд-во Иностранной литературы. Москва. 1954 г. 572с. 2. Процессы и аппараты химической технологии. Общий курс: [Электронный ресурс]: в 2 кн. / В. Г. Айнштейн, М. К. Захаров, Г. А. Носов [и др.]; Под ред. В. Г. Айнштейна. — 5-е изд. (эл.). — М.: БИНОМ. Лаборатория знаний, 2014. 3. Захаров М.К. Учебно-методическое пособие: Ректификационная установка непрерывного действия. Методические указания по выполнению курсового проекта. Учебно-методическое пособие. Изд. ИПЦ МИТХТ им. М.В. Ломоносова. 2010. 66с. 4. База данных национального института стандартов и технологий (NIST). 5. Коган В.Б., Фридман В.М., Кафаров В.В. Равновесие между жидкостью и паром, М., Наука, 1966, кн. 1,2. 6. Огородников С.К., Лестева Т.М. и др. Азеотропные смеси. Изд-во «Химия», Л., 1971, 848 стр. 7. Компьютерная система научных исследований и предпроектной разработки технологических систем ректификации. Мозжухин А.С., Ямпуров В.Л. Наука и технология углеводородов. 2000. №4. С.126
Введение
Одним из основных процессов разделения жидких многокомпонентных смесей в промышленности основного органического и нефтехимического синтеза является ректификация. Данный процесс отвечает специфике указанных отраслей, прежде всего крупнотоннажности производств и требованию достаточно высокой степени чистоты получаемых продуктов. Последнее является показателем эффективности работы ректификационных установок, который зависит как от конструктивных особенностей колонны и физико-химических свойств разделяемой смеси, так и от выбора оптимального технологического режима. На стадии исследования физико-химических свойств разделяемой смеси и оценки возможности ее разделения ключевая роль отводится лабораторным методам исследования – периодической и непрерывной ректификации. Непрерывная ректификация позволяет определить статические параметры работы колонны при разделении жидкой многокомпонентной смеси известного состава. Основное значение периодической ректификации заключается в определении структуры диаграммы парожидкостного равновесия с целью качественной и количественной идентификации компонентов смеси.
Ректификация. Ректификация — процесс переноса компонента (компонентов) между жидкой и насыщенной конденсирующейся паровой фазами при противотоке этих фаз. Организация потоков пара и жидкости, а также их взаимодействие реализуются в специальных массообменных аппаратах — ректификационных колоннах. Поток пара создается за счет подвода теплоты (энергии) в выносной кипятильник ректификационной установки и испарения в нем части нижнего продукта. Поток жидкости (флегмы или орошения) организуется за счет возврата в колонну конденсата уходящего с верха колонны пара. Процесс тепломассообмена заключается в непрерывном обмене компонентами между жидкой и паровой фазами. Стекающая вниз жидкая фаза обогащается тяжелокипящим компонентом, а поднимающийся пар – легкокипящим. Взаимодействие потоков осуществляется на специальных контактных устройствах, размещенных по высоте ректификационной колонны. Можно выделить три основных типа массообменных устройств: тарельчатые, насадочные и пленочные. При расчете процесса ректификации оперируют понятием «теоретической тарелки», т.е. тарелки, на которой достигается равновесие между покидающими ее жидкостью и паром. Методы определения числа теоретических тарелок подробно описаны в работе [1]. В реальных условиях между данными потоками равновесие не достигается. Поэтому для проведения процесса ректификации потребуется большее число ступеней контакта, чем теоретическое. Мерой совершенства контактного устройства (тарелки, насадки) является степень отличия реального состава пара и жидкости после их взаимодействия в контактном устройстве от предельно возможного (теоретически достижимого) равновесного состояния. Эта степень отличия характеризуется коэффициентом полезного действия контактного устройства и в значительной степени определяет совершенство самой ректификационной колонны. Основными рабочими параметрами процесса ректификации являются давление, флегмовое число, число теоретических тарелок, уровень подачи питания. Под флегмовым числом понимается отношение количества возвращаемой в аппарат флегмы (части верхнего продукта) к количеству отбираемого дистиллята. От величины этого параметра зависит как качество получаемого продукта, так и энергетические затраты на его достижение. Чем больше флегмовое число, т.е. чем больше возвращается в аппарат флегмы на единицу отбираемого дистиллята, тем чище будет получаться товарный продукт, но энергетические затраты при этом будут также возрастать.
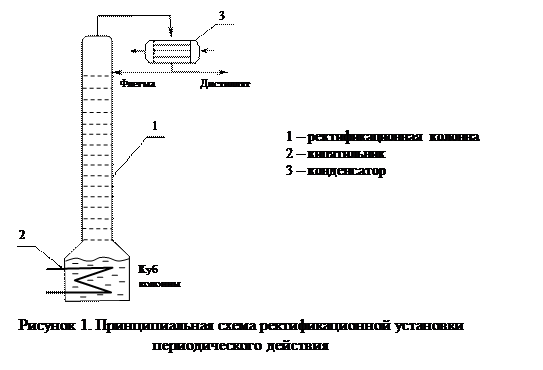
Режимы проведения ректификационных процессов в лаборатории. В зависимости от поставленных задач используют различные режимы проведения процессов: периодическая, полунепрерывная и непрерывная ректификация. Периодическая и полунепрерывная ректификация. Ректификация в периодическом режиме заключается в разгонке определенного количества смеси, имеющейся в кубе. Причем смесь однократно вводится в куб аппарата, что и обуславливает название процесса. Основное отличие периодического процесса от непрерывного состоит в том, что при периодическом процессе непрерывно меняется состав куба. Принципиальная схема ректификационной колонны периодического действия представлена на рисунке 1. Различают простую перегонку и фракционированную. При простой перегонке все количество дистиллята собирают в одном приемнике. После окончания процесса исходная смесь оказывается разделенная на две части: дистиллят и кубовый остаток. При фракционированной разгонке дистиллят состоит из отдельных фракций.
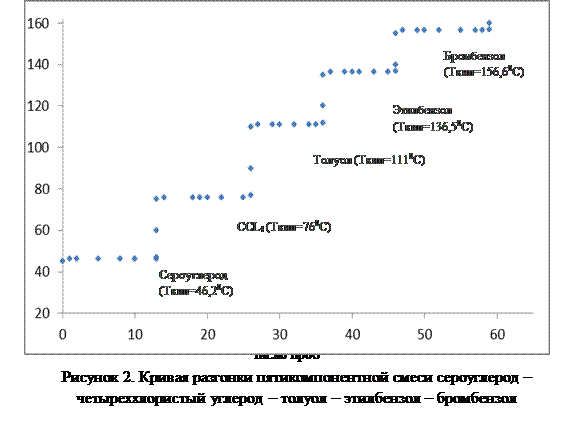
Периодическая ректификация в лаборатории преследует обычно две цели: 1) количественное определение состава перегоняемой жидкости; 2) выделение одного или большего числа компонентов из смеси, которые подвергаются дальнейшему исследованию. Периодическая ректификация позволяет разделить смесь на фракции определенного состава. Метод ректификационного анализа основан на том, что при отгонке дистиллята постоянного состава (чистого вещества или смеси), состав кубовой жидкости в концентрационном треугольнике изменяется по прямой линии, которая проходит через точки составов исходной смеси и дистиллята. Подвергая ректификации ряд смесей, точки состава которых лежат в различных областях концентрационного треугольника, и анализируя получающиеся кривые разгонки, выражающие зависимость между количествами и температурой кипения дистиллята, можно получить представление об условиях разделения смеси ректификацией. Если колонна имеет достаточную эффективность и работает так, что отделяет каждый из компонентов в достаточно чистом виде от всех остальных компонентов, находящихся в исходной смеси, то полученная кривая разгонки будет состоять из ряда горизонтальных линий или «ступенек», соединенных между собой. Пример кривой разгонки пятикомпонентной зеотропной системы сероуглерод – четыреххлористый углерод – толуол – этилбензол – бромбензол представлен на рисунке 2. Каждая ступенька отвечает чистому компоненту с его температурой кипения. Количество вещества, полученное в результате разделения, также может быть определено из кривой разгонки.
Часто в лабораторных установках используют полунепрерывный режим работы, который позволяет более эффективно использовать тепло и повысить производительность. От периодического он отличается тем, что в куб по мере отбора дистиллята добавляется смесь, подлежащая разделению. Питание исходной смесью может быть произведено непосредственно в куб или выше него, а исходная смесь должна быть предварительно нагрета до температуры, близкой к температуре кипения. Этот метод применяют главным образом тогда, когда нужно отделить легкокипящую фракцию или сконцентрировать смесь, содержащую растворенные твердые вещества. Непрерывная ректификация. При непрерывном режиме работы подачу исходной смеси осуществляют постоянно в точку питания. Уровень питания делит колонну на укрепляющую и исчерпывающую части. После пуска аппарата все условия проведения процесса ректификации остаются постоянными. Основное преимущество непрерывной ректификации состоит в том, что разделяемая смесь находится в сравнительно мягких температурных условиях. Таким образом, работая в непрерывном режиме, часто удается на лабораторных установках достигнуть производительности полупромышленных аппаратов периодического действия. Другое преимущество состоит в том, что при устойчивой работе колонны получают дистиллят и кубовую жидкость постоянного состава. Кроме того, расход тепла оказывается значительно ниже, чем при периодическом режиме. Основные области применения непрерывной ректификации в лаборатории можно классифицировать следующим образом: 1. Опытная ректификация с использованием промышленных методов: · исследования процессов, которые должны быть осуществлены в полупромышленном или промышленном масштабе; · сравнительная ректификация. 2. Предварительное фракционирование больших количеств веществ: · отделение низкокипящей фракции; · выделение средней фракции; · отделение высококипящего остатка. 3. Ректификация с целью получения продуктов: · разделение термически нестойких смесей; · выделение чистых компонентов из смеси; · очистка сырья и растворителей.
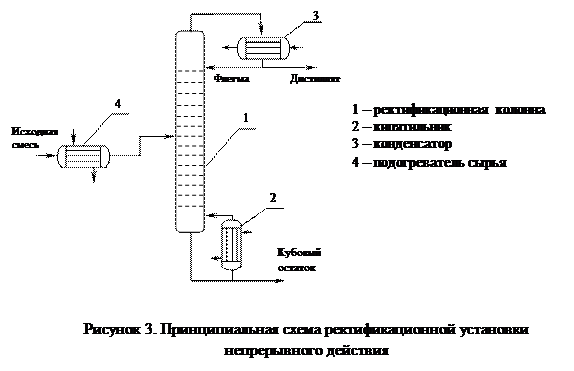
Принципиальная схема ректификационной установки непрерывного действия представлена на рисунке 3.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-12-09; просмотров: 1012; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.20 (0.056 с.) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||