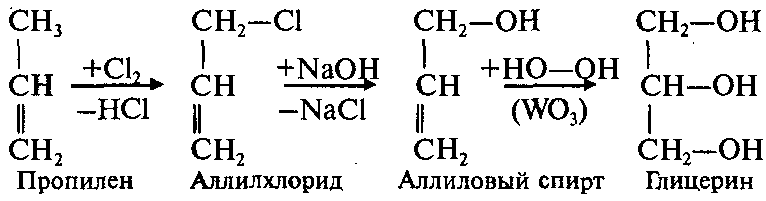Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Спирты. Гомологический ряд, изомерия, номенклатура.
Спирты – это производные углеводородов, у которых один или более атомов водорода замещены на гидроксигруппу (-ОН). Общая формула - СnH2n+1OH – предельные одноатомные Гомолог ряд: СН3 – ОН метанол, метиловый спирт СН3 –СН2 – ОН этанол, этиловый спирт СН3 –СН2 – СН2 – ОН пропанол-1, пропиловый спирт СН3 –СНOH – СН3 пропанол-2, изопропиловый спирт Общая формула - СnH2n (OH)2- предельные двуатомные Гомолог ряд: Этандиол-1,2, пропандиол-1,2, пропандиол-1,3 Общая формула: СnH2n-1 (OH)3 – предельные трехатомные Изомерия: углеродного скелета Положения OH-группы(пропанол-1, пропанол-2) Межклассовая с простыми эфирам Номенклатура: Для наименования спиртов используется систематическая номенклатура (ИЮПАК), а также для низших спиртов простого строения широко употребима радикальноспиртовая (рациональная) номенклатура (этиловый спирт). Линейные молекулы по систематической номенклатуре именуют следующим образом: к названию соответствующего алкана добавляют окончание –ол. Начиная с пропанола, в конце названия цифрой через дефис указывают положение гидроксигруппы. У разветвлённых молекул находят главную цепь. В ней должен быть атом углерода, связанный с гидроксигруппой. Цепь нумеруют с того конца, к которому ближе гидроксигруппа. Называют радикалы в общепринятом порядке, в конце – спирт по главной цепи с указанием положения ОН-группы (цифрой через дефис) В названии двухатомных спиртов используются общеизвестные правила: к соответствующему алкану добавляется окончание –диол. Затем цифрами через дефис указывают положения гидроксигрупп. Спирты. Способы получения. Предельные одноатомные 1) Гидратация алкенов: CH2=CH2+ H-OH->CH3-CH2OH(этанол) 2) Щелочной гидролиз моногалогеналкиловв
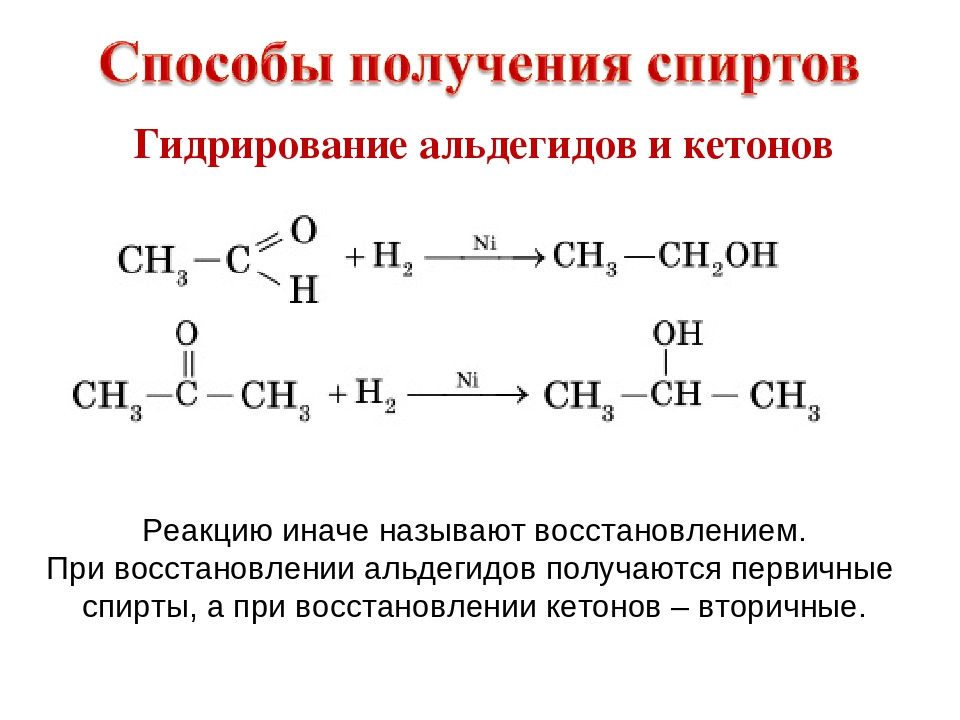
3) Гидрирование альдегидов и кетонов. Из альдегидов – первичные спирты, из кетонов – вторичные
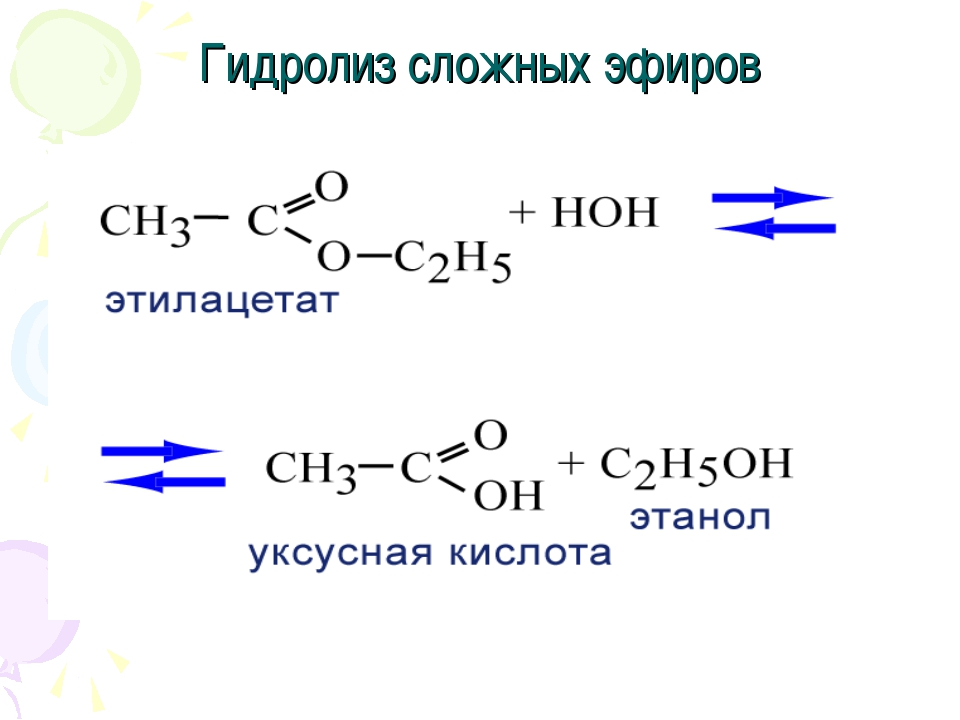
4) Гидролиз сложных эфиров
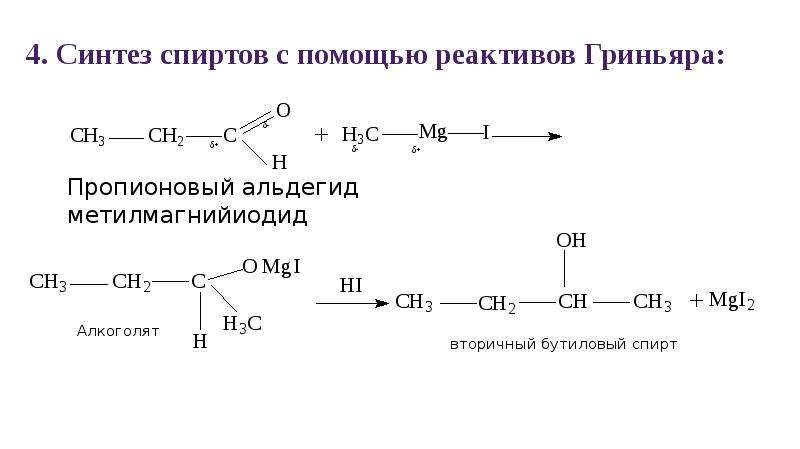
5) Синтез Гриньяра
Из альдегидов – первичные, кетонов – третичные 6) Брожение сахаров C6H12O6->ферменты 2C2H5OH + 2CO2 Предельные двухатомные Получение
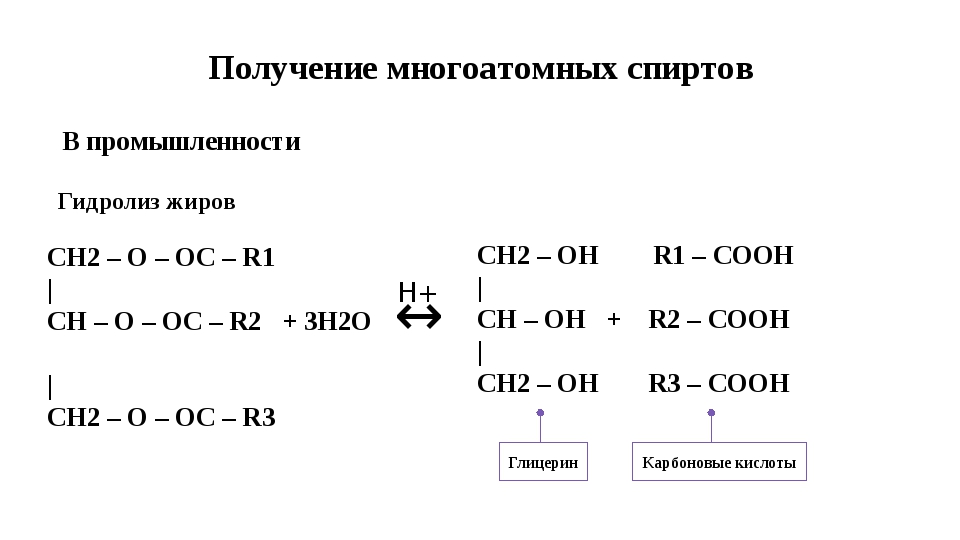
2) Г идратация алкенов(реакция Вагнера) СH2=Ch2+KMnO4+H20-> CH2OH-CH2OH(этандиол-1,2) + 2NaBr Предельные трехатомные
Из пропилена(лучше посмотрите в лекции, не нашла норм картинки) Спирты. Химические свойства.
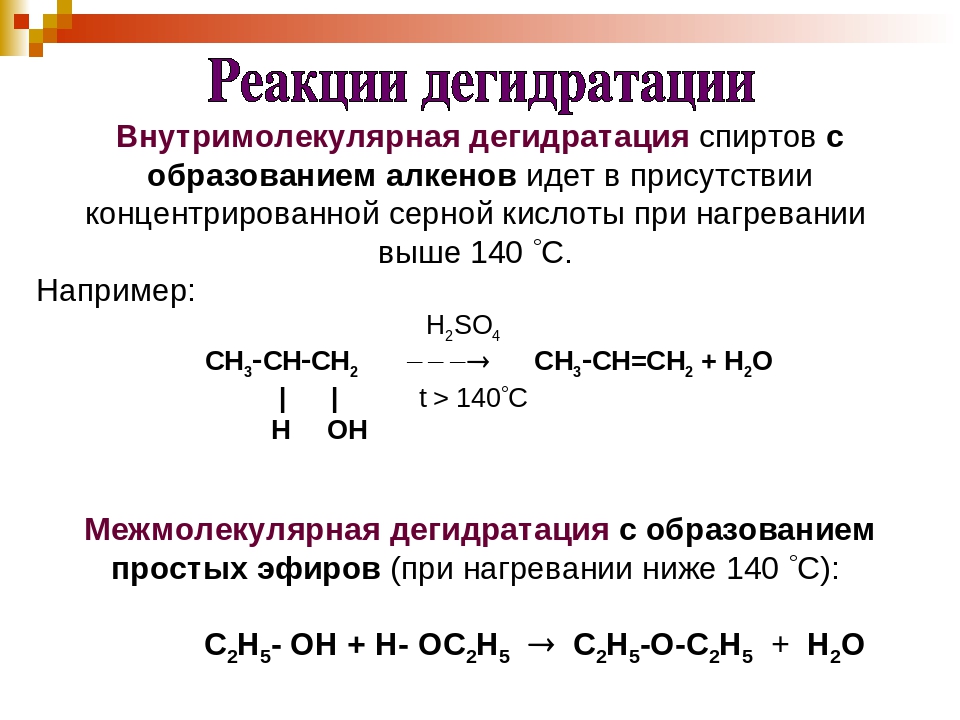
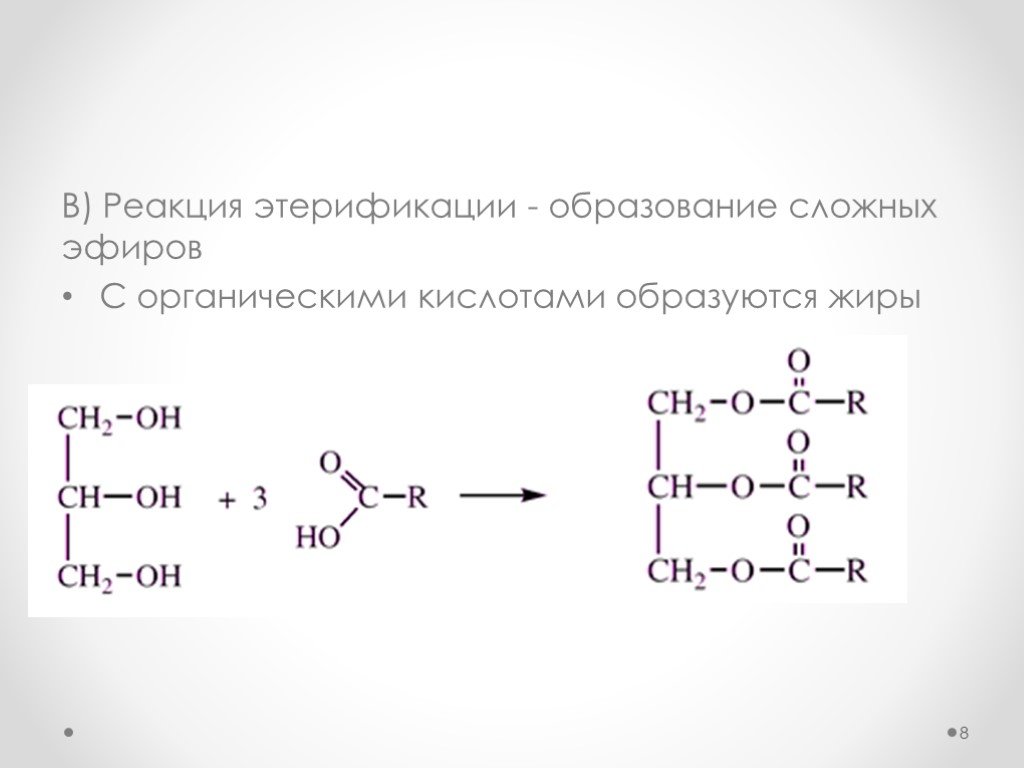
Одноатомные Р-ции на гидроксильный водород: Взаимод с щелочными МЕ: 2 CH3-OH+ 2Na -> 2CH3-ONa (метилат натрия) + H2 Образование сложных эфиров: CH3COOH+ CH3OH-> CH3-CO=O-CH3 (метил-ацетат) + H2O Образование простых эфиров(межмолекулярная дегидратация): CH3-OH + HO-CH3 -> CH3 – O-CH3 (диметиловый эфир) + H2O Один спирт отдает только гидроксильный водород, другой он группу Реакции на гидроксил Замещение на атом галогена: CH3-OH + PCl5 -> CH3-Cl + POCL3 + HCl Внутримолекулярная дегидратация
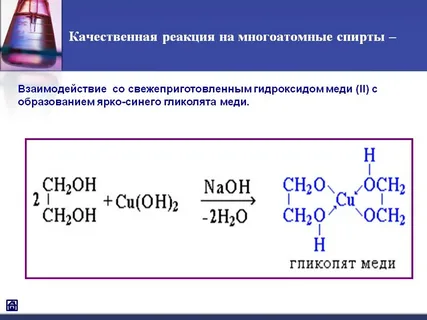
Межмолекулярная дегидратация: CH3-OH + HO-CH3 -> CH3 – O-CH3 (диметиловый эфир) + H2O Реакции окисления Первичные – до альдегидов, вторичные – до кетонов, третичные – с трудом Двухатомные Взаимод с Cu(OH)2
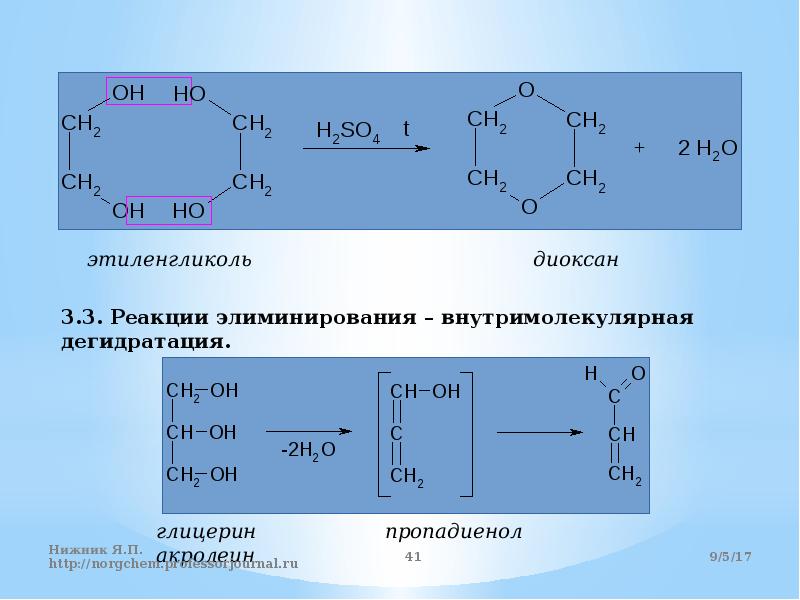
Реация дегидратации: внутримолек(2) и межмолек(1)
Т рехатомные ОБРАЗОВАНИЕ ГЛИЦЕРАТОВ
|
|||||
|
Последнее изменение этой страницы: 2020-12-09; просмотров: 762; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.223.123 (0.005 с.) |