Кейс
 Впервые этот газ был замечен Парацельсом в первой половине XVI века, но только Лемери в конце XVII века выделил его из обыкновенного воздуха, показав его горючесть. В дальнейшем это вещество было изучено Кавендишом. Лавуазье назвал этот газ - «рождающий воду».
Впервые этот газ был замечен Парацельсом в первой половине XVI века, но только Лемери в конце XVII века выделил его из обыкновенного воздуха, показав его горючесть. В дальнейшем это вещество было изучено Кавендишом. Лавуазье назвал этот газ - «рождающий воду».
Самый легкий газ. Активно использовался в дирижаблестроении, пока не сгорел немецкий дирижабль Гинденбург.
Вопросы:
1. Назовите самый легкий газ.
2. Какие свойства этого газа обусловили его применение.
 Водород – самый легкий газ, легче просто быть не может. Он в 14,5 раз легче воздуха. И когда придумали, как получать его в больших количествах, то именно это его свойство стали использовать в первую очередь. Водородом стали наполнять воздушные шары. В первых воздушных шарах подъемную силу создавал горячий воздух. Он легче холодного и поднимается вверх. И если нагреть воздух в шаре – то он будет поднимать и шар, и груз, который к шару прикреплен. Но это хорошо для развлечений. Подъемная сила такого шара невелика, и большие грузы он перевозить не сможет. К тому же воздух в шаре нужно все время подогревать. А вот если наполнить шар газом, который легче воздуха, то такой шар может оказаться куда полезней. Водород и стали использовать в качестве такого газа, причем не только в воздушных шарах. Воздушный шар может поднять груз, а дальше – как ветер дует. Для того чтобы летать туда, куда нужно, придумали дирижабль, воздушный шар с мотором, который крутил пропеллер. В начале XX века дирижабли были главным воздушным транспортом. Самолеты того времени летали недалеко и пассажиров взять не могли. А дирижабли регулярно летали из Германии в США, затрачивая на дорогу около двух дней. Крупнейший из пассажирских дирижаблей, «Отто фон Гинденбург» мог перевозить около 100 человек.
Водород – самый легкий газ, легче просто быть не может. Он в 14,5 раз легче воздуха. И когда придумали, как получать его в больших количествах, то именно это его свойство стали использовать в первую очередь. Водородом стали наполнять воздушные шары. В первых воздушных шарах подъемную силу создавал горячий воздух. Он легче холодного и поднимается вверх. И если нагреть воздух в шаре – то он будет поднимать и шар, и груз, который к шару прикреплен. Но это хорошо для развлечений. Подъемная сила такого шара невелика, и большие грузы он перевозить не сможет. К тому же воздух в шаре нужно все время подогревать. А вот если наполнить шар газом, который легче воздуха, то такой шар может оказаться куда полезней. Водород и стали использовать в качестве такого газа, причем не только в воздушных шарах. Воздушный шар может поднять груз, а дальше – как ветер дует. Для того чтобы летать туда, куда нужно, придумали дирижабль, воздушный шар с мотором, который крутил пропеллер. В начале XX века дирижабли были главным воздушным транспортом. Самолеты того времени летали недалеко и пассажиров взять не могли. А дирижабли регулярно летали из Германии в США, затрачивая на дорогу около двух дней. Крупнейший из пассажирских дирижаблей, «Отто фон Гинденбург» мог перевозить около 100 человек.
 Но водород не только легкий, он еще и очень легко загорается, а в смеси с воздухом – взрывается. При этом получается вода, именно поэтому водород называется порождающим воду (греческое название hydrogen переводится как «порождающий воду»). Горючесть водорода и погубила дирижабли. В последнем рейсе в 1937 году «Отто фон Гинденбург» взорвался и сгорел.
Но водород не только легкий, он еще и очень легко загорается, а в смеси с воздухом – взрывается. При этом получается вода, именно поэтому водород называется порождающим воду (греческое название hydrogen переводится как «порождающий воду»). Горючесть водорода и погубила дирижабли. В последнем рейсе в 1937 году «Отто фон Гинденбург» взорвался и сгорел.

 Это стало концом времени летательных аппаратов легче воздуха, им на смену приходили самолеты. Но не везде оказалось легко вытеснить водород. Метеорологам для исследования атмосферы часто нужно знать температуру, ветер и другие погодные условия на большой высоте, скажем в 20-30 км. Проще всего поднять туда нужные приборы на воздушном шаре, наполненном тем самым водородом. Только такой воздушный шар может взлететь достаточно высоко. Но в экспедицию баллон с газом не понесешь, он очень тяжелый, его с трудом несут два взрослых человека. Но водород несложно получить, для этого нужны твердая щелочь, алюминий и вода. Вода есть везде, а щелочь и алюминий гораздо легче баллона, несколько килограмм хватит надолго.
Это стало концом времени летательных аппаратов легче воздуха, им на смену приходили самолеты. Но не везде оказалось легко вытеснить водород. Метеорологам для исследования атмосферы часто нужно знать температуру, ветер и другие погодные условия на большой высоте, скажем в 20-30 км. Проще всего поднять туда нужные приборы на воздушном шаре, наполненном тем самым водородом. Только такой воздушный шар может взлететь достаточно высоко. Но в экспедицию баллон с газом не понесешь, он очень тяжелый, его с трудом несут два взрослых человека. Но водород несложно получить, для этого нужны твердая щелочь, алюминий и вода. Вода есть везде, а щелочь и алюминий гораздо легче баллона, несколько килограмм хватит надолго.
Но даже такое опасное свойство водорода как горючесть, удалось поставить на службу человеку. Водород горит и при этом выделяется много тепла. Прекрасно. Сделаем специальную горелку с очень горячим пламенем. Температура пламени в кухонной плите – около 600°С.  Это не так много, можно расплавить свинец или олово или согнуть стеклянную палочку. Но для приготовления еды более высокой температуры и не нужно. Температура пламени водородной горелки в четыре раза выше – около 2400°С. Такая температура нужна стеклодуву, чтобы сделать из стекла ажурную вазу сложной формы, ювелиру, чтобы расплавить серебро или золото и сделать украшение.
Это не так много, можно расплавить свинец или олово или согнуть стеклянную палочку. Но для приготовления еды более высокой температуры и не нужно. Температура пламени водородной горелки в четыре раза выше – около 2400°С. Такая температура нужна стеклодуву, чтобы сделать из стекла ажурную вазу сложной формы, ювелиру, чтобы расплавить серебро или золото и сделать украшение.
 А для дома – железо, из которого сделана кастрюля, расплавится при температуре почти на 1000° меньшей. Наверное, дома нам водородная горелка не пригодится. Но у водорода есть и еще одно полезное качество – когда он горит, то получается только вода. Конечно в виде пара, но атмосферу она загрязнять почти не будет. А это значит, что водород можно использовать как топливо для автомобилей, и они не будут ни чадить, не дымить. Только на пути создания таких автомобилей есть одна серьезная проблема: водород, в отличие от бензина, - газ. И чтобы его хранить, нужно закачать его под давлением в стальной баллон. А чтобы баллон выдержал, его стенки должны быть очень толстыми и баллон – тяжелым и большим. Для обычной машины это не очень удобный вариант и тогда ученые стали придумывать, как хранить водород более просто. Оказалось, что есть вещества, которые растворяют водород. Например, металл палладий поглощает водород в огромных количествах, 1 см3 палладия может растворить в 850 раз больший объем водорода. Но палладий дорогой и такой «топливный бак» может стоить существенно больше, чем остальной автомобиль. Впрочем, ученые такие люди, которым только поставь сложную задачу. Ведь решать такие задачи куда интересней, чем простые. В результате были созданы специальные пористые материалы, которые позволяли хранить водород без вышеупомянутых проблем. И тут ученые задумались – а зачем вообще сжигать водород в двигателе? Обычный бензиновый двигатель – штука сложная и не слишком эффективная. К тому же вы помните – при горении водорода температура очень высокая, и хотя сам водород при горении дает только воду, но при такой температуре начинает «гореть» воздух – кислород взаимодействует с азотом и в итоге получается азотная кислота, которая служит причиной кислотных дождей. С бензиновыми двигателями ситуация похожая, но там и без нее загрязнений достаточно. К тому же такие двигатели еще и шумят. Может быть лучше использовать в машинах по-настоящему чистые электродвигатели? Они не шумят, не загрязняют воздух, можно очень сильно упростить всю схему машины и сделать ее дешевле. Вот только как водород превратить в электричество? Оказывается это можно сделать. Есть такое интересное устройство – топливный элемент, в котором водород «горит» при комнатной температуре, превращаясь в воду и давая сразу электрический ток. По своему устройству он очень похож на обычную батарейку, только батарейка закрыта и в ней расходуется вещество, которое ее производитель положил туда на заводе, а в топливный элемент мы всегда можем добавить новую порцию нужного вещества. Фирма «Самсунг» разрабатывает такие топливные элементы в качестве батарей для телефонов и ноутбуков.
А для дома – железо, из которого сделана кастрюля, расплавится при температуре почти на 1000° меньшей. Наверное, дома нам водородная горелка не пригодится. Но у водорода есть и еще одно полезное качество – когда он горит, то получается только вода. Конечно в виде пара, но атмосферу она загрязнять почти не будет. А это значит, что водород можно использовать как топливо для автомобилей, и они не будут ни чадить, не дымить. Только на пути создания таких автомобилей есть одна серьезная проблема: водород, в отличие от бензина, - газ. И чтобы его хранить, нужно закачать его под давлением в стальной баллон. А чтобы баллон выдержал, его стенки должны быть очень толстыми и баллон – тяжелым и большим. Для обычной машины это не очень удобный вариант и тогда ученые стали придумывать, как хранить водород более просто. Оказалось, что есть вещества, которые растворяют водород. Например, металл палладий поглощает водород в огромных количествах, 1 см3 палладия может растворить в 850 раз больший объем водорода. Но палладий дорогой и такой «топливный бак» может стоить существенно больше, чем остальной автомобиль. Впрочем, ученые такие люди, которым только поставь сложную задачу. Ведь решать такие задачи куда интересней, чем простые. В результате были созданы специальные пористые материалы, которые позволяли хранить водород без вышеупомянутых проблем. И тут ученые задумались – а зачем вообще сжигать водород в двигателе? Обычный бензиновый двигатель – штука сложная и не слишком эффективная. К тому же вы помните – при горении водорода температура очень высокая, и хотя сам водород при горении дает только воду, но при такой температуре начинает «гореть» воздух – кислород взаимодействует с азотом и в итоге получается азотная кислота, которая служит причиной кислотных дождей. С бензиновыми двигателями ситуация похожая, но там и без нее загрязнений достаточно. К тому же такие двигатели еще и шумят. Может быть лучше использовать в машинах по-настоящему чистые электродвигатели? Они не шумят, не загрязняют воздух, можно очень сильно упростить всю схему машины и сделать ее дешевле. Вот только как водород превратить в электричество? Оказывается это можно сделать. Есть такое интересное устройство – топливный элемент, в котором водород «горит» при комнатной температуре, превращаясь в воду и давая сразу электрический ток. По своему устройству он очень похож на обычную батарейку, только батарейка закрыта и в ней расходуется вещество, которое ее производитель положил туда на заводе, а в топливный элемент мы всегда можем добавить новую порцию нужного вещества. Фирма «Самсунг» разрабатывает такие топливные элементы в качестве батарей для телефонов и ноутбуков.
 Представьте, что лет через пять, когда заряд вашего телефона будет заканчиваться, вам не нужно будет искать розетку, а потребуется только заправить телефон новой порцией спирта.
Представьте, что лет через пять, когда заряд вашего телефона будет заканчиваться, вам не нужно будет искать розетку, а потребуется только заправить телефон новой порцией спирта.
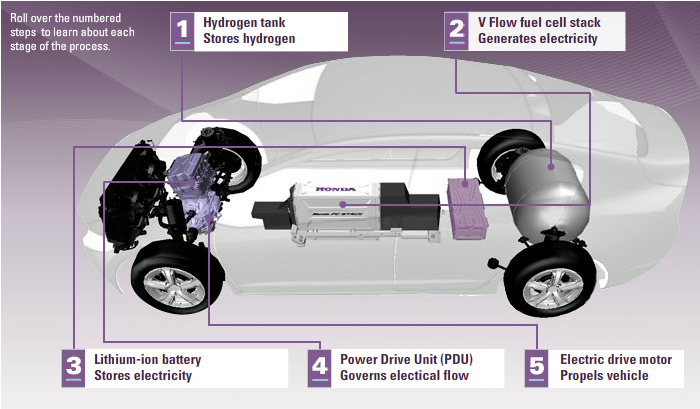
С водородом еще интересней. Электромобили на водородных топливных элементах уже выпускают, пусть и небольшими партиями.


 Впервые этот газ был замечен Парацельсом в первой половине XVI века, но только Лемери в конце XVII века выделил его из обыкновенного воздуха, показав его горючесть. В дальнейшем это вещество было изучено Кавендишом. Лавуазье назвал этот газ - «рождающий воду».
Впервые этот газ был замечен Парацельсом в первой половине XVI века, но только Лемери в конце XVII века выделил его из обыкновенного воздуха, показав его горючесть. В дальнейшем это вещество было изучено Кавендишом. Лавуазье назвал этот газ - «рождающий воду». Водород – самый легкий газ, легче просто быть не может. Он в 14,5 раз легче воздуха. И когда придумали, как получать его в больших количествах, то именно это его свойство стали использовать в первую очередь. Водородом стали наполнять воздушные шары. В первых воздушных шарах подъемную силу создавал горячий воздух. Он легче холодного и поднимается вверх. И если нагреть воздух в шаре – то он будет поднимать и шар, и груз, который к шару прикреплен. Но это хорошо для развлечений. Подъемная сила такого шара невелика, и большие грузы он перевозить не сможет. К тому же воздух в шаре нужно все время подогревать. А вот если наполнить шар газом, который легче воздуха, то такой шар может оказаться куда полезней. Водород и стали использовать в качестве такого газа, причем не только в воздушных шарах. Воздушный шар может поднять груз, а дальше – как ветер дует. Для того чтобы летать туда, куда нужно, придумали дирижабль, воздушный шар с мотором, который крутил пропеллер. В начале XX века дирижабли были главным воздушным транспортом. Самолеты того времени летали недалеко и пассажиров взять не могли. А дирижабли регулярно летали из Германии в США, затрачивая на дорогу около двух дней. Крупнейший из пассажирских дирижаблей, «Отто фон Гинденбург» мог перевозить около 100 человек.
Водород – самый легкий газ, легче просто быть не может. Он в 14,5 раз легче воздуха. И когда придумали, как получать его в больших количествах, то именно это его свойство стали использовать в первую очередь. Водородом стали наполнять воздушные шары. В первых воздушных шарах подъемную силу создавал горячий воздух. Он легче холодного и поднимается вверх. И если нагреть воздух в шаре – то он будет поднимать и шар, и груз, который к шару прикреплен. Но это хорошо для развлечений. Подъемная сила такого шара невелика, и большие грузы он перевозить не сможет. К тому же воздух в шаре нужно все время подогревать. А вот если наполнить шар газом, который легче воздуха, то такой шар может оказаться куда полезней. Водород и стали использовать в качестве такого газа, причем не только в воздушных шарах. Воздушный шар может поднять груз, а дальше – как ветер дует. Для того чтобы летать туда, куда нужно, придумали дирижабль, воздушный шар с мотором, который крутил пропеллер. В начале XX века дирижабли были главным воздушным транспортом. Самолеты того времени летали недалеко и пассажиров взять не могли. А дирижабли регулярно летали из Германии в США, затрачивая на дорогу около двух дней. Крупнейший из пассажирских дирижаблей, «Отто фон Гинденбург» мог перевозить около 100 человек. Но водород не только легкий, он еще и очень легко загорается, а в смеси с воздухом – взрывается. При этом получается вода, именно поэтому водород называется порождающим воду (греческое название hydrogen переводится как «порождающий воду»). Горючесть водорода и погубила дирижабли. В последнем рейсе в 1937 году «Отто фон Гинденбург» взорвался и сгорел.
Но водород не только легкий, он еще и очень легко загорается, а в смеси с воздухом – взрывается. При этом получается вода, именно поэтому водород называется порождающим воду (греческое название hydrogen переводится как «порождающий воду»). Горючесть водорода и погубила дирижабли. В последнем рейсе в 1937 году «Отто фон Гинденбург» взорвался и сгорел.
 Это стало концом времени летательных аппаратов легче воздуха, им на смену приходили самолеты. Но не везде оказалось легко вытеснить водород. Метеорологам для исследования атмосферы часто нужно знать температуру, ветер и другие погодные условия на большой высоте, скажем в 20-30 км. Проще всего поднять туда нужные приборы на воздушном шаре, наполненном тем самым водородом. Только такой воздушный шар может взлететь достаточно высоко. Но в экспедицию баллон с газом не понесешь, он очень тяжелый, его с трудом несут два взрослых человека. Но водород несложно получить, для этого нужны твердая щелочь, алюминий и вода. Вода есть везде, а щелочь и алюминий гораздо легче баллона, несколько килограмм хватит надолго.
Это стало концом времени летательных аппаратов легче воздуха, им на смену приходили самолеты. Но не везде оказалось легко вытеснить водород. Метеорологам для исследования атмосферы часто нужно знать температуру, ветер и другие погодные условия на большой высоте, скажем в 20-30 км. Проще всего поднять туда нужные приборы на воздушном шаре, наполненном тем самым водородом. Только такой воздушный шар может взлететь достаточно высоко. Но в экспедицию баллон с газом не понесешь, он очень тяжелый, его с трудом несут два взрослых человека. Но водород несложно получить, для этого нужны твердая щелочь, алюминий и вода. Вода есть везде, а щелочь и алюминий гораздо легче баллона, несколько килограмм хватит надолго. Это не так много, можно расплавить свинец или олово или согнуть стеклянную палочку. Но для приготовления еды более высокой температуры и не нужно. Температура пламени водородной горелки в четыре раза выше – около 2400°С. Такая температура нужна стеклодуву, чтобы сделать из стекла ажурную вазу сложной формы, ювелиру, чтобы расплавить серебро или золото и сделать украшение.
Это не так много, можно расплавить свинец или олово или согнуть стеклянную палочку. Но для приготовления еды более высокой температуры и не нужно. Температура пламени водородной горелки в четыре раза выше – около 2400°С. Такая температура нужна стеклодуву, чтобы сделать из стекла ажурную вазу сложной формы, ювелиру, чтобы расплавить серебро или золото и сделать украшение. А для дома – железо, из которого сделана кастрюля, расплавится при температуре почти на 1000° меньшей. Наверное, дома нам водородная горелка не пригодится. Но у водорода есть и еще одно полезное качество – когда он горит, то получается только вода. Конечно в виде пара, но атмосферу она загрязнять почти не будет. А это значит, что водород можно использовать как топливо для автомобилей, и они не будут ни чадить, не дымить. Только на пути создания таких автомобилей есть одна серьезная проблема: водород, в отличие от бензина, - газ. И чтобы его хранить, нужно закачать его под давлением в стальной баллон. А чтобы баллон выдержал, его стенки должны быть очень толстыми и баллон – тяжелым и большим. Для обычной машины это не очень удобный вариант и тогда ученые стали придумывать, как хранить водород более просто. Оказалось, что есть вещества, которые растворяют водород. Например, металл палладий поглощает водород в огромных количествах, 1 см3 палладия может растворить в 850 раз больший объем водорода. Но палладий дорогой и такой «топливный бак» может стоить существенно больше, чем остальной автомобиль. Впрочем, ученые такие люди, которым только поставь сложную задачу. Ведь решать такие задачи куда интересней, чем простые. В результате были созданы специальные пористые материалы, которые позволяли хранить водород без вышеупомянутых проблем. И тут ученые задумались – а зачем вообще сжигать водород в двигателе? Обычный бензиновый двигатель – штука сложная и не слишком эффективная. К тому же вы помните – при горении водорода температура очень высокая, и хотя сам водород при горении дает только воду, но при такой температуре начинает «гореть» воздух – кислород взаимодействует с азотом и в итоге получается азотная кислота, которая служит причиной кислотных дождей. С бензиновыми двигателями ситуация похожая, но там и без нее загрязнений достаточно. К тому же такие двигатели еще и шумят. Может быть лучше использовать в машинах по-настоящему чистые электродвигатели? Они не шумят, не загрязняют воздух, можно очень сильно упростить всю схему машины и сделать ее дешевле. Вот только как водород превратить в электричество? Оказывается это можно сделать. Есть такое интересное устройство – топливный элемент, в котором водород «горит» при комнатной температуре, превращаясь в воду и давая сразу электрический ток. По своему устройству он очень похож на обычную батарейку, только батарейка закрыта и в ней расходуется вещество, которое ее производитель положил туда на заводе, а в топливный элемент мы всегда можем добавить новую порцию нужного вещества. Фирма «Самсунг» разрабатывает такие топливные элементы в качестве батарей для телефонов и ноутбуков.
А для дома – железо, из которого сделана кастрюля, расплавится при температуре почти на 1000° меньшей. Наверное, дома нам водородная горелка не пригодится. Но у водорода есть и еще одно полезное качество – когда он горит, то получается только вода. Конечно в виде пара, но атмосферу она загрязнять почти не будет. А это значит, что водород можно использовать как топливо для автомобилей, и они не будут ни чадить, не дымить. Только на пути создания таких автомобилей есть одна серьезная проблема: водород, в отличие от бензина, - газ. И чтобы его хранить, нужно закачать его под давлением в стальной баллон. А чтобы баллон выдержал, его стенки должны быть очень толстыми и баллон – тяжелым и большим. Для обычной машины это не очень удобный вариант и тогда ученые стали придумывать, как хранить водород более просто. Оказалось, что есть вещества, которые растворяют водород. Например, металл палладий поглощает водород в огромных количествах, 1 см3 палладия может растворить в 850 раз больший объем водорода. Но палладий дорогой и такой «топливный бак» может стоить существенно больше, чем остальной автомобиль. Впрочем, ученые такие люди, которым только поставь сложную задачу. Ведь решать такие задачи куда интересней, чем простые. В результате были созданы специальные пористые материалы, которые позволяли хранить водород без вышеупомянутых проблем. И тут ученые задумались – а зачем вообще сжигать водород в двигателе? Обычный бензиновый двигатель – штука сложная и не слишком эффективная. К тому же вы помните – при горении водорода температура очень высокая, и хотя сам водород при горении дает только воду, но при такой температуре начинает «гореть» воздух – кислород взаимодействует с азотом и в итоге получается азотная кислота, которая служит причиной кислотных дождей. С бензиновыми двигателями ситуация похожая, но там и без нее загрязнений достаточно. К тому же такие двигатели еще и шумят. Может быть лучше использовать в машинах по-настоящему чистые электродвигатели? Они не шумят, не загрязняют воздух, можно очень сильно упростить всю схему машины и сделать ее дешевле. Вот только как водород превратить в электричество? Оказывается это можно сделать. Есть такое интересное устройство – топливный элемент, в котором водород «горит» при комнатной температуре, превращаясь в воду и давая сразу электрический ток. По своему устройству он очень похож на обычную батарейку, только батарейка закрыта и в ней расходуется вещество, которое ее производитель положил туда на заводе, а в топливный элемент мы всегда можем добавить новую порцию нужного вещества. Фирма «Самсунг» разрабатывает такие топливные элементы в качестве батарей для телефонов и ноутбуков. Представьте, что лет через пять, когда заряд вашего телефона будет заканчиваться, вам не нужно будет искать розетку, а потребуется только заправить телефон новой порцией спирта.
Представьте, что лет через пять, когда заряд вашего телефона будет заканчиваться, вам не нужно будет искать розетку, а потребуется только заправить телефон новой порцией спирта.



