
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Водородный показатель среды.Содержание книги
Поиск на нашем сайте
Занятие № 5 ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ СРЕДЫ. ГИДРОЛИЗ СОЛЕЙ Теоретическая часть
Электролиты — вещества, проводящие электрический ток. Процесс распада вещества на ионы под действием растворителя называется электролитической диссоциацией и является обратимым. Например, диссоциация оснований, кислот, солей:
NaOH ↔ Na+ + OH-
H2SO4 ↔ H+ + HSO4- (1 ступень) HSO4– ↔ H+ + SO42- (2 ступень)
Al2(SO4)3 ↔ 2Al3+ + 3SO42-. Сила электролита определяется степенью электролитической диссоциации a и выражается в процентах или в долях единицы. Вычислить ее можно по формулам: N a = ¾¾¾, N0 где N — число молекул, распавшихся на ионы; N0 — общее число молекул электролита в растворе; I – 1 или a = ¾¾¾, N – 1 где i — изотонический коэффициент; n — число ионов электролита в растворе. Более точным критерием для сравнения силы электролитов служит константа диссоциации. Константой диссоциации называется величина, показывающая отношение произведения концентрации ионов к концентрации недиссоциированных молекул слабого электролита в момент равновесия. Например,
[H+] • [ClO– ] Kдис = ¾¾¾¾¾¾ = 3,2•10–8. [HClO] Чем меньше значение константы диссоциации, тем слабее электролит. Для слабых электролитов константа и степень диссоциации находятся в следующей зависимости (закон разбавления Оствальда): К дис = С • a2; a = Ö К/C, где С — молярная концентрация электролита, моль/л Истинная степень диссоциации сильных электролитов в растворах любой концентрации равна 100 %. Многоосновные кислоты, диссоциация которых протекает ступенчато, характеризуется несколькими константами диссоциации. Например:
Исходя из значений приведенных констант диссоциации можно отметить, что К¢ > К¢¢, т. е. процесс распада электролита на ионы идет активнее по первой ступени.
Ионные реакции При взаимодействии растворов электролитов реакции происходят между ионами растворенных веществ. Химический процесс можно записать в молекулярной и ионно-молекулярной формах. Однако ионная форма отображает его точнее. При составлении ионных уравнений реакций вещества малодиссоциированные, малорастворимые (выпадающие в осадок) и газообразные изображаются в виде молекул:
1) H2SO4 + BaCl2 = BaSO4 ¯ + 2HCl 2H+ + SO42- + Ba2+ + 2Cl- = BaSO4 ¯ + 2H+ + 2Cl- – полное (развернутое) ионно-молекулярное уравнение; Ba2+ + SO42- = BaSO4 ¯ – сокращенное ионно-молекулярное уравнение. Сокращенное ионно-молекулярное уравнение указывает на то, что в реакции участвуют только ионы Ва2+ и сульфат - ионы SO42-.
2) Na2CO3 + 2HCl = 2NaCl + H2O + CO2 2Na+ + CO32- + 2H+ + 2Cl = 2Na+ + 2Cl- + H2O + CO2 СО32- + 2Н+ = Н2О + СО2 . Водородный показатель среды Вода является слабым электролитом и диссоциирует по уравнению
Константа диссоциации воды весьма мала: [H+] • [OH-] K = ¾¾¾¾¾ = 1,8 • 10-16. [H2O] Принимая концентрацию воды [Н2O] величиной практически постоянной и учитывая, что молярная концентрация воды в воде равна 1000/18 = 55,56 моль/л, получаем [H+] • [OH-] = 1,8 • 10-16 • 55,56 = 1 • 10-14 = К H2O. Произведение концентрации ионов водорода и ионов гидроксида называется ионным произведением воды. Так как при диссоциации одной молекулы воды получается один ион водорода и один ион гидроксида, то [H+] = [OH-] = 10-7 моль/л. Если к воде прибавить кислоту, то [H+] > 10-7 моль/л, а если прибавить щелочь, то [H+] < 10-7 моль/л. Таким образом, степень кислотности или щелочности раствора можно выразить с помощью концентрации ионов [H+] или [OH-]. Отрицательный десятичный логарифм концентрации водородных ионов принято называть водородным показателем рН рН = –lg [H+]. Тогда рН различных растворов будут иметь следующие значения : кислый pH < 7; нейтральный pH = 7; щелочной pH > 7. Гидролиз Гидролиз солей — это взаимодействие вещества с водой, при котором составные части вещества соединяются с составными частями воды. Различают несколько случаев гидролиза 1. Гидролиз соли, образованной сильным основанием и слабой одноосновной кислотой, идет с образованием сильного основания и слабой кислоты. (гидролиз по аниону)
Гидролиз соли, образованной сильным основанием и слабой многоосновной кислотой, протекает ступенчато:
  Na2CO3 + H2O NaHCO3 + NaOH Na2CO3 + H2O NaHCO3 + NaOH
2. Гидролиз соли слабого основания и сильной кислоты, идет с образованием основной соли и кислоты (гидролиз по катиону):
3. Гидролиз соли слабого основания и слабой одноосновной кислоты, идет с образованием слабого основания и слабой кислоты (гидролиз по катиону и аниону).
Уксусная кислота и гидроксид аммония — малодиссоциирующие вещества, однако незначительно они диссоциируют. В зависимости от степени диссоциации и определяют рН. В данном случае степени диссоциации для СН3СООН и NH4OH равны (a= 1,3 %). Следовательно, рН = 7.
Гидролиз соли, образованной слабым основанием и слабой одноосновной кислотой, идет ступенчато и продуктами являются основные соли и кислота:
Гидролиз соли, образованной слабым основанием и слабой летучей многоосновной кислотой, идет до конца (продукты гидролиза - слабое основание и слабая кислота).
4. Соли, образованные сильной кислотой и сильным основанием, гидролизу не подвергаются. Например,
ЛАБОРАТОРНАЯ РАБОТА № 4 Опыт 6. Полный гидролиз К 1-2 мл раствора Al2(SO4)3 прилейте такой же объем раствора соды Na2CO3. Наблюдайте выделение углекислого газа СО2 и образование осадка Al(OH)3. Напишите молекулярное и ионно-молекулярное уравнение происходящих реакций. КОНТРОЛЬНЫЕ ЗАДАНИЯ К ЛАБОРАТОРНОЙ РАБОТЕ № 5 Вариант 1 1. Определите рН 0,01 М раствора гидроксида бария. 2. Напишите молекулярные и ионно-молекулярные уравнения гидролиза раствора солей Pb(NO3)2. Вариант 2 1. Определите рН и рОН 0,1-молярного раствора едкого натра. 2. Как влияет на гидролиз сульфида натрия добавление щелочи? Вариант 3 1. Концентрация гидроксид-ионов в растворе равна 10-10 моль/л. Чему равен рН этого раствора? 2. Напишите молекулярные и ионно-молекулярные уравнения гидролиза раствора соли KCN. Вариант 4 1. Определите [H+] и [OH-] в растворе, рН которого равен 7,0. 2. Напишите молекулярные и ионно-молекулярные уравнения гидролиза соли: SrCl2. Вариант 5 1. Вычислите рН 0,2 н раствора NH4Cl. 2. Напишите молекулярные и ионно-молекулярные уравнения гидролиза соли KNO2. Вариант 6 1. Для реакции некоторой соли рН равно 4. Определите концентрацию ионов водорода и гидроксида в этом растворе. 2. Напишите молекулярные и ионно-молекулярные уравнения гидролиза соли NH4NO3. Как влияет на гидролиз добавление СН3СООН? Вариант 7 1. Вычислите рН 3,5 % (по массе) раствора HСl (r = 1,01 г/мл). 2. Напишите молекулярные и ионно-молекулярные уравнения гидролиза CrCl3. Укажите значение рН раствора этой соли. Вариант 8 1. Закончите уравнения следующих реакций с учетом возможности необратимого гидролиза взятых солей: Al2(SO4)3 + Na2S =...; FeCl3 + (NH4)2CO3 =.... 2. Вычислите значения рН растворов, в которых концентрация ОН- ионов (моль/л) равна 8 • 10-9, 3 • 10-6. Какова реакция среды этих растворов? Занятие № 5 ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ СРЕДЫ. ГИДРОЛИЗ СОЛЕЙ Теоретическая часть
Электролиты — вещества, проводящие электрический ток. Процесс распада вещества на ионы под действием растворителя называется электролитической диссоциацией и является обратимым. Например, диссоциация оснований, кислот, солей:
NaOH ↔ Na+ + OH-
H2SO4 ↔ H+ + HSO4- (1 ступень) HSO4– ↔ H+ + SO42- (2 ступень)
Al2(SO4)3 ↔ 2Al3+ + 3SO42-. Сила электролита определяется степенью электролитической диссоциации a и выражается в процентах или в долях единицы. Вычислить ее можно по формулам: N a = ¾¾¾, N0 где N — число молекул, распавшихся на ионы; N0 — общее число молекул электролита в растворе; I – 1 или a = ¾¾¾, N – 1 где i — изотонический коэффициент; n — число ионов электролита в растворе. Более точным критерием для сравнения силы электролитов служит константа диссоциации. Константой диссоциации называется величина, показывающая отношение произведения концентрации ионов к концентрации недиссоциированных молекул слабого электролита в момент равновесия. Например,
[H+] • [ClO– ] Kдис = ¾¾¾¾¾¾ = 3,2•10–8. [HClO] Чем меньше значение константы диссоциации, тем слабее электролит. Для слабых электролитов константа и степень диссоциации находятся в следующей зависимости (закон разбавления Оствальда): К дис = С • a2; a = Ö К/C, где С — молярная концентрация электролита, моль/л Истинная степень диссоциации сильных электролитов в растворах любой концентрации равна 100 %. Многоосновные кислоты, диссоциация которых протекает ступенчато, характеризуется несколькими константами диссоциации. Например:
Исходя из значений приведенных констант диссоциации можно отметить, что К¢ > К¢¢, т. е. процесс распада электролита на ионы идет активнее по первой ступени.
Ионные реакции При взаимодействии растворов электролитов реакции происходят между ионами растворенных веществ. Химический процесс можно записать в молекулярной и ионно-молекулярной формах. Однако ионная форма отображает его точнее. При составлении ионных уравнений реакций вещества малодиссоциированные, малорастворимые (выпадающие в осадок) и газообразные изображаются в виде молекул:
1) H2SO4 + BaCl2 = BaSO4 ¯ + 2HCl 2H+ + SO42- + Ba2+ + 2Cl- = BaSO4 ¯ + 2H+ + 2Cl- – полное (развернутое) ионно-молекулярное уравнение; Ba2+ + SO42- = BaSO4 ¯ – сокращенное ионно-молекулярное уравнение. Сокращенное ионно-молекулярное уравнение указывает на то, что в реакции участвуют только ионы Ва2+ и сульфат - ионы SO42-.
2) Na2CO3 + 2HCl = 2NaCl + H2O + CO2 2Na+ + CO32- + 2H+ + 2Cl = 2Na+ + 2Cl- + H2O + CO2 СО32- + 2Н+ = Н2О + СО2 . Водородный показатель среды Вода является слабым электролитом и диссоциирует по уравнению
Константа диссоциации воды весьма мала: [H+] • [OH-] K = ¾¾¾¾¾ = 1,8 • 10-16. [H2O] Принимая концентрацию воды [Н2O] величиной практически постоянной и учитывая, что молярная концентрация воды в воде равна 1000/18 = 55,56 моль/л, получаем [H+] • [OH-] = 1,8 • 10-16 • 55,56 = 1 • 10-14 = К H2O. Произведение концентрации ионов водорода и ионов гидроксида называется ионным произведением воды. Так как при диссоциации одной молекулы воды получается один ион водорода и один ион гидроксида, то [H+] = [OH-] = 10-7 моль/л. Если к воде прибавить кислоту, то [H+] > 10-7 моль/л, а если прибавить щелочь, то [H+] < 10-7 моль/л. Таким образом, степень кислотности или щелочности раствора можно выразить с помощью концентрации ионов [H+] или [OH-].
|
||||||||
|
Последнее изменение этой страницы: 2016-04-08; просмотров: 403; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.116.24.148 (0.008 с.) |


 HClO H+ + ClO-
HClO H+ + ClO-
 H2S H+ + HS- К¢дис = 1,02 • 10-7,
H2S H+ + HS- К¢дис = 1,02 • 10-7,
 HS- H+ + S2- К¢¢дис = 1,3 • 10-13.
HS- H+ + S2- К¢¢дис = 1,3 • 10-13.
 Н2О Н+ + ОН-.
Н2О Н+ + ОН-.
 NaCH3COO + H2O NaOH + CH3COOH
NaCH3COO + H2O NaOH + CH3COOH
 Na+ + CH3COO- + H2O Na+ + OH- + CH3COOH
Na+ + CH3COO- + H2O Na+ + OH- + CH3COOH
 CH3COO- + H2O OH- + CH3COOH рН > 7
CH3COO- + H2O OH- + CH3COOH рН > 7
 2Na+ + CO32- + H2O Na+ + HCO3- + Na+ + OH-
2Na+ + CO32- + H2O Na+ + HCO3- + Na+ + OH-
 CO32- + H2O HCO3- + OH- pH > 7
CO32- + H2O HCO3- + OH- pH > 7
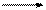 NaHCO3 + H2O NaOH + H2CO3
NaHCO3 + H2O NaOH + H2CO3
 HCO3- + H2O OH- + H2CO3 pH > 7
HCO3- + H2O OH- + H2CO3 pH > 7
 ZnCl2 + H2O ZnOHCl + HCl
ZnCl2 + H2O ZnOHCl + HCl
 Zn2+ + 2Cl- + H2O (ZnOH)+ + Cl- + H+ + Cl-
Zn2+ + 2Cl- + H2O (ZnOH)+ + Cl- + H+ + Cl-
 Zn2+ + H2O (ZnOH)+ + H+ pH < 7
Zn2+ + H2O (ZnOH)+ + H+ pH < 7
 CH3COONH4 + H2O CH3COOH + NH4OH
CH3COONH4 + H2O CH3COOH + NH4OH
 CH3COO- + NH4+ NH4OH + CH3COOH
CH3COO- + NH4+ NH4OH + CH3COOH
 Al(CH3COO)3 + H2O AlOH(CH3COO)2 + CH3COOH
Al(CH3COO)3 + H2O AlOH(CH3COO)2 + CH3COOH
 Al3+ + H2O (AlOH)2+ + CH3COOH
Al3+ + H2O (AlOH)2+ + CH3COOH
 AlOH(CH3COO)2 + H2O Al(OH)2CH3COO + CH3COOH
AlOH(CH3COO)2 + H2O Al(OH)2CH3COO + CH3COOH
 (AlOH)2+ + H2O Al(OH)+ + CH3COOH
(AlOH)2+ + H2O Al(OH)+ + CH3COOH
 Al2S3 + 6H2O 2Al(OH)3 ¯ + 3H2S.
Al2S3 + 6H2O 2Al(OH)3 ¯ + 3H2S. NaCl + H2O NaOH + HСl
NaCl + H2O NaOH + HСl
 H2O H+ + OH-.
H2O H+ + OH-.


