
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
РАУЛЬ (Raoult), Франсуа МариСодержание книги Поиск на нашем сайте
(10 мая 1830 г. – 1 апреля 1901 г.) Французский химик Франсуа Мари Рауль родился в Фурн-ан-Веп, Нормандия. Первоначальное образование получил в Лионской коллегии; учился в Парижском университете. С 1853 г. был учителем в Реймском лицее, затем в колледже в Сен-Дье, а с 1865 г. в лицее в Сансе; в 1867-1901 гг. работал в Гренобльском университете, где был профессором химии (с 1870), а затем и деканом факультета. Научная деятельность Рауля началась в 1863 г.; его первые исследования относились к переходу химической энергии в энергию электрического тока. В своих исследованиях Рауль пытался объяснить различие между количеством теплоты, выделенным в гальваническом элементе и вычисленным по закону Джоуля-Ленца, различными вторичными процессами. Главной заслугой Рауля стали выполненные им исследования понижения температуры замерзания и понижения упругости пара (или, что то же самое, повышения температуры кипения) растворителя при введении в него растворенного вещества. Первая часть этих исследований была опубликована в 1882 г., и принадлежит к одним из первых блестящих исследований в области физической химии растворов. Рауль провёл многочисленные измерения температур замерзания и кипения водных и неводных растворов различных веществ и пришёл в выводу: количества различных веществ, которые вызывают одинаковое (по сравнению с чистым растворителем) понижение температуры замерзания или повышение температуры кипения, зависят только от их молекулярных масс. Законы Рауля дали возможность определять молекулярные массы по понижению температуры замерзания или по повышению температуры кипения разбавленных растворов. Рауль ввёл в химию термин "криоскопия"; сконструировал газовую горелку для газового анализа (1876), усовершенствованную позже Р. В. Бунзеном. Открыл закон понижения сжимаемости растворов с увеличением их концентрации, обнаружил тиофен в техническом бензоле.
Из этого закона, в частности, вытекает, что с повышением концентрации растворенного вещества в воде (т. е с уменьшением концентрации Кр1 воды) парциальное давление водяных паров над поверхностью раствора уменьшается. В этом случае, если водный раствор используется в качестве рабочего тела, вступающего в непосредственный контакт с воздухом, над его поверхностью образуется слой влажного воздуха, равновесного относительно данного раствора. Параметры воздуха над раствором будут отличаться от параметров насыщенного воздуха над водой. Парциальное давление водяного пара в воздухе над раствором, а также его влагосодержание и энтальпия определяются температурой раствора и температурой его замерзания. Особенность их использования состоит лишь в том, что относительная влажность
где р1 р1,0 —давление пара непосредственно над поверхностью раствора и воды. К наиболее существенным недостаткам водных растворов солей следует отнести значительную коррозионную активность. Особенно высокой коррозионной активностью по отношению к сталям и сплавам на основе железа обладают растворы бромистого лития. Поэтому в качестве конструктивных материалов при использовании бромистолитиевых растворов применяют латунь и медь. Меньшей коррозионной активностью обладают растворы хлористого лития, а также хлористого кальция и натрия. Коррозионную активность этих растворов можно свести к минимуму путем поддержания значения коэффициента электролитической диссоциации pH = 7 - 8,5. Для поддержания рН раствора на допустимом уровне следует добавлять ингибиторные добавки. Коррозионную активность хлористолитиевого раствора можно уменьшить применяя в качестве ингибиторов хромовые соли Na2CrO4 или К2Сr2О7, добавляемые в количестве 1—2% массы раствора. Для распространенного в системах кондиционирования с промежуточным теплоносителем раствора хлористого кальция в качестве ингибиторных добавок используют хромовую соль Na2Cr207-2H20. При температурах рабочих тел выше 20°С может применяться раствор нитрита натрия. Растворы натрита натрия являются (при концентрации 28%) коррозионно инертными по отношению к сталям и сплавам на основе железа. Нитрит натрия пожаро- и взрывобезопасен, но обладает некоторой ядовитостью, что требует определенной осторожности при обращении с ним. Список литературы: 1. Богословский В.Н. и др. Кондиционирование воздуха и холодоснабжение: Учебник для вузов / В.Н. Богословский, О.Я Кокорин, Л.В. Петров; Под ред. В.Н. Богословского. – М.:Стройиздат, 1985.- 367 с.,ил. 2. Самин Д. К. 100 великих ученых. - М.: Вече, 2000) 3. ВЛАЖНЫЙ ВОЗДУХ,ABOK СПРАВОЧНОЕ ПОСОБИЕ - 1 – 2004.Разработан творческим коллективом Некоммерческого Партнерства "Инженеры по отоплению, вентиляции, кондиционированию воздуха, теплоснабжению и строительной теплофизике" (НП "АВОК") канд. техн. наук М.Г. Тарабанов (НИЦ "Инвент"), канд. техн. наук В.Д. Коркин (СПбГАИЖСА), В.Ф. Сергеев (НИЦ "Инвент") 4.. Храмов Ю.А. Физики. Биографический справочник. М.: Наука, 1983. 400 с. 5. Большая советская энциклопедия. В 30 тт. 6. Гоголин А.А. Кондиционирование воздуха в мясной промышленности. - М., "Пищевая промышленность", 1966 7. ASHRAE HANDBOOK. FUNDAMETALS. ASHRAE, Atlanta, 2001.
|
||||
|
Последнее изменение этой страницы: 2016-04-07; просмотров: 379; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.235.107 (0.009 с.) |

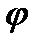 1 = const над раствором будет отличаться от
1 = const над раствором будет отличаться от 


