
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Диаграмма состояний III рода ⇐ ПредыдущаяСтр 6 из 6
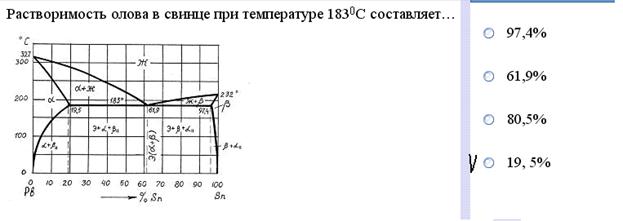
(Сплавы с ограниченной растворимостью компонентов в твердом состоянии) Диаграмма состояния сплавов, образующих твердые растворы с ограниченной растворимостью компонентов представлены на рис. 4.3. Выше линии ликвидуса АСВ все сплавы из компонентов А и Б (например, Сu и Аg) находятся в виде жидких растворов (рис. 4.3). Ниже линии солидуса AD СЕВ все сплавы находятся в твердом состоянии в виде трех структурных областей (трех фаз): 1) твердого раствора α-фазы — раствор компонента Б в А (Аg в Сu); 2) твердого раствора β-фазы — раствор компонента А в Б (Си в Аg); 3) и между этими областями размещены сплавы, состоящие из смеси α - и β - твердых растворов (область FDСЕG). Максимальные концентрации α - и β - твердых растворов имеют место при температуре, отвечающей линии DСЕ (для сплавов системы Сu—Аg 779°С). При охлаждении сплавов до 0˚С концентрация компонента Б в α -твердом растворе уменьшается, см, кривую DF (Аg уменьшается в α -твердом растворе); уменьшается также концентрация компонента A в β-твердом растворе, см. кривую ЕG (Сu уменьшается в β -твердом растворе). Если при температуре 779˚С Au в α -твердом растворе содержится 7%, а Сu в β -растворе — 8%, то при 0°С концентрация Аg в а-твердом растворе уменьшается до 0%, а концентрация Сu в β-твердом растворе — до 1 %. Таким образом, состав α,- и β - фазы переменен и с понижением температуры раствора изменяется.
Рис. 4.3.3,а. Диаграмма состояния сплавов, образующих твердые растворы с ограниченной растворимостью компонентов, в общем виде.
Рис. 4.3.3,б. Диаграмма состояния сплавов, образующих твердые растворы с ограниченной растворимостью компонентов, для системы Cu-Ag.
Твердые растворы α- и β- фазы с максимальной концентрацией растворимого компонента (соответственно Б и А) образуются между линиями ликвидуса и солидуса. В этих областях α- и β- фазы находятся вместе с жидким раствором. На линии DСЕ сплавы затвердевают и образуют механическую смесь кристаллов α-твердого раствора и β-твердого раствора. Двухкомпонентные сплавы, в которых происходит одновременная кристаллизация α- и β- фазы при постоянной и самой низкой для данной системы температуре, называются эвтектическими, а структура - их эвтектикой. Эвтектический сплав образуется в точке С. Сплавы, располагающиеся влево от эвтектического состава (левее точки С) и имеющие концентрацию компонентов в пределах точек D и С, называются доэвтектическими, а справа точки С — в пределах точек С и Е — заэвтектическими.
Как уже отмечалось, с понижением температуры растворимость компонента Б в α-фазе и компонента А в β-фазе все время снижается. В результате а- и β-твердые растворы становятся пересыщенными и происходит вторичная кристаллизация: компонент Б выделяется из α-фазы, образуя отдельные кристаллы, называемые вторичными (βII), а компонент А - из (β-фазы, образуя вторичные кристаллы (αII). Эти вторичные кристаллы находятся не в структурно свободном состоянии, а в виде твердого раствора; α11-это твердый раствор А в Б, а βII- твердый раствор Б в А. Таким образом, при понижении температуры на линии DC выделяются вторичные кристаллы βII, а на линии ЕС- вторичные кристаллы α11. Следовательно, в левой области диаграммы состояния образуется гетерогенная структура, представляющая механическую смесь кристаллов твердого раствора α и вторичных кристаллов βII., а в правой - гетерогенная структура из смеси кристаллов β + αII. В доэвтектических сплавах (ниже линии DС) при охлаждении из α-фазы выделяется βII - фаза и образуется гетерогенная структура (конгломератного типа), состоящая из эвтектики плюс α- и βII-фаза. В заэвтектических сплавах (ниже линии СЕ) при охлаждении из β -фазы выделяется αII-фаза и образуется гетерогенная структура из эвтектики плюс β - и αII - фаза.
.
I.4. Диаграмма “Железо-цементит”
Строение и свойства железа Железо при обычных температурах имеет о.ц.к. решетку и его называют α-Fe.
При нагреве до температуры 910°С Fe сохраняет решетку объемноцентрированного куба. Однако, начиная с температуры 770˚С и выше, Fe становится немагнитным (парамагнетиком). Это Fe часто называют β-Fe. При температуре 910°С происходит перегруппировка атомов, и решетка становится г.ц.к.; такое железо называют γ-Fe. При температуре 1400°С вновь происходит перегруппировка атомов Fe, и образуется решетка о.ц.к. Это высокотемпературное α-Fe нередко называют δ-Fe. При температуре 1539°С
Критическая температура превращения γ-Fe ↔ α-Fe (δ-Fe) при 1400°С (1392°С) обозначают точкой Ac4 (Ar4 ), температуру превращения α-Fe (β -Fe) ↔ γ -Fe при 910°C (898°C) - точкой Ac3 (Ar3). Температуру Кюри, равную 770°С (768°С), обозначают точкой Ас2(Аr2). При переходе α -Fe в γ -Fe кристаллическая решетка перестраивается из о.ц.к. в г.ц.к., при этом происходит ее объемное сжатие.
4.4.2. Компоненты и фазы в сплавах системы железо − углерод Основными компонентами сплавов системы Fe − С является железо и углерод. Углерод − неметаллический элемент. Его плотность — 2,5 Мг/м3, Тпл = 3500°С. Он полиморфен и в обычных условиях находится в виде графита. Графит имеет решетку гексагональную, слоистую; обладает низкой прочностью и относительно невысокой электропроводностью. Углерод растворяется в Fe, образуя жидкие и твердые растворы, а также образует с Fe химическое соединение − цементит (карбид железа Fe3C). В высокоуглеродистых сплавах (в чугунах) углерод может находиться еще и в виде свободного графита. Основными фазами и структурными составляющими сплавов системы Fe − С, от которых зависят свойства и поведение сплавов при механических и тепловых нагрузках, являются: феррит Ф, аустенит А, цементит Ц и продукты их эвтектического и эвтектоидного превращения: ледебурит Л и перлит П. Феррит (от лат. ferrum − железо) − это твердый раствор углерода в α-железе. Различают низкотемпературный а-Ф с растворимостью углерода до 0,02% и высокотемпературный δ-Ф с предельной растворимостью углерода 0,1%. Атомы растворенного углерода в Ф располагаются в центре граней о.ц.к. решетки, а также в вакансиях, на дислокациях и других дефектах. Феррит имеет невысокие твердость (НВ Аустенит (по имени английского ученого Аустена) − это твердый раствор углерода (и других элементов) в γ-Fe. Атомы растворенного в аустените углерода располагаются в центре элементарных ячеек г.ц.к. решетки. В зависимости от температуры, в А углерода может раствориться до 2,14% (при Т= 1147°С), т.е. больше, чем в Ф. Аустенит обычно существует только при Т> 727°С. При комнатной температуре он иногда в небольшом количестве сохраняется только в закаленной стали. Аустенит пластичен, его твердость НВ=160-200 кгс/мм2, прочность σ=1600—2000 МПа, δ = 40—50%. А − парамагнетик, хуже проводит электрический ток и тепло, чем Ф. Способность α- и γ-Fe растворять неодинаковое количество углерода играет важную роль при термической и химико-термической обработке стали. Цементит (указывает на твердость этой фазы) — это химическое соединение Fe с С − карбид железа Fe3C. Содержание углерода в Ц 6,67%, температура плавления точно не установлена в связи с возможностью его распада и принимается равной примерно 1550°С (в литературе встречается и 1600°, и 1250°С). Цементит при определенных условиях может распадаться на феррит и графит. До температуры 210°С (точка Ао) Ц слабо магнитен, выше − становится практически немагнитным. Цементит является самой твердой и хрупкой фазой в сплавах Fe − С. Его твердость составляет НВ=800 кгс/мм2, прочность σ=8000 МПа, а пластичность практически равна нулю, поэтому он способен только к небольшим упругим деформациям. Чем больше Ц в сплавах Fe − С, тем большей твердостью и меньшей пластичностью они обладают (например, чугуны).
Различают цементит Ц первичный ЦI, − кристаллизуется непосредственно из жидкого раствора системы Fe − С, вторичный ЦII − продукт распада аустенита и третичный ЦIII − продукт распада феррита. Ледебурит (по имени немецкого ученого Ледебура) имеет эвтектическую структуру (колониального типа), состоящую из аустенита и цементита, одновременно кристаллизующихся из жидкого раствора при постоянной температуре, равной 1147°С. Ледебурит содержит углерода 4,3%. Он присутствует во всех затвердевших сплавах, содержащих углерод от 2,14 до 6,67%, называемых чугунами (в сталях его нет). Образование Л идет из жидкого раствора по схеме
(цифры в этой схеме и в схеме, приведенной ниже, указывают содержание углерода в данной фазе). Таким образом, при 1147°С имеет место эвтектическое превращение, в результате которого образуется ледебурит. При температурах выше 727°С ледебурит представляет собой аустенитно-цементитную эвтектику и обозначается через Ла. При температурах, равной и ниже 727°С, аустенит превращается в перлит (см. ниже) и образуется структура, содержащая перлит и цементит. Эта структура обозначается буквой Лп. Ледебурит − твердая и хрупкая структурная составляющая чугунов. При обычных температурах его твердость НВ=650 кгс/мм2, прочность σ=6500 МПа. Перлит (от франц. perle — жемчуг, указывает на перламутровый отлив шлифа) − представляет собой эвтектоидную структуру, состоящую из смеси зерен (пластинок) феррита и цементита, образующуюся при постоянной температуре, равной 727°С в результате распада аустенита. При остывании Л до 727°С содержание в нем углерода становится равным 0,8%. Распад происходит по схеме
Распад Л называют эвтектоидным превращением, а образующуюся смесь тонких пластинок цементита и расположенных между ними более толстых пластинок феррита − эвтектоидной. Вообще эвтектоидным превращением называют процесс, когда твердый раствор определенного состава (в данном случае аустенит) при постоянной температуре трансформируется в структуру, состоящую из новых твердых фаз (в данном случае Ф и Ц). Перлит образуется как в сталях, так и в чугунах и играет важную роль в формировании их механических характеристик. Механические свойства П определяются формой и размером частиц цементитной фазы; чем мельче смесь, тем лучше свойства. Пластинчатый перлит имеет
НВ=180-220 кгс/мм2, σ=1800—2200 МПа, δ = 20%.
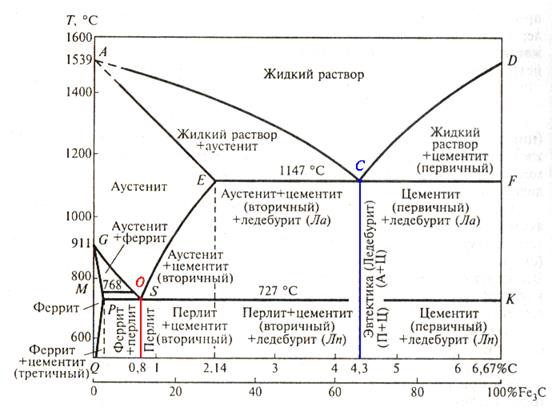
4.4.3. Диаграмма состояния сплавов системы железо−углерод Диаграмма состояния сплавов железа с углеродом дает возможность определить строении углеродистых сталей и чугунов в зависимости от содержания углерода и температуры, выбрать режимы термической и других видов обработки. На рис. 4.4.2 представлена упрощенная диаграмма состояния сплавов системы Fe − С (Fe − Fe3C). Диаграмма построена по содержанию углерода в количестве от 0 до 6,67% или по содержанию цементита от 0 до 100%. На диаграмме точка A (1539°С) соответствует Тпл (Тзат) Fe, а точка D (~1550°С) − Тпл (Тзат) цементита. Линия ACD − это линия ликвидуса, которая показывает температуру начала затвердевания (конца плавления) сталей и белых чугунов. Выше линии ACD сплавы находятся в жидком состоянии. Линия AECF- это линия солидуса, которая показывает температуру конца затвердевания (начала плавления) всех сплавов системы Fe − С.
Рис. 4.4.2. Упрощенная диаграмма состояний соединения «железо-цементит» По линии ликвидуса АС при температурах, соответствующих этой линии, из жидкого раствора кристаллизуется аустенит, а на линии CD − первичный цементит ЦI. В точке С при температуре 1147°С и содержании углерода 4,3% из жидкого раствора одновременно кристаллизуются А и ЦI, образуя эвтектику, называемую ледебуритом. На линии солидуса АЕ при температурах, соответствующих этой линии, окончательно затвердевают сплавы Fe-С с содержанием углерода до 2,14% и образуется структура аустенита. Сплавы Fe с содержанием углерода до 2,14% называют сталями. Стали - это сплавы железа Fe с углеродом С, в которых в результате первичной кристаллизации в равновесных условиях образуется аустенитная структура. На линии солидуса ЕС (температура 1147°С) окончательно затвердевают сплавы Fe − С с содержанием углерода от 2,14 до 4,3%, и образуется эвтектика ледебурита. Поскольку при более высоких температурах из жидкого раствора выделяется аустенит, такие сплавы после затвердевания имеют структуру, представляющую смесь аустенита и ледебурита (А + Ла). На линии солидуса CF (1147°С) окончательно затвердевают сплавы Fe − С с содержанием углерода от 4,3 до 6,6%. При этом также образуется структура ледебурита. Вследствие того, что при более высоких температурах из жидкого раствора выделяется цементит (первичный), такие сплавы после затвердевания (при 1147°С) имеют структуру, представляющую смесь первичного цементита и ледебурита (ЦI + Ла).
Таким образом, на линии ECF жидкие сплавы эвтектического состава кристаллизуются с образованием ледебурита, поэтому линию температур ECF называют линией эвтектического равновесия. Ледебурит присутствует во всех затвердевших сплавах, содержащих углерод от 2,14 до 6,67%. Такие сплавы называют чугунами.Если цвет излома чугуна серебристо-белый, такой чугун называют белым; в нем практически весь углерод находится в связанном состоянии в виде цементита. Чугуны с включениями графита называют серыми. В области АСЕ находится смесь двух фаз - жидкого раствора и кристаллов аустенита. В области CDF находится смесь, также состоящая из двух фаз - жидкого раствора и кристаллов цементита (первичного). В области AGSE в результате первичной кристаллизации образуется однофазная структура - аустенит. При охлаждении твердых сплавов в них происходят фазовые и структурные изменения, связанные с аллотропическими превращениями Fe и изменением растворимости в нем углерода. Эти изменения (фазовые превращения) в сплавах Fe − С характеризуют линии GSE, PSK, GPQ. Линия GS показывает начало превращения аустенита в феррит, а линия GP - конец этого превращения, имеющего место при охлаждении. Поэтому в области GSP будет двухфазная структура, состоящая из аустенита и феррита. Критические точки А3 лежат на линии GS. Линия SE показывает, что с понижением температуры твердых растворов растворимость углерода в аустените уменьшается. Если при 1147°С в аустените углерода содержится 2,14%, то при 727°С − 0,8%. В сталях с содержанием углерода от 0,8 до 2,14% с понижением температуры из аустенита выделяется избыточный углерод, который образует вторичный цементит ЦII. Следовательно, ниже линии SE (до температуры 727°С) сталь имеет структуру, состоящую из А и ЦII. Критические точки, лежащие на линии SE, обозначают Аст. В чугунах с содержанием углерода от 2,14 до 4,3% при 1147°С, как уже отмечалось выше, структура состоит из А и Л. С понижением температуры из аустенита также начнет выделяться вторичный цементит. Поэтому ниже линии ЕС до температуры 727°С белые чугуны имеют структуру, состоящую из А, Л и ЦII. На «стальном» участке диаграммы «железо-цементит» точка S (углерода 0,8%) называется эвтектоидной точкой, а линия PSK - эвтектоидной линией. В связи с этим углеродистые стали в зависимости от содержания углерода подразделяются относительно эвтектоидной точки S на эвтектоидные (углерода 0,8%), доэвтектоидные (углерода менее 0,8%) и заэвтектоидные (углерода менее 0,8%). Линия PSK ( 727°С ) − это линия эвтектоидного равновесия. Ниже температуры 727°С сплавы Fe − С имеют следующие структуры: − стали с содержанием углерода 0,8% имеют структуру перлита и называются эвтектоидпыми сталями (структуру см. рис. 10.15, в, г); − стали с содержанием углерода от 0,02% при 727°С (-0,006% при 20°С) до 0,8% имеют структуру, состоящую из Ф и П, и называются доэвтектоидными сталями. Железо, содержащее углерода 0,02% и менее и имеющее однофазную структуру Ф, называют технически чистым железом(общее содержание примеси не более 0,1 - 0,2%). − стали с содержанием углерода от 0,8 до 2,14% имеют структуру, состоящую из П и ЦII, и называются заэвтектоидными сталями.
При температуре ниже 727°С микроструктура эвтектоидных сталей состоит только из перлита, доэвтектоидных − из феррита и перлита, заэвтектоидных − из перлита и цементита вторичного. На «чугунном» участке диаграммы точка С (углерода 4,3%) называется эвтектической точкой, а линия ЕС - эвтектической линией. Чугуны по аналогии с углеродистыми сталями в зависимости от содержания углерода, но уже относительно эвтектической точки С, подразделяются на эвтектические (углерода 4,3%), доэвтектические (углерода менее 4,3%) и заэвтектические (углерода более 4,3%). При температуре ниже 727°С структура эвтектических чугунов состоит из эвтектики ледебурита низкотемпературного (Лп), доэвтектических чугунов − из перлита и ледебурита (Лп) и заэвтектичеекпх чугунов − из ледебурита (Лп) и цементита первичного (Щ, Белые чугуны с содержанием углерода 4,3% имеют структуру ледебурита, представляющего при температурах ниже 727°С смесь П и ЦЛа, а выше 727°С − смесь А и Ц(Лп). Называют эти чугуны эвтектическими. Белые чугуны с содержанием углерода от 2,14 до 4,3% ниже температуры 727°С имеют структуру, представляющую смесь П, Лп и ЦII, называются доэвтектическими чугунами (см. рис. 10.16, а). Белые чугуны с содержанием углерода от 4,3 до 6,67% ниже 727°С имеют структуру, состоящую из смеси ЦI и Лп. Их называют заэвтектическиыи чугунами. Таким образом, при температуре 727°С происходит окончательный распад аустенита и превращение его в перлит. Линия PQ показывает, что с понижением температуры растворимость углерода в феррите уменьшается от 0,02% при 727°С до 0,006% при комнатной температуре и из феррита выделяется углерод и виде третичного цементита ЦIII. В большинстве сплавов Fe − С третичный цементит структурно не выявляется. Линия МО (температура Кюри равна 768°C) показывает, что при нагревании ферромагнитный феррит переходит в парамагнитный, а при охлаждении наоборот. Для равновесных сплавов (т.е. отожженных образцов) системы Fe − С при Т< 727°С, включая комнатную, все структуры, охватываемые диаграммой Fe − С при содержании углерода от 0% (0% Fc3C) до 6,67% (100% Fe3C), состоят только из двух фаз − феррита и цементита, находящихся в них в разных количественных соотношениях.
|
|||||||||
|
Последнее изменение этой страницы: 2017-02-19; просмотров: 672; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.126.74 (0.036 с.) |




 5°С Fе плавится.
5°С Fе плавится.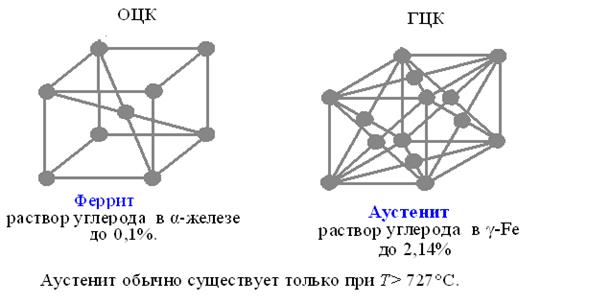
 80 кгс/мм2) и прочностью (σв= 250 МПа) и высокую пластичность: его относительное удлинение перед разрывом δ = 50%. Поэтому технически чистое Fe (применяется в электротехнике), структуру которого представляют зерна феррита, хорошо подвергается холодной деформации, т.е. хорошо штампуется, прокатывается, протягивается в холодном состоянии. Чем больше феррита в Fe − C сплавах, тем они более пластичны.
80 кгс/мм2) и прочностью (σв= 250 МПа) и высокую пластичность: его относительное удлинение перед разрывом δ = 50%. Поэтому технически чистое Fe (применяется в электротехнике), структуру которого представляют зерна феррита, хорошо подвергается холодной деформации, т.е. хорошо штампуется, прокатывается, протягивается в холодном состоянии. Чем больше феррита в Fe − C сплавах, тем они более пластичны.













