Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Органических кислот на твёрдых адсорбентах”.Содержание книги
Поиск на нашем сайте
В лабораторной работе исследуют процесс адсорбции из раствора уксусной кислоты на активированном угле. Перед началом работы тщательно промывают хромовой смесью, обычной водой, а затем дистиллированной водой 6 рабочих колб. В одну из них получают исходный раствор уксусной кислоты у преподавателя. Затем из исходного раствора готовят еще пять растворов путем разбавления каждого вдвое. Для этого в пять сухих колб наливают пипеткой по 50 мл дистиллированной воды. Затем отбирают пипеткой из колбы 50 мл исходного раствора, вносят их в первую из пяти приготовленных колб, хорошо взбалтывают, затем несколько раз набирают этот раствор в пипетку и выливают его обратно в ту же колбу, таким образом споласкивая пипетку приготовленным раствором. Отбирают из этой колбы 50 мл приготовленного раствора и переносят его во вторую колбу, снова хорошо перемешивают, так же как в предыдущем случае, споласкивают пипетку новым раствором и повторяют эту операцию до тех пор, пока не будут приготовлены все шесть растворов, включая исходный. Взвешивают шесть навесок активированного угля по 1 г каждая и вносят их по одной в каждую из шести колб с растворами. Встряхивают колбы с углем (порядка 2-3 минут) и оставляют в покое примерно на 50 -60 минут. Это свободное время используют для определения концентрации исходного раствора уксусной кислоты, который был получен у преподавателя. Делают это посредством титрования трех аликвот исходного раствора (по 10 мл каждая) раствором NaOH с известной концентрацией (этот раствор установлен в специальных емкостях непосредственно возле рабочего места).. По уравнению: 10мл*Nк-ты = VNaOH(мл)*NNaOH рассчитывают концентрацию в каждой пробе кислоты. Вычисляют среднюю концентрацию исходного раствора и проверяют её у преподавателя. По истечении 50-60 минут отфильтровывают приготовленные растворы, отбрасывая первые порции (около 10мл) фильтрата. Оставшийся раствор используют для титрования кислоты тем же раствором щёлочи, что и для исходного раствора (титруют по три порции каждого раствора). Полученные значения сх записывают в таблицу. Заметим, что до адсорбции нужно оттитровать только исходный раствор, а концентрации в остальных колбах после разведения просто рассчитывают посредством уменьшения в два раза концентрации кислоты в каждой последующей колбе. Полученные данные вносят в таблицы, как показано в образце оформления протокола работы, после чего строят график для определения констант в уравнении Фрейндлиха (рис.IX.11). Образец оформления протокола по лабораторной работе №3. Выполнил студент … группы …..курса ….. Определение концентрации исходной кислоты посредством титрования 0.108N NaOH. Таблица №1
Формула для расчета: Vк-тыNк-ты = VNaOHNNaOH; т.к. С NaOH = 0.108, то Сисходн. к-ты = (34.8*0.1080)/10 = 0.3683 моль/л. Путём последовательного разбавления исходной задачи с концентрацией кислоты 0,3683 моль/л вдвое приготовим ещё 5 растворов с концентрациями: 1) 0,1842 моль/л; 2) 0,0921 моль/л; 3) 0,0460 моль/л; 4) 0,0230 моль/л; 5) 0,0115 моль/л К каждому из этих шести растворов добавим по 1 г угля и оставим на 1 час. (Это время целесообразно использовать для титрования исходного раствора кислоты.) Затем отфильтруем уголь, а фильтраты употребим для титрования по три порции каждая по 10 мл всё тем же раствором щёлочи (С NaOH = 0,108 моль/л). Результаты титрования поместим в Таблицу №2
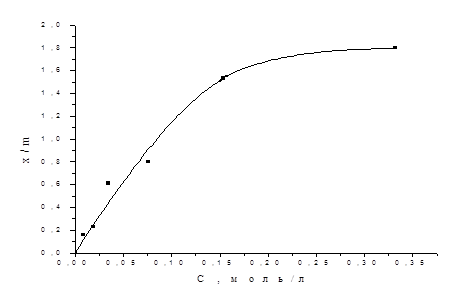
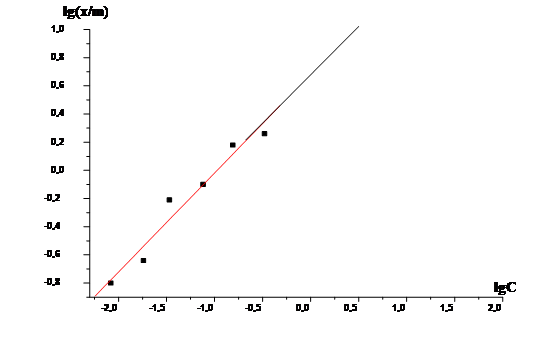
Расчет величин x/m проводят по формуле (IX.11), которая с учетом массы адсорбента в 1г, объема раствора 50мл и коэффициента перевода концентрации в ммоль/л, равного 1000, выглядит как: (IX.12) x/m = (с0 –сх)* 50 Результаты расчётов поместим в Таблицу №3
Изотерма адсорбции
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-10; просмотров: 220; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.22.42.25 (0.005 с.) |