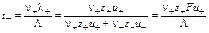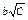Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема: растворы неэлектролитовСодержание книги
Поиск на нашем сайте
Зависимость давления р пара растворителя в равновесии с идеальным раствором от мольной доли х растворителя в растворе (закон Рауля)
р = хр o
р o - давление насыщенного пара чистого* растворителя. То же, выраженное через мольную долю растворенного вещества х 2 в двухкомпонентной системе: (р o – р)/ р o = х 2 Понижение температуры Т замерзания идеального разбавленного раствора по сравнению с температурой замерзания чистого растворителя Т о : D Т = K cryo m, где D Т = Т о – Т, m – моляльность, М – молярная масса чистого растворителя, D Н пл – молярная энтальпия плавления растворителя. Повышение температуры кипения идеального разбавленного раствора Т по сравнению с температурой кипения чистого растворителя Т о : D Т = K ebu m, где D Т = Т – Т о, D Н исп – молярная энтальпия испарения растворителя. Осмотическое давление идеального разбавленного раствора:
p = CRT
Тема: растворы электролитов
Средний ионный коэффициент активности электролита, одна формульная единица которого образует n ионов (n+ катионов и n– анионов, n+ + n– = n):
где g+ и g– - индивидуальные коэффициенты активности катиона и аниона. То же для симметричного электролита (n+ = n–):
Коэффициент активности (g i) i -ого иона с зарядом zi и средний ионный коэффициент активности электролита, образующего ионы с зарядами z + и z – (I < 0.1 моль/л; уравнение Дебая-Хюккеля):
где А и В константы, åi - эффективный радиус иона, (А = 0.5092 (л/моль)1/2, В = 0.3301 л1/2 моль–1/2 Å–1 при 298.15 К, если растворитель – вода) То же при I < 0.01 моль/л (предельное уравнение Дебая Хюккеля):
Коэффициенты активности при I < 0.001 моль/л: g i» 1, g±» 1. Константа диссоциации слабого электролита в растворе
То же для слабого 1-1 электролита (z+ = |z–| = 1) КА ƒ К+ + А–:
где a - степень диссоциации, С – общая (валовая) концентрация электролита. Произведение растворимости K S твёрдого электролита (константа равновесия K S = где C S – растворимость (концентрация насыщенного раствора) То же для 1-1 электролита (z+ = |z–| = 1) КА(т) ƒ К+ (aq) + А– (aq): K S Ионное произведение воды: K W где K W = К [H2O] ×g, К – константа равновесия диссоциации воды. Константа кондуктометрической ячейки (определение):
К яч = k R W
где R W - электрическое сопротивление ячейки, k – удельная проводимость раствора. Выражение константы К яч через расстояние между электродами и площадь поверхности электродов К яч = L / S Молярная электрическая проводимость катионов и анионов (определение):
l+ = z + Fu +, l– = z – Fu –
Связь молярной электрической проводимости электролита с ионными проводимостями (закон Кольрауша независимого движения ионов)
L = n+l+ + n–l–
где l+ и l– - молярные электрические проводимости катиона и аниона, соответственно, L = k/с – молярная проводимость электролита по определению. Выражения для числа переноса катиона:
(аналогичные уравнения справедливы для числа переноса аниона) Эмпирическая зависимость проводимости сильного электролита от концентрации (уравнение Кольрауша, "закон квадратного корня") L = Lo – где b - эмпирический коэффициент, Lo – предельная молярная проводимость (проводимость электролита при бесконечном разбавлении раствора). Степень диссоциации слабого электролита: a = L/Lo Выражение константы диссоциации слабого 1-1 электролита (z+ = |z–| = 1) через молярную проводимость (I < 0.001 моль/л; закон разведения Оствальда):
|
||
|
Последнее изменение этой страницы: 2017-02-09; просмотров: 545; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.20 (0.005 с.) |

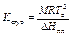
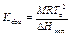
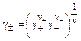
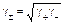
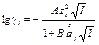 ;
; 
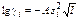 ;
; 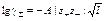
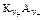 ƒ
ƒ 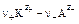 :
:
 =
= 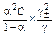
 ):
): =
= 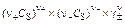
 =
=