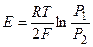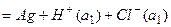Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Окислительно-восстановительные электроды
1. Понятие, функция электрода, электродная реакция Название окислительно-восстановительных электродов или
2. Примеры а) ферри-ферратный эл-д:
б) хингидронный:
Область работы: 0<pH<8 Основные типы гальванических элементов 1. Краткая характеристика элементов а) по источнику электрической энергии – физические, химические и концентрационные – в физических цепях источником эл. энергии служит различие в физическом состоянии электродов (аллотропические, гравита-ционные, термогальванические) – в химических гальванических элементах источником эл. энергии служит химическая энергия реакции, протекающей в элементе – концентрационными наз. элементы, в которых оба электрода одинаковы по своей природе, но различаются активностями одного или нескольких веществ - участников электродной реакции. Электрическая энергия в них получается за счет разности концентраций электрохимически активных веществ в двух одинаковых по химической природе электродах б) по наличию границы жидких фаз (без и с переносом) Химические гальванические элементы а) простые химические цепи, понятие (1 раствор) 1) элемент из водородного и хлорсеребряного электродов
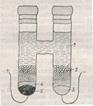
а) состав и устройство элемента Вестона, б) условная запись эл-та и ур-ние реакции
в) применение элемента – источник стандартной ЭДС
б) сложные химические элементы (2 раствора) 1) элемент Якоби-Даниэля, 2) вывод уравнения Нернста элемента Я-Д через
3) недостаток – наличие диффузионного потенциала 4) химический г.э. – хим. источник электрической энергии Концентрационные гальванические элементы 1. Понятие, элементы с переносом и без переноса Элементы с переносом Концентрационными элементами с переносом наз. элементы, составленные из одинаковых по химической природе электродов, но с разными по концентрациям растворами электролитов, причем между р-рами имеется непосредственная граница соприкосновения
т.о. в ходе работы элемента происходит перенос потенциал-определяющих ионов из одного полуэлемента в другой и при выравнивании концентраций работа элемента прекращается 2. Элементы без переноса 1) амальгамные,
2) газовые, 3) эл. цепь из двух хим. элементов с одним раствором электролита, включенных навстречу друг другу
+
|
|||||
|
Последнее изменение этой страницы: 2017-01-25; просмотров: 113; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.219.95.244 (0.005 с.) |
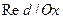 -электродов закрепилось за группой электродов, которые представляют собой инертный проводящий материал
-электродов закрепилось за группой электродов, которые представляют собой инертный проводящий материал 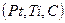 , погруженный в раствор, содержащий и окисленную, и восстановленную формы одного и того же элемента.
, погруженный в раствор, содержащий и окисленную, и восстановленную формы одного и того же элемента.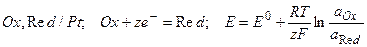
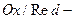 электродов, потенциал которых
электродов, потенциал которых 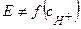 :
: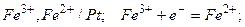

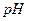
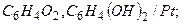

 .
.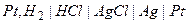

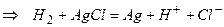
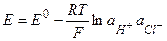
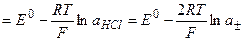
 2) пример – элемент Вестона
2) пример – элемент Вестона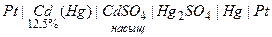 ,
, 


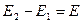
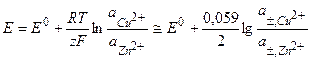
 ,
, 

 ,
, 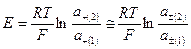
 где
где 

 ,
,