Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Электродвижущая сила (ЭДС) гальванического элемента
ЭДС – разность потенциалов на концах правильно разомкнутого гальванического элемента 1. Условная схема электрохимической цепи: 2. Запись ЭДС через гальвани-потенциалы:
т.к. 3. Условный электродный потенциал, а) необходимость введения условного электродного потенц-ла
в) определение условного электродного потенциала в водородной шкале, г) уравнение для условного электродного потенциала:
4. Связь ЭДС гальванического элемента с потенциалами электродов а) найдем разницу условных электродных потенциалов
б) сопоставление с уравнением для ЭДС данного элемента вывод Правило знаков ЭДС элементов и электродных потенциалов 1. Основополагающее правило – ЭДС положительна, если внутри гальванического элемента положительное электри-чество (катионы) перемещается слева направо (Стокгольм, международная конференция 1953г.) 2. Выводы. При разряде ионов на правом электроде - процесс восстановления (электрод заряжается положительно), а сам электрод – положительный полюс г.э. (катод); на левом электроде – процесс окисления (отрицательный полюс, анод). 3. Соответствие знака ЭДС системе знаков теории хим. сродства а) б) Термодинам. уравнение, связывающее ЭДС с активностями участников реакции, протекающей в г. элементе 1. Вывод уравнения: основан на теории хим. сродства: а) б) 2. 3. Пример – элемент Якоби-Даниэля: а) реакция: б) 4. Разбавленные растворы,
Классификация электродов Электроды I и II рода, газовые, Ox-Red эл-ды, мембранные Электроды 1го рода 1. Понятие, условная запись и электродный процесс
2. Вывод уравнения Нернста а) условная схема электрохимич. цепи и химическая реакция
б) 2. Примеры: а) б) амальгамный электрод, 4. Неметалл/раствор, Электроды 2го рода 1. Понятие, условная запись и потенциалопределяющая реакция на электроде 2 го рода: 2. Вывод уравнения Нернста а) условная схема электрохимич. цепи и химическая реакция
б) 3. Примеры а) б) в) ртутнооксидный эл-д:
4. Электроды 2го рода – как электроды сравнения а) недостатки водородного электрода 1) неудобен и опасен в эксплуатации (баллон с газообраз-ным водородом, сложность поддержания постоянства давления
2) чувствительность потенциала электрода к загрязнениям и микропримесям в растворе (отравление б) достоинства электродов 2-го рода 1) устойчивое и воспроизводимое от электрода к электроду значение потенциала 2) простота в изготовлении и эксплуатации в)
Газовые электроды 1. Понятие, устройство и функция электрода-катализатора Газовые электроды состоят из металлического проводника, который одновременно контактирует и с газом, пропускаемым через раствор электролита, и с самим раствором, содержащим ионы, природа которых соответствует продуктам окисления или восстановления этого газа на электроде. Металлический проводник, обычно, платиновая проволока, покрытая осадком платиновой черни, сам в электродной реакции участия не принимает, а выполняет лишь функцию инертного проводника и катализирует процесс установления адсорбционного равновесия. 2. Примеры а) водородный электрод,
б) кислородный электрод:
|
|||||
|
Последнее изменение этой страницы: 2017-01-25; просмотров: 313; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.42.94 (0.016 с.) |

 ;
;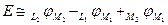 ,
,
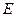
 б) стандартный водородный электрод,
б) стандартный водородный электрод,

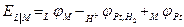
 ,
,








 и
и  , самопроизвольный процесс
, самопроизвольный процесс

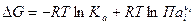
 , где
, где  при
при  .
.
 ,
,  ;
; 

 , т.к.
, т.к. 
 ,:
,: - уравнение Нернста (1890)
- уравнение Нернста (1890)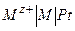 ,
, 






 ,
,  ,
, 
 :
: 
 :
:  ,
, 





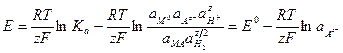
 ,
, 
 ,
, 
 ,
, ,
, 
 , взрывоопасен)
, взрывоопасен) )
) [(насыщ., 0,1н, 1н) каломельный, хлорсеребр.)
[(насыщ., 0,1н, 1н) каломельный, хлорсеребр.)

 ,
, 
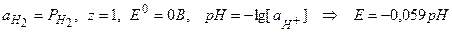
 ;
;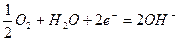
 ,
,