
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Модульная единица 1 структурная организация мономерных белков и основы их функционированияСтр 1 из 90Следующая ⇒
ТЕМА 1.1. СТРУКТУРНАЯ ОРГАНИЗАЦИЯ БЕЛКОВ. ЭТАПЫ ФОРМИРОВАНИЯ НАТИВНОЙ КОНФОРМАЦИИ БЕЛКОВ Белки - это полимерные молекулы, мономерами которых являются всего 20 α-аминокислот. Набор и порядок соединения аминокислот в белке определяется строением генов в ДНК индивидумов. Каждый белок в соответствии с его специфической структурой выполняет свойственную ему функцию. Набор белков данного организма определяет его фенотипические особенности, а также наличие наследственных болезней или предрасположенность к их развитию. 1. Аминокислоты, входящие в состав белков. Пептидная связь. Белки - полимеры, построенные из мономеров - 20 α-аминокислот, общая формула которых
К гидрофильным относятся радикалы, содержащие анионные, катионные и полярные незаряженные функциональные группы. К гидрофобным относятся радикалы, содержащие метильные группы, алифатические цепи или циклы. 2. Пептидные связи соединяют аминокислоты в пептиды. При синтезе пептида α-карбоксильная группа одной аминокислоты взаимодействует с α-аминогруппой другой аминокислоты с образованием пептидной связи:
Мономеры аминокислот, входящих в состав полипептидов, называются аминокислотными остатками. Цепь повторяющихся групп - NH-CH-CO - образует пептидный остов. Аминокислотный остаток, имеющий свободную α-аминогруппу, называется N-концевым, а имеющий свободную α-карбоксильную группу - С-концевым. Пептиды записывают и читают с N-конца к С-концу.
Пептидная связь, образуемая иминогруппой пролина, отличается от других пептидных связей: у атома азота пептидной группы отсутствует водород, вместо него имеется связь с радикалом, в результате одна сторона цикла включается в пептидный остов:
Пептидные связи очень прочные, и для их химического неферментативного гидролиза требуются жесткие условия: анализируемый белок гидролизуют в концентрированной соляной кислоте при температуре около 110° в течение 24 часов. В живой клетке пептидные связи могут разрываться с помощью протеолитических ферментов, называемых протеазами или пептидгидролазами. 3. Первичная структура белков. Аминокислотные остатки в пептидных цепях разных белков чередуются не случайным образом, а расположены в определенном порядке. Линейная последовательность или порядок чередования аминокислотных остатков в полипептидной цепи называется первичной структурой белка. Первичная структура каждого индивидуального белка закодирована в молекуле ДНК (в участке, называемом геном) и реализуется в ходе транскрипции (переписывания информации на мРНК) и трансляции (синтез первичной структуры белка). Следовательно, первичная структура белков индивидуального человека - наследственно передаваемая от родителей детям информация, определяющая особенности строения белков данного организма, от которых зависит функция имеющихся белков (рис. 1.2.).
Каждый из примерно 100 000 индивидуальных белков в организме человека имеет уникальную первичную структуру. В молекулах одного типа белка (например, альбумина) одинаковое чередование аминокислотных остатков, что отличает альбумин от любого другого индивидуального белка. Последовательность аминокислотных остатков в пептидной цепи можно рассматривать как форму записи информации. Эта информация определяет пространственную укладку линейной пептидной цепи в более компактную трехмерную структуру, называемую конформацией белка. Процесс формирования функционально активной конформации белка носит название фолдинг.
4. Конформация белков. Свободное вращение в пептидном остове возможно между атомом азота пептидной группы и соседним α-углеродным атомом, а также между α-углеродным атомом и углеродом карбонильной группы. Вследствие взаимодействия функциональных групп аминокислотных остатков первичная структура белков может приобретать более сложные пространственные структуры. В глобулярных белках различают два основных уровня укладки конформации пептидных цепей: вторичную и третичную структуры. Вторичная структура белков - это пространственная структура, формирующаяся в результате образования водородных связей между функциональными группами -С=О и - NH- пептидного остова. При этом пептидная цепь может приобретать регулярные структуры двух типов: α-спирали и β-структуры. В α-спирали водородные связи образуются между атомом кислорода карбонильной группы и водородом амидного азота 4-й от него аминокислоты; боковые цепи аминокислотных остатков располагаются по периферии спирали, не участвуя в образовании вторичной структуры (рис. 1.3.). Объемные радикалы или радикалы, несущие одинаковые заряды, препятствуют формированию α-спирали. Остаток пролина, имеющий кольцевую структуру, прерывает α-спираль, так как из-за отсутствия водорода у атома азота в пептидной цепи невозможно образовать водородную связь. Связь между азотом и α-углеродным атомом входит в состав цикла пролина, поэтому пептидный остов в этом месте приобретает изгиб. β-Структура формируется между линейными областями пептидного остова одной полипептидной цепи, образуя при этом складчатые структуры. Полипептидные цепи или их части могут формировать параллельные или антипараллельные β-структуры. В первом случае N- и С-концы взаимодействующих пептидных цепей совпадают, а во втором - имеют противоположное направление (рис. 1.4).
β-структуры обозначены широкими стрелками: А - Антипараллельная β-структура. Б - Параллельные β-складчатые структуры В некоторых белках β-структуры могут формироваться за счет образования водородных связей между атомами пептидного остова разных полипептидных цепей. В белках также встречаются области с нерегулярной вторичной структурой, к которым относят изгибы, петли, повороты полипептидного остова. Они часто располагаются в местах, где меняется направление пептидной цепи, например, при формировании параллельной β-складчатой структуры. По наличию α-спиралей и β-структур глобулярные белки могут быть разделены на четыре категории. В первую категорию включены белки, в которых имеются только α-спирали, например, миоглобин и гемоглобин (рис. 1.5). Во вторую категорию входят белки, в которых имеются и α-спирали, и β-структуры, например триозофосфатизомераза или похожий по структуре домен пируваткиназы (рис. 1.6). Рис. 1.5. Вторичная структура миоглобина (А) и β-цепи гемоглобина (Б), содержащие восемь α-спиралей
В третью категорию включены белки, имеющие только вторичную β-структуру. Такие структуры обнаружены в иммуноглобулинах, ферменте супероксиддисмутазе (рис. 1.7). В четвертую категорию включены белки, имеющие в своем составе незначительное количество регулярных вторичных структур. К таким белкам можно отнести небольшие, богатые цистеином белки или металлопротеины. Третичная структура белка - тип конформации, образующийся за счет взаимодействий между радикалами аминокислот, которые могут находиться на значительном расстоянии друг от друга в пептидной цепи. Большинство белков при этом формируют пространственную структуру, напоминающую глобулу (глобулярные белки). Так как гидрофобные радикалы аминокислот имеют тенденцию к объединению с помощью так называемых гидрофобных взаимодействий и межмолекулярных ван-дер-ваальсовых сил, внутри белковой глобулы образуется плотное гидрофобное ядро. Гидрофильные ионизированные и неионизированные радикалы в основном располагаются на поверхности белка и определяют его растворимость в воде.
1 - ионная связь - возникает между положительно и отрицательно заряженными функциональными группами; 2 - водородная связь - возникает между гидрофильной незаряженной и любой другой гидрофильной группой; 3 - гидрофобные взаимодействия - возникают между гидрофобными радикалами; 4 - дисульфидная связь - формируется за счет окисления SH-групп остатков цистеина и их взаимодействия друг с другом Гидрофильные аминокислотные остатки, оказавшиеся внутри гидрофобного ядра, могут взаимодействовать друг с другом с помощью ионных и водородных связей (рис. 1.8). Ионные и водородные связи, а также гидрофобные взаимодействия относятся к числу слабых: их энергия ненамного превышает энергию теплового движения молекул при комнатной температуре. Конформация белка поддерживается за счет возникновения множества таких слабых связей. Так как атомы, из которых состоит белок, находятся в постоянном движении, то возможен разрыв одних слабых связей и образование других, что приводит к небольшим перемещениям отдельных участков полипептидной цепи. Это свойство белков изменять конформацию в результате разрыва одних и образования других слабых связей называется конформационной лабильностью.
В организме человека функционируют системы, поддерживающие гомеостаз - постоянство внутренней среды в определенных допустимых для здорового организма пределах. В условиях гомеостаза небольшие изменения конформации не нарушают общую структуру и функцию белков. Функционально активная конформация белка называется нативной конформацией. Изменение внутренней среды (например, концентрации глюкозы, ионов Са, протонов и т.д.) приводит к изменению конформации и нарушению функций белков. Третичная структура некоторых белков стабилизирована дисульфидными связями, образующимися за счет взаимодействия -SH групп двух остатков
цистеина (рис. 1.9). Большинство внутриклеточных белков не имеет в третичной структуре ковалентных дисульфидных связей. Их наличие характерно для секретируемых клеткой белков, что обеспечивает их большую стабильность во внеклеточных условиях. Так, дисульфидные связи имеются в молекулах инсулина и иммуноглобулинов. Инсулин - белковый гормон, синтезирующийся в β-клетках поджелудочной железы и секретируемый в кровь в ответ на повышение концентрации глюкозы в крови. В структуре инсулина имеются две дисульфидные связи, соединяющие полипептидные А- и В-цепи, и одна дисульфидная связь внутри А-цепи (рис. 1.10).
5. Супервторичная структура белков. В разных по первичной структуре и функциям белках иногда выявляются сходные сочетания и взаиморасположение вторичных структур, которые называются супервторичной структурой. Она занимает промежуточное положение между вторичной и третичной структурами, поскольку это специфическое сочетание элементов вторичной структуры при формировании третичной структуры белка. Супервторичные структуры имеют специфические названия, такие как «α-спираль-поворот-а-спираль», «лейциновая застежка молния», «цинковые пальцы» и др. Такие супервторичные структуры характерны для ДНК-связывающих белков. «Лейциновая застежка-молния». Этот вид супервторичной структуры используется для соединения двух белков. На поверхности взаимодействующих белков имеются α-спиральные участки, содержащие не менее четырех остатков лейцина. Лейциновые остатки в α-спирали располагаются через шесть аминокислот один от другого. Так как каждый виток α-спирали содержит 3,6 аминокислотных остатка, радикалы лейцина находятся на поверхности каждого второго витка. Лейциновые остатки α-спирали одного белка могут взаимодействовать с лейциновыми остатками другого белка (гидрофобные взаимодействия), соединяя их вместе (рис. 1.11.). Многие ДНК связывающие белки функционируют в составе олигомерных комплексов, где отдельные субъединицы связываются друг с другом «лейциновыми застежками».
Примером таких белков могут служить гистоны. Гистоны - ядерные белки, в состав которых входит большое количество положительно заряженных аминокислот - аргинина и лизина (до 80%). Молекулы гистонов объединяются в олигомерные комплексы, содержащие восемь мономеров с помощью «лейциновых застежек», несмотря на значительный одноименный заряд этих молекул. «Цинковый палец» - вариант супервторичной структуры, характерный для ДНК-связывающих белков, имеет вид вытянутого фрагмента на поверхности белка и содержит около 20 аминокислотных остатков (рис. 1.12). Форму «вытянутого пальца» поддерживает атом цинка, связанный с радикалами четыре аминокислот - двух остатков цистеина и двух - гистидина. В некоторых случаях вместо остатков гистидина находятся остатки цистеина. Два близко лежащих остатка цистеина отделены от двух других остатков Гисили Циспоследовательностью, состоящей примерно из 12 аминокислотных остатков. Этот участок белка образует α-спираль, радикалы которой могут специфично связываться с регуляторными участками большой бороздки ДНК. Специфичность связывания индивидуального
регуляторного ДНК-связывающего белка зависит от последовательности аминокислотных остатков, расположенных в области «цинкового пальца». Такие структуры содержат, в частности, рецепторы стероидных гормонов, участвующих в регуляции транскрипции (считывание информации с ДНК на РНК).
|
|||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 560; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.1.158 (0.037 с.) |
 Аминокислоты различаются по строению, размерам, физико-химическим свойствам радикалов, присоединенных к α-углеродному атому. Функциональные группы аминокислот определяют особенности свойств разных α-аминокислот. Встречающиеся в α-аминокислотах радикалы можно разделить на несколько групп:
Аминокислоты различаются по строению, размерам, физико-химическим свойствам радикалов, присоединенных к α-углеродному атому. Функциональные группы аминокислот определяют особенности свойств разных α-аминокислот. Встречающиеся в α-аминокислотах радикалы можно разделить на несколько групп: Пролин, в отличие от других 19 мономеров белков, не аминокислота, а иминокислота, радикал в пролине связан как с α-углеродным атомом, так и с иминогруппой
Пролин, в отличие от других 19 мономеров белков, не аминокислота, а иминокислота, радикал в пролине связан как с α-углеродным атомом, так и с иминогруппой Аминокислоты различаются по растворимости в воде. Это связано со способностью радикалов взаимодействовать с водой (гидратироваться).
Аминокислоты различаются по растворимости в воде. Это связано со способностью радикалов взаимодействовать с водой (гидратироваться). Белки представляют собой полипептиды, т.е. линейные полимеры α-аминокислот, соединенных пептидной связью (рис. 1.1.)
Белки представляют собой полипептиды, т.е. линейные полимеры α-аминокислот, соединенных пептидной связью (рис. 1.1.) Рис. 1.1. Термины, используемые при описании строения пептидов
Рис. 1.1. Термины, используемые при описании строения пептидов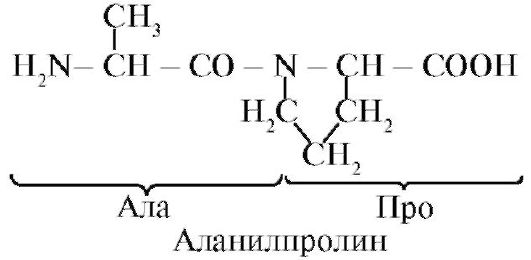 Пептиды различаются аминокислотным составом, количеством аминокислот и порядком соединения аминокислот, например, Сер-Ала-Глу-Гис и Гис-Глу-Ала-Сер - два разных пептида.
Пептиды различаются аминокислотным составом, количеством аминокислот и порядком соединения аминокислот, например, Сер-Ала-Глу-Гис и Гис-Глу-Ала-Сер - два разных пептида. Рис. 1.2. Взаимосвязь между генотипом и конформацией белков, синтезирующихся в организме индивидума
Рис. 1.2. Взаимосвязь между генотипом и конформацией белков, синтезирующихся в организме индивидума Рис. 1.3. Вторичная структура белка - α-спираль
Рис. 1.3. Вторичная структура белка - α-спираль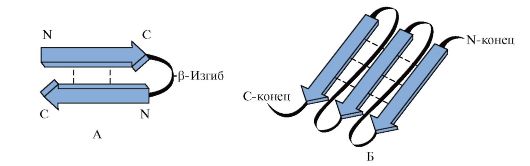 Рис. 1.4. Параллельные и антипараллельные β-складчатые структуры
Рис. 1.4. Параллельные и антипараллельные β-складчатые структуры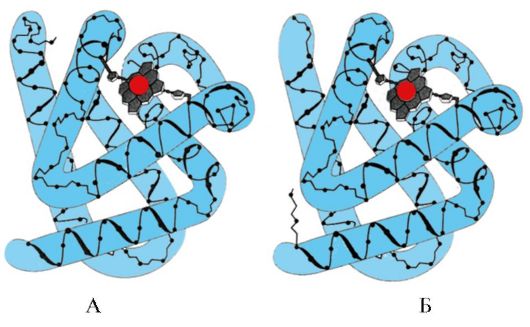
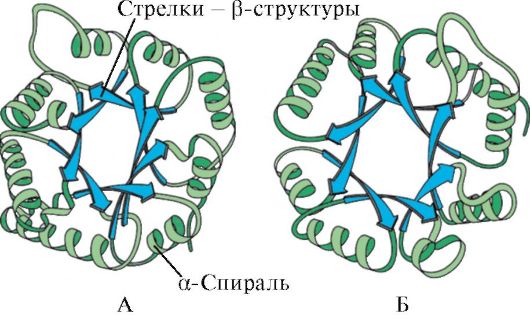 Рис. 1.6. Вторичная структура триозофосфатизомеразы и домена пируваткиназы
Рис. 1.6. Вторичная структура триозофосфатизомеразы и домена пируваткиназы Рис. 1.7. Вторичная структура константного домена иммуноглобулина (А) и фермента супероксиддисмутазы (Б)
Рис. 1.7. Вторичная структура константного домена иммуноглобулина (А) и фермента супероксиддисмутазы (Б) Рис. 1.8. Типы связей, возникающих между радикалами аминокислот при формировании третичной структуры белка
Рис. 1.8. Типы связей, возникающих между радикалами аминокислот при формировании третичной структуры белка Рис. 1.9. Образование дисульфидной связи в молекуле белка
Рис. 1.9. Образование дисульфидной связи в молекуле белка Рис. 1.10. Дисульфидные связи в структуре инсулина
Рис. 1.10. Дисульфидные связи в структуре инсулина Рис. 1.11. «Лейциновая застежка-молния» между α-спиральными участками двух белков
Рис. 1.11. «Лейциновая застежка-молния» между α-спиральными участками двух белков Рис. 1.12. Первичная структура участка ДНК-связывающих белков, формирующих структуру «цинкового пальца» (буквами обозначены аминокислоты, входящие в состав этой структуры)
Рис. 1.12. Первичная структура участка ДНК-связывающих белков, формирующих структуру «цинкового пальца» (буквами обозначены аминокислоты, входящие в состав этой структуры)


